คุณสมบัติโครงสร้างอีเธอร์อีเทอร์การใช้ประโยชน์
เอทิลอีเทอร์, หรือที่เรียกว่า diethyl ether เป็นสารประกอบอินทรีย์ที่มีสูตรทางเคมีคือ C4H10O. เป็นลักษณะโดยเป็นของเหลวที่ไม่มีสีและระเหยได้ดังนั้นขวดจะต้องปิดให้สนิทที่สุด.
อีเธอร์นี้จัดว่าเป็นสมาชิกของ dialkyl ethers; นั่นคือพวกเขามีสูตร ROR 'โดยที่ R และ R' แทนส่วนคาร์บอนที่แตกต่างกัน และตามที่อธิบายชื่อกลางของมันคือ diethyl ether เป็นอนุมูลสองตัว - เอทิลที่จับกับอะตอมของออกซิเจน.

อีเทอร์อีเทอร์เริ่มแรกถูกนำมาใช้เป็นยาชาทั่วไปนำมาใช้ในปี 1846 โดยวิลเลียมโทมัสกรีนมอร์ตัน อย่างไรก็ตามเนื่องจากความไวไฟการใช้งานจึงถูกปฏิเสธแทนที่ด้วยยาชาที่อันตรายน้อยกว่า.
สารประกอบนี้ยังถูกใช้เพื่อประเมินเวลาของการไหลเวียนโลหิตในระหว่างการประเมินสถานะของหัวใจและหลอดเลือดของผู้ป่วย.
ภายในร่างกาย diethyl ether สามารถเปลี่ยนเป็นคาร์บอนไดออกไซด์และสาร ท้ายที่สุดถูกขับออกมาทางปัสสาวะ อย่างไรก็ตามอีเทอร์ส่วนใหญ่ที่หายใจออกทางปอดโดยไม่ต้องผ่านการดัดแปลงใด ๆ.
ในทางกลับกันมันถูกใช้เป็นตัวทำละลายสำหรับสบู่น้ำมันน้ำหอมอัลคาลอยด์และเหงือก.
ดัชนี
- 1 โครงสร้างของเอทิลอีเธอร์
- 1.1 แรงระหว่างโมเลกุล
- 2 คุณสมบัติทางกายภาพและทางเคมี
- 2.1 ชื่ออื่น
- 2.2 สูตรโมเลกุล
- 2.3 น้ำหนักโมเลกุล
- 2.4 ลักษณะทางกายภาพ
- 2.5 กลิ่น
- 2.6 รสชาติ
- 2.7 จุดเดือด
- 2.8 จุดหลอมเหลว
- 2.9 จุดวาบไฟ
- 2.10 การละลายในน้ำ
- 2.11 การละลายในของเหลวอื่น ๆ
- 2.12 ความหนาแน่น
- 2.13 ความหนาแน่นไอ
- 2.14 ความดันไอ
- 2.15 ความเสถียร
- 2.16 การจุดระเบิดอัตโนมัติ
- 2.17 การสลายตัว
- 2.18 ความหนืด
- 2.19 ความร้อนจากการเผาไหม้
- 2.20 การระเหยความร้อน
- 2.21 แรงตึงผิว
- 2.22 ไอออไนเซชันที่มีศักยภาพ
- 2.23 เกณฑ์กลิ่น
- 2.24 ดัชนีการหักเหของแสง
- 3 การได้รับ
- 3.1 จากเอทิลแอลกอฮอล์
- 3.2 จากเอทิลีน
- 4 ความเป็นพิษ
- 5 ใช้
- 5.1 ตัวทำละลายอินทรีย์
- 5.2 การดมยาสลบ
- 5.3 วิญญาณของอีเธอร์
- 5.4 การประเมินการไหลเวียนโลหิต
- 5.5 การสอนในห้องปฏิบัติการ
- 6 อ้างอิง
โครงสร้างของ ethyl ether
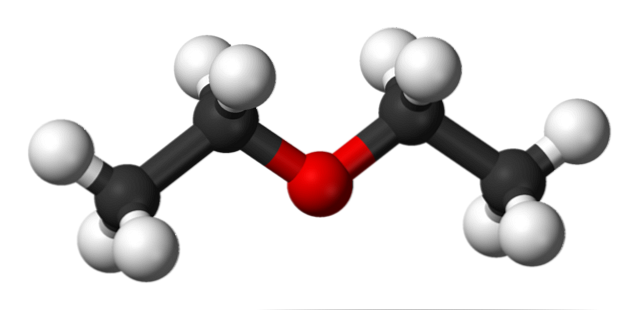
ในภาพด้านบนเรามีตัวแทนของแบบจำลองทรงกลมและแท่งของโครงสร้างโมเลกุลของเอทิลอีเทอร์.
ดังจะเห็นได้ว่าทรงกลมสีแดงซึ่งตรงกับอะตอมออกซิเจนมีกลุ่มเอทิลสองกลุ่มเชื่อมโยงกันทั้งสองด้าน ลิงก์ทั้งหมดนั้นเรียบง่ายยืดหยุ่นและหมุนได้รอบแกนσ.
การหมุนเหล่านี้มาจากสเตอริโอไอโซเมอร์ มากกว่า isomers พวกมันเป็นทางเลือกของสหรัฐฯ โครงสร้างของภาพตรงกับตัวต่อต้านผู้ต่อต้านซึ่งกลุ่มอะตอมทั้งหมดจะถูกเซ (แยกจากกัน).
คนอื่นจะเป็นคนรักอะไร บดบังและแม้ว่าภาพของคุณจะไม่สามารถใช้งานได้เพียงแค่เห็นภาพด้วยรูปตัว U ที่ปลายด้านบนของ U จะอยู่ในกลุ่มเมธิล -CH3, ซึ่งจะได้สัมผัสกับการขับไล่ steric (พวกเขาจะชนกันในอวกาศ).
ดังนั้นจึงคาดว่าโมเลกุล CH3CH2เอมโอช2CH3 นำมาใช้ต่อต้านโครงสร้างส่วนใหญ่ของเวลา.
แรงระหว่างโมเลกุล
แรงระหว่างโมเลกุลคือโมเลกุลของเอทิลอีเทอร์ภายใต้สถานะของเหลว? พวกมันถูกเก็บรักษาไว้ในของเหลวเป็นส่วนใหญ่เนื่องจากกองกำลังการกระจายเนื่องจากช่วงเวลาไดโพล (1.5D) ขาดพื้นที่ที่มีความหนาแน่นทางอิเล็กทรอนิกส์เพียงพอ (δ +)
นี่เป็นเพราะไม่มีอะตอมคาร์บอนของกลุ่มเอทิลให้ความหนาแน่นอิเล็กตรอนมากเกินไปกับอะตอมออกซิเจน ด้านบนมีแผนที่ของศักย์ไฟฟ้าสถิตของเอทิลอีเธอร์ที่มือ (ภาพล่าง) สังเกตการขาดของพื้นที่สีน้ำเงิน.
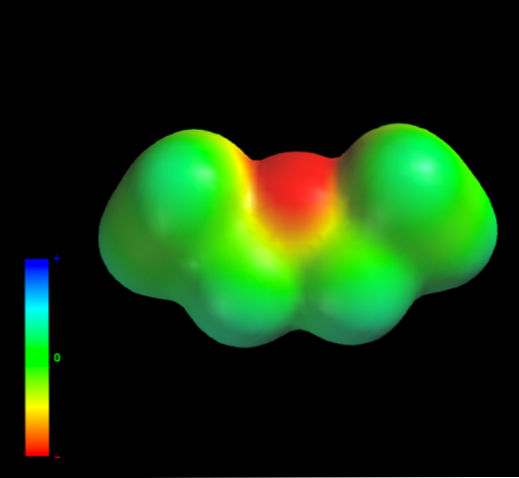
ออกซิเจนไม่สามารถสร้างพันธะไฮโดรเจนได้อีกเช่นกันเนื่องจากไม่มีพันธะ O-H ในโครงสร้างโมเลกุล ดังนั้นจึงเป็นไดโพลแบบทันทีและมวลโมเลกุลของพวกมันซึ่งเป็นที่โปรดปรานของกองกำลังกระจาย.
อย่างไรก็ตามเรื่องนี้มันสามารถละลายในน้ำได้สูง ทำไม? เนื่องจากอะตอมของออกซิเจนที่มีความหนาแน่นของอิเล็กตรอนสูงกว่าสามารถรับพันธะไฮโดรเจนจากโมเลกุลของน้ำได้:
(CH3CH2)2Oδ- - δ+H-OH
ปฏิกิริยาเหล่านี้มีความรับผิดชอบ 6.04 กรัมของอีเธอร์นี้ละลายในน้ำ 100 มล.
คุณสมบัติทางกายภาพและทางเคมี
ชื่ออื่น ๆ
-Diethyl ether
-ethoxyethane
-เอทิลออกไซด์
สูตรโมเลกุล
C4H10O หรือ (C2H5)2O.
น้ำหนักโมเลกุล
74.14 กรัม / โมล.
ลักษณะทางกายภาพ
ของเหลวไม่มีสี.
กลิ่น
หวานและเผ็ด.
รสชาติ
การเผาไหม้และหวาน.
จุดเดือด
94.3 ºF (34.6 ºC) ถึง 760 mmHg.
จุดหลอมเหลว
-177.3 ºF (-116.3 ªC) ผลึกเสถียร.
จุดติดไฟ
-49ºF (ภาชนะปิด).
การละลายในน้ำ
6.04 g / 100mL ที่ 25 ºC.
การละลายในของเหลวอื่น ๆ
ผสมกับแอลกอฮอล์อะลิฟาติกสายสั้นเบนซินเบนซินคลอโรฟอร์มปิโตรเลียมอีเธอร์ตัวทำละลายไขมันน้ำมันหลายชนิดและกรดไฮโดรคลอริกเข้มข้น.
ละลายในอะซิโตนและละลายได้ในเอทานอล นอกจากนี้ยังละลายได้ในแนฟทาเบนซีนและน้ำมัน.
ความหนาแน่น
0.714 mg / mL ที่ 68 ªF (20 ºC).
ความหนาแน่นของไอ
2.55 (สัมพันธ์กับอากาศที่มีความหนาแน่น 1).
แรงดันไอน้ำ
442 mmHg ที่68ºF 538 mmHg ที่ 25 ° C 58.6 kPa ที่ 20 ºC.
ความมั่นคง
มันจะถูกออกซิไดซ์อย่างช้าๆโดยการกระทำของอากาศความชื้นและแสงด้วยการก่อตัวของเปอร์ออกไซด์.
การก่อตัวของเปอร์ออกไซด์สามารถเกิดขึ้นได้ในภาชนะอีเธอร์ที่เปิดออกและยังคงอยู่ในที่เก็บนานกว่าหกเดือน เปอร์ออกไซด์สามารถทำให้เกิดการระเบิดจากแรงเสียดทานแรงกระแทกหรือความร้อน.
หลีกเลี่ยงการสัมผัสกับ: สังกะสี, ฮาโลเจน, ออกไซด์ของโลหะที่ไม่ใช่โลหะ, ตัวออกซิไดซ์ที่แรง, chromyl chloride, น้ำมัน tementin, ไนเตรตและคลอไรด์โลหะ.
จุดระเบิดอัตโนมัติ
356ºF (180ºC).
การจำแนก
เมื่ออบอุ่นขึ้นมันจะสลายตัวปล่อยควันที่ฉุนและน่ารำคาญออกมา.
ความเหนียว
0.2448 cPoise ที่ 20 ºC.
ความร้อนจากการเผาไหม้
8,807 Kcal / g.
ความร้อนจากการระเหย
89.8 แคลอรี่ / กรัมที่ 30 ºC.
แรงตึงผิว
17.06 dynes / cm ที่20º C.
ศักย์ไฟฟ้า
9.53 eV.
เกณฑ์กลิ่น
0.83 ppm (ไม่ได้รับความบริสุทธิ์).
ดัชนีหักเห
1,355 ที่ 15 ºC.
การได้รับ
จากเอทิลแอลกอฮอล์
เอทิลอีเทอร์สามารถหาได้จากเอทิลแอลกอฮอล์ในที่ที่มีกรดซัลฟูริกเป็นตัวเร่งปฏิกิริยา กรดซัลฟิวริกในตัวกลางที่เป็นน้ำจะแยกตัวออกมาเพื่อสร้างไฮโดรเนียมไอออน3O+.
เอทิลแอลกอฮอล์ปราศจากแอลกอฮอล์จะไหลผ่านสารละลายกรดซัลฟิวริกซึ่งให้ความร้อนระหว่าง 130 ° C และ 140 ° C ทำให้เกิดการรวมตัวกันของโมเลกุลเอทิลแอลกอฮอล์ ต่อจากนั้นโมเลกุลอื่นของเอทิลแอลกอฮอล์ที่ไม่มีโปรตอนจะทำปฏิกิริยากับโมเลกุลที่ถูกสร้างขึ้น.
เมื่อสิ่งนี้เกิดขึ้นการจู่โจมของนิวคลีโอฟิลของโมเลกุลที่สองของเอทิลแอลกอฮอล์ส่งเสริมการปล่อยน้ำจากโมเลกุลแรก เป็นผลให้เกิดเอทธิลอีเทอร์แบบโปรตอน (CH3CH2OHCH2CH3) พร้อมออกซิเจนที่มีประจุเป็นบางส่วน.
อย่างไรก็ตามวิธีการสังเคราะห์นี้สูญเสียประสิทธิภาพเนื่องจากกรดซัลฟูริกเจือจางกับน้ำที่เกิดขึ้นในกระบวนการ (ผลิตภัณฑ์ของการขาดน้ำของเอทิลแอลกอฮอล์).
อุณหภูมิของปฏิกิริยามีความสำคัญ ที่อุณหภูมิต่ำกว่า 130 ° C ปฏิกิริยาจะช้าและส่วนใหญ่เอทิลแอลกอฮอล์จะถูกกลั่น.
สูงกว่า 150 ° C กรดซัลฟิวริกทำให้เกิดการก่อตัวของเอทิลีน (อัลคีนพันธะคู่) แทนที่จะรวมกับเอทิลแอลกอฮอล์เพื่อสร้างเอทิลอีเทอร์.
จากเอทิลีน
ในกระบวนการตรงกันข้ามนั่นคือการให้ความชุ่มชื้นของเอทิลีนในเฟสของไอระเหยอีเทอร์อีเทอร์สามารถเกิดเป็นผลพลอยได้นอกเหนือจากเอทิลแอลกอฮอล์ ในความเป็นจริงเส้นทางสังเคราะห์นี้ผลิตสารประกอบอินทรีย์ส่วนใหญ่.
กระบวนการนี้ใช้ตัวเร่งปฏิกิริยากรดฟอสฟอริกซึ่งจับจ้องอยู่ที่การสนับสนุนที่มั่นคงสามารถปรับตัวเพื่อผลิตอีเธอร์ได้มากขึ้น.
การคายน้ำในเฟสไอของเอทานอลต่อตัวเร่งปฏิกิริยาอะลูมินาสามารถให้ผลตอบแทน 95% ในการผลิตเอทิลอีเทอร์.
ความเป็นพิษ
สามารถสร้างการระคายเคืองต่อผิวหนังและดวงตาโดยการสัมผัส การสัมผัสกับผิวหนังสามารถทำให้แห้งและแตกได้ อีเธอร์มักจะไม่แทรกซึมผิวหนังเนื่องจากระเหยได้อย่างรวดเร็ว.
การระคายเคืองของดวงตาที่เกิดจากอีเธอร์มักจะไม่รุนแรงและในกรณีของการระคายเคืองอย่างรุนแรงความเสียหายมักจะย้อนกลับได้.
การกลืนกินของมันผลิตผลกระทบยาเสพติดและการระคายเคืองกระเพาะอาหาร การกลืนกินอย่างรุนแรงสามารถทำให้เกิดความเสียหายไต.
การสูดดมอีเธอร์อาจทำให้เกิดการระคายเคืองในจมูกและลำคอ ในกรณีที่สูดดมอีเธอร์สามารถเกิดขึ้นได้: อาการง่วงนอน, ตื่นเต้น, เวียนหัว, อาเจียน, การหายใจผิดปกติและการหลั่งน้ำลายเพิ่มขึ้น.
การเปิดรับแสงสูงอาจทำให้หมดสติและเสียชีวิตได้.
OSHA กำหนดค่า จำกัด การเปิดรับแสงโดยเฉลี่ยที่ 800 ppm ในช่วงเวลา 8 ชั่วโมง.
ระดับของการระคายเคืองที่ตา: 100 ppm (คน) ระดับของการระคายเคืองที่ตา: 1200 mg / m3 (400 ppm).
การใช้งาน
ตัวทำละลายอินทรีย์
เป็นตัวทำละลายอินทรีย์ที่ใช้ในการละลายโบรมีนไอโอดีนและฮาโลเจนอื่น ๆ ไขมันส่วนใหญ่ (ไขมัน), เรซิน, ยางบริสุทธิ์, อัลคาลอยด์บางชนิด, เหงือก, น้ำหอม, เซลลูโลสอะซิเตท, เซลลูโลสไนเตรต, ไฮโดรคาร์บอนและสีย้อม.
นอกจากนี้ยังใช้ในการสกัดหลักการทำงานของเนื้อเยื่อและพืชสัตว์เพราะมันมีความหนาแน่นต่ำกว่าน้ำและลอยอยู่บนมันทิ้งสารที่ต้องการละลายในอีเธอร์.
การดมยาสลบ
มันถูกใช้เป็นยาสลบทั่วไปตั้งแต่ปี 1840 แทนที่คลอโรฟอร์มเพื่อให้ได้เปรียบในการรักษา อย่างไรก็ตามมันเป็นสารไวไฟและดังนั้นจึงพบปัญหาร้ายแรงสำหรับการใช้งานภายในการตั้งค่าทางคลินิก.
นอกจากนี้ยังผลิตในผู้ป่วยบางผลข้างเคียงหลังผ่าตัดที่ไม่พึงประสงค์เช่นคลื่นไส้และอาเจียน.
ด้วยเหตุผลเหล่านี้การใช้อีเธอร์เป็นยาชาทั่วไปจึงถูกทิ้งไปแทนที่ด้วยยาสลบอื่น ๆ เช่น halothane.
วิญญาณของอีเธอร์
อีเทอร์ผสมกับเอทานอลถูกนำมาใช้ในการสร้างวิธีการแก้ปัญหาที่เรียกว่าวิญญาณของอีเธอร์ที่ใช้ในการรักษาอาการท้องอืดท้องอืดและรูปแบบที่รุนแรงก.
การประเมินการไหลเวียนโลหิต
อีเธอร์ถูกใช้เพื่อประเมินการไหลเวียนโลหิตระหว่างแขนและปอด อีเธอร์จะถูกฉีดเข้าไปในแขนนำเลือดไปยังห้องโถงด้านขวาจากนั้นไปที่ช่องที่ถูกต้องและจากนั้นไปยังปอด.
เวลาที่ผ่านไปจากการฉีดอีเธอร์จนถึงการดูดซับกลิ่นอีเธอร์ในอากาศที่หายใจออกมีประมาณ 4 ถึง 6 วินาที.
สอนทดลอง
อีเธอร์ใช้ในการสอนห้องปฏิบัติการในการทดลองหลาย ๆ ครั้ง ตัวอย่างเช่นในการสาธิตกฎหมายของพันธุศาสตร์เมนเดล.
อีเธอร์ใช้ในการมึนแมลงวันของสกุล Drosophila และอนุญาตให้มีการสลับที่จำเป็นระหว่างพวกเขาเพื่อที่จะนำหลักฐานกฎหมายของพันธุ
การอ้างอิง
- Graham Solomons T.W. , Craig B. Fryhle (2011) เคมีอินทรีย์ เอมีน (10TH ฉบับที่.) ไวลีย์พลัส.
- Carey F. (2008) เคมีอินทรีย์ (ฉบับที่หก) Mc Graw Hill.
- เดอะเซเวียร์ (2018) Diethyl ether วิทยาศาสตร์โดยตรง ดึงมาจาก: sciencedirect.com
- บรรณาธิการสารานุกรมบริแทนนิกา (2018) Ethyl ether Britannica ncyclopædia ดึงมาจาก: britannica.com
- PubChem (2018) อีเทอร์ สืบค้นจาก: pubchem.ncbi.nlm.nih.gov
- วิกิพีเดีย (2018) Diethyl ether สืบค้นจาก: en.wikipedia.org
- แผ่นความปลอดภัย XI: ethyl ether [PDF] กู้คืนจาก: quimica.unam.mx


