กระบวนการปฏิกิริยาคายความร้อนชนิดและตัวอย่าง
ปฏิกิริยาคายความร้อน เป็นปฏิกิริยาเคมีชนิดหนึ่งที่เกิดการถ่ายเทพลังงานส่วนใหญ่อยู่ในรูปของความร้อนหรือการปล่อยแสง ชื่อนี้มาจากคำนำหน้ากรีก นอก, ซึ่งหมายถึง "ต่างประเทศ" และคำว่า "ความร้อน" ซึ่งหมายถึงความร้อนหรืออุณหภูมิ.
ในแง่นี้ปฏิกิริยาคายความร้อนสามารถถ่ายโอนพลังงานประเภทอื่นไปยังสภาพแวดล้อมที่เกิดขึ้นเช่นการระเบิดและวิธีการถ่ายโอนพลังงานจลน์และโซนิคเมื่อสารที่อยู่ในเฟสก๊าซที่อุณหภูมิสูงขยายตัว วิธีรุนแรง.
ในทำนองเดียวกันในกรณีที่ใช้แบตเตอรี่จะมีปฏิกิริยาคายความร้อนด้วยเช่นกันเฉพาะในกรณีนี้พลังงานไฟฟ้าถูกขนส่ง.
ดัชนี
- 1 กระบวนการ
- 2 ประเภท
- 2.1 ปฏิกิริยาการเผาไหม้
- 2.2 ปฏิกิริยาการทำให้เป็นกลาง
- 2.3 ปฏิกิริยาออกซิเดชัน
- 2.4 ปฏิกิริยาของปลวก
- 2.5 ปฏิกิริยาพอลิเมอร์
- 2.6 ปฏิกิริยานิวเคลียร์ฟิชชัน
- 2.7 ปฏิกิริยาอื่น ๆ
- 3 ตัวอย่าง
- 4 อ้างอิง
กระบวนการ
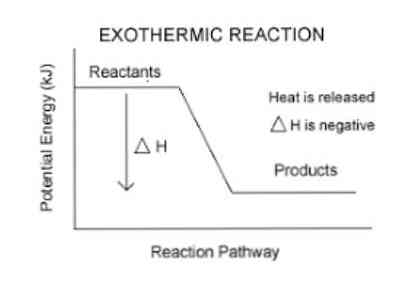
ก่อนหน้านี้มีการกล่าวถึงว่าเมื่อเกิดปฏิกิริยาคายความร้อนเกิดการปลดปล่อยพลังงานซึ่งสามารถมองเห็นได้ง่ายขึ้นในสมการต่อไปนี้:
รีเอเจนต์→ผลิตภัณฑ์ + พลังงาน
ดังนั้นในการหาปริมาณพลังงานที่ดูดซับหรือปล่อยออกมาจากระบบจะใช้พารามิเตอร์ทางอุณหพลศาสตร์เรียกว่าเอนทาลปี (แทนด้วย "H") หากในระบบ (ในกรณีนี้ปฏิกิริยาทางเคมี) มีการปลดปล่อยพลังงานไปสู่สิ่งแวดล้อมแล้วการเปลี่ยนแปลงของเอนทาลปี (แสดงเป็นΔH) จะมีค่าเป็นลบ.
มิฉะนั้นหากความแปรผันของตัววัดนี้เป็นค่าบวกจะสะท้อนการดูดซับความร้อนจากสภาพแวดล้อม นอกจากนี้ขนาดของการเปลี่ยนแปลงเอนทาลปีของระบบคือการแสดงออกของปริมาณพลังงานที่ถูกถ่ายโอนไปยังหรือจากสภาพแวดล้อม.
ยิ่งมีขนาดใหญ่ขึ้น largerH ยิ่งปล่อยพลังงานจากระบบไปยังสื่อรอบข้างมากขึ้นเท่านั้น.
นี่เป็นเพราะในปฏิกิริยาเหล่านี้พลังงานสุทธิที่ปล่อยออกมาเมื่อมีการสร้างลิงค์ใหม่มากกว่าพลังงานสุทธิที่ใช้ในการแยกส่วนของลิงก์.
จากข้างต้นสามารถสรุปได้ว่าปฏิกิริยาประเภทนี้เป็นเรื่องธรรมดามากเนื่องจากผลิตภัณฑ์ของปฏิกิริยามีปริมาณพลังงานที่เก็บไว้ในพันธะที่มีค่ามากกว่าที่มีอยู่ในสารตั้งต้น.
ชนิด
ปฏิกิริยาคายความร้อนมีหลายประเภทในสาขาเคมีต่าง ๆ ไม่ว่าจะในห้องปฏิบัติการหรือในอุตสาหกรรม บางชนิดเกิดขึ้นเองและอื่น ๆ ต้องการเงื่อนไขเฉพาะหรือสารบางชนิดเช่นตัวเร่งปฏิกิริยาที่จะสร้างขึ้น.
ต่อไปนี้เป็นปฏิกิริยาคายความร้อนที่สำคัญที่สุด:
ปฏิกิริยาการเผาไหม้
ปฏิกิริยาการเผาไหม้เป็นปฏิกิริยาประเภทรีดอกซ์ที่เกิดขึ้นเมื่อสารหนึ่งอย่างหรือมากกว่าทำปฏิกิริยากับออกซิเจนโดยทั่วไปจะส่งผลให้เกิดการปล่อยแสงและพลังงานความร้อน - นั่นคือแสงและความร้อน - เมื่อเกิดเปลวไฟ.
ปฏิกิริยาการทำให้เป็นกลาง
ปฏิกิริยาการทำให้เป็นกลางเป็นลักษณะการทำงานร่วมกันระหว่างชนิดของกรดและสารอัลคาไลน์ (ฐาน) เพื่อสร้างเกลือและน้ำซึ่งแสดงให้เห็นถึงธรรมชาติคายความร้อน.
ปฏิกิริยาออกซิเดชัน
มีปฏิกิริยาหลายชนิดในลักษณะนี้ที่แสดงพฤติกรรมคายความร้อนเนื่องจากการออกซิเดชั่นของออกซิเจนทำให้เกิดการปลดปล่อยพลังงานจำนวนมากเช่นเดียวกับการเกิดออกซิเดชันของไฮโดรคาร์บอน.
ปฏิกิริยาของปลวก
ปฏิกิริยานี้สามารถสร้างอุณหภูมิประมาณ 3000 ° C และเนื่องจากความสัมพันธ์ที่สูงของผงอะลูมิเนียมที่มีออกไซด์ของโลหะจำนวนมากจึงถูกใช้ในการเชื่อมเหล็กและเหล็ก.
ปฏิกิริยาพอลิเมอไรเซชัน
ปฏิกิริยาประเภทนี้เป็นสิ่งที่เกิดขึ้นเมื่อสารเคมีชนิดหนึ่งเรียกว่าโมโนเมอร์ทำปฏิกิริยาซึ่งเป็นหน่วยที่เมื่อรวมกันถูกทำซ้ำในโซ่เพื่อสร้างโครงสร้างโมเลกุลที่เรียกว่าโพลีเมอร์.
ปฏิกิริยานิวเคลียร์ฟิชชัน
กระบวนการนี้หมายถึงการแบ่งนิวเคลียสของอะตอมที่ถือว่าหนัก - นั่นคือมีจำนวนมวล (A) มากกว่า 200 - เพื่อผลิตชิ้นส่วนหรือนิวเคลียสที่มีขนาดเล็กลงที่มีมวลปานกลาง.
ในปฏิกิริยานี้เมื่อเกิดนิวตรอนหนึ่งตัวขึ้นไปพลังงานจำนวนมากจะถูกปล่อยออกมาเพราะแกนที่มีน้ำหนักมากกว่ามีความเสถียรต่ำกว่าผลิตภัณฑ์.
ปฏิกิริยาอื่น ๆ
นอกจากนี้ยังมีปฏิกิริยาคายความร้อนอื่น ๆ ที่เกี่ยวข้องอย่างมากเช่นการคายน้ำของคาร์โบไฮเดรตบางอย่างเมื่อทำปฏิกิริยากับกรดซัลฟูริกการดูดซึมของน้ำที่มีโซเดียมไฮดรอกไซด์สัมผัสกับอากาศเปิดหรือการออกซิเดชั่นของโลหะชนิดต่างๆ.
ตัวอย่าง
ด้านล่างเป็นตัวอย่างของปฏิกิริยาคายความร้อนซึ่งก่อให้เกิดการเปลี่ยนแปลงของเอนทัลปีที่มีค่าเป็นลบเนื่องจากความจริงที่ว่าพวกเขาปล่อยพลังงานดังที่กล่าวไว้ข้างต้น.
ตัวอย่างเช่นการเผาไหม้ของโพรเพนเป็นปฏิกิริยาคายความร้อนที่เกิดขึ้นเอง:
C3H8(g) + 5O2(g) → 3CO2(g) + 4H2O (l)
อีกกรณีของพฤติกรรมคายความร้อนแสดงโดยปฏิกิริยาการทำให้เป็นกลางระหว่างโซเดียมคาร์บอเนตและกรดไฮโดรคลอริก:
NaHCO3(ac) + HCl (ac) → NaCl (ac) + H2O (l) + CO2(G)
การเกิดออกซิเดชันของเอธานอลต่อกรดอะซิติกที่ใช้ในเครื่องวิเคราะห์ลมหายใจก็แสดงให้เห็นซึ่งปฏิกิริยาที่สมบูรณ์จะแสดงในสมการต่อไปนี้:
3CH3CH2OH + 2K2Cr2O7 + 8H2SW4 → CH3COOH + 2Cr (SO4)3 + 2K2SW4 + 11H2O
ปฏิกิริยาคายความร้อนอีกประเภทหนึ่งคือปฏิกิริยาที่เรียกว่าเทอร์ไมต์ซึ่งอลูมิเนียมผสมกับโลหะออกไซด์ดังตัวอย่างด้านล่าง:
2Al (s) + ศรัทธา2O3(s) →อัล2O3(s) + Fe (l)
นอกเหนือจากตัวอย่างที่อธิบายข้างต้นแล้วยังมีปฏิกิริยาที่หลากหลายซึ่งถือว่าเป็นการคายความร้อนเช่นการสลายตัวของสารอินทรีย์บางชนิดเพื่อการทำปุ๋ยหมัก.
มันยังเน้นการเกิดออกซิเดชันของ luciferin รงควัตถุโดยการกระทำของเอนไซม์ luciferase ในการผลิตลักษณะ bioluminescence ของหิ่งห้อยและแม้แต่การหายใจในปฏิกิริยาอื่น ๆ อีกมากมาย.
การอ้างอิง
- วิกิพีเดีย ( N.d. ) ปฏิกิริยาคายความร้อน สืบค้นจาก es.wikipedia.org
- บีบีซี ( N.d. ) การเปลี่ยนแปลงพลังงานและปฏิกิริยาย้อนกลับ เรียกดูจาก bbc.co.uk
- ช้างอาร์ (2550) เคมีรุ่นที่เก้า (McGraw-Hill).
- Walker, D. (2007) ปฏิกิริยาเคมี ดึงมาจาก books.google.co.th
- Saunders, N. (2007) สำรวจปฏิกิริยาเคมี ดึงมาจาก books.google.co.th


