รัศมีอะตอมเป็นวิธีการวัดการเปลี่ยนแปลงในตารางธาตุตัวอย่าง
รัศมีอะตอม มันเป็นพารามิเตอร์ที่สำคัญสำหรับคุณสมบัติเป็นระยะขององค์ประกอบของตารางธาตุ มันเกี่ยวข้องโดยตรงกับขนาดของอะตอมเนื่องจากในรัศมีที่มากขึ้นมีขนาดใหญ่หรือใหญ่ ในทำนองเดียวกันมันมีความเกี่ยวข้องกับลักษณะทางอิเล็กทรอนิกส์ของเดียวกัน.
ตราบใดที่อะตอมมีอิเล็กตรอนมากขึ้นขนาดและรัศมีของอะตอมก็จะยิ่งมากขึ้น ทั้งสองถูกกำหนดโดยอิเล็กตรอนของเปลือกวาเลนซ์เพราะในระยะทางไกลกว่าวงโคจรของพวกเขาความน่าจะเป็นของการหาอิเล็กตรอนเข้าใกล้ศูนย์ ตรงกันข้ามเกิดขึ้นในบริเวณใกล้เคียงของนิวเคลียส: ความน่าจะเป็นในการหาอิเล็กตรอนเพิ่มขึ้น.

ภาพด้านบนแสดงถึงบรรจุภัณฑ์ของสำลีก้อน โปรดทราบว่าแต่ละอันล้อมรอบด้วยเพื่อนบ้านหกคนโดยไม่นับแถวบนหรือแถวล่างที่เป็นไปได้อื่น ๆ วิธีที่ลูกบอลฝ้ายถูกบีบอัดจะกำหนดขนาดและรัศมีของมัน เหมือนกับที่มันเกิดขึ้นกับอะตอม.
องค์ประกอบตามลักษณะทางเคมีของพวกมันมีปฏิสัมพันธ์กับอะตอมของตัวเองไม่ทางใดก็ทางหนึ่ง ดังนั้นขนาดของรัศมีอะตอมจึงแตกต่างกันไปตามประเภทของพันธะที่มีอยู่และการบรรจุที่เป็นของแข็งของอะตอม.
ดัชนี
- 1 วัดรัศมีของอะตอมอย่างไร?
- 1.1 การหาระยะทางนิวเคลียร์
- 1.2 หน่วย
- 2 มันมีการเปลี่ยนแปลงในตารางธาตุอย่างไร?
- 2.1 ช่วงเวลาหนึ่ง
- 2.2 จากมากไปน้อยโดยกลุ่ม
- 2.3 Lanthanide contraction
- 3 ตัวอย่าง
- 4 อ้างอิง
วัดรัศมีของอะตอมอย่างไร?
ในภาพหลักนั้นสามารถวัดเส้นผ่านศูนย์กลางของลูกฝ้ายได้ง่ายแล้วหารด้วยสอง อย่างไรก็ตามทรงกลมของอะตอมไม่ได้ถูกกำหนดอย่างสมบูรณ์ ทำไม? เนื่องจากอิเล็กตรอนไหลเวียนและแพร่กระจายในพื้นที่เฉพาะของพื้นที่: orbitals.
ดังนั้นอะตอมจึงถือได้ว่าเป็นทรงกลมที่มีขอบที่ไม่สามารถต้านทานได้ซึ่งเป็นไปไม่ได้ที่จะพูดได้อย่างแน่นอนถึงสิ่งที่พวกมันสิ้นสุด ตัวอย่างเช่นในภาพด้านบนบริเวณกึ่งกลางใกล้กับนิวเคลียสจะมีสีที่เข้มกว่าในขณะที่ขอบเบลอ.
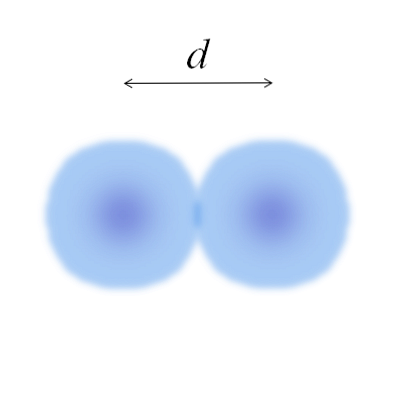
ภาพแสดงโมเลกุลไดอะตอมมิก2 (เช่นเดียวกับ Cl2, H2, O2, ฯลฯ ) สมมติว่าอะตอมเป็นวัตถุทรงกลมหากระยะทางถูกกำหนด d ที่แยกนิวเคลียสทั้งสองในพันธะโควาเลนต์แล้วมันจะเพียงพอที่จะแบ่งออกเป็นสองส่วน (d/ 2) เพื่อให้ได้รัศมีอะตอม แม่นยำยิ่งขึ้นรัศมีโควาเลนต์ของ E สำหรับ E2.
และถ้า E ไม่ได้สร้างพันธะโควาเลนต์ด้วยตัวเอง แต่มันเป็นองค์ประกอบที่เป็นโลหะ? แล้วก็ d มันจะถูกระบุด้วยจำนวนเพื่อนบ้านที่ล้อมรอบ E ในโครงสร้างโลหะของมัน นั่นคือโดยหมายเลขการประสานงาน (N.C) ของอะตอมภายในบรรจุภัณฑ์ (จดจำลูกฝ้ายของภาพหลัก).
การกำหนดระยะทางนิวเคลียร์
เพื่อตรวจสอบ d, ซึ่งเป็นระยะทางนิวเคลียร์สำหรับสองอะตอมในโมเลกุลหรือบรรจุภัณฑ์มันต้องใช้เทคนิคการวิเคราะห์ทางกายภาพ.
หนึ่งในสิ่งที่ใช้กันมากที่สุดคือการเลี้ยวเบนของรังสีเอกซ์ในลำแสงนั้นฉายรังสีผ่านผลึกและศึกษารูปแบบการเลี้ยวเบนซึ่งเป็นผลมาจากปฏิกิริยาระหว่างอิเล็กตรอนและรังสีแม่เหล็กไฟฟ้า สามารถรับรูปแบบการเลี้ยวเบนที่แตกต่างกันและขึ้นอยู่กับการบรรจุดังนั้นค่าอื่น ๆ ของ d.
หากอะตอมนั้น "ตึง" ในตาข่ายคริสตัลพวกเขาจะแสดงค่าที่แตกต่างกันของ d เปรียบเทียบกับสิ่งที่พวกเขาจะได้ถ้าพวกเขา "สบาย" ยิ่งไปกว่านั้นระยะทางนิวเคลียร์เหล่านี้อาจแกว่งไปมาในค่าดังนั้นรัศมีอะตอมประกอบด้วยค่าเฉลี่ยของการวัดดังกล่าว.
รัศมีอะตอมและหมายเลขพิกัดมีความสัมพันธ์กันอย่างไร V. Goldschmidt สร้างความสัมพันธ์ระหว่างทั้งสองซึ่งใน N.C ที่ 12 มีค่าสัมพัทธ์เท่ากับ 1 จาก 0.97 สำหรับการบรรจุที่อะตอมมีค่า NC เท่ากับ 8 0.96 ของ, สำหรับ N.C เท่ากับ 6; และ 0.88 สำหรับ N.C ของ 4.
หน่วย
จากค่าของ N.C เท่ากับ 12 มีการสร้างตารางจำนวนมากเปรียบเทียบรัศมีอะตอมมิกขององค์ประกอบทั้งหมดของตารางธาตุ.
เนื่องจากไม่ใช่องค์ประกอบทั้งหมดที่มีโครงสร้างที่กะทัดรัดเช่นนี้ (N.C น้อยกว่า 12) ความสัมพันธ์ของ V. Goldschmidt จะใช้ในการคำนวณรัศมีอะตอมของมันและแสดงมันสำหรับการบรรจุเดียวกัน ด้วยวิธีนี้การวัดของรัศมีอะตอมจึงเป็นมาตรฐาน.
แต่พวกเขาแสดงออกในหน่วยใด? ที่กำหนดว่า d มีขนาดเล็กมากควรใช้กับหน่วยอังสตรอม (∙ 10 ∙ 10)-10m) หรือใช้กันอย่างแพร่หลาย picometer (10 ∙ 10-12เมตร).
มันเปลี่ยนไปอย่างไรในตารางธาตุ?
ตลอดระยะเวลาหนึ่ง
รัศมีอะตอมที่กำหนดสำหรับองค์ประกอบโลหะจะได้รับชื่อรัศมีโลหะในขณะที่องค์ประกอบที่ไม่ใช่โลหะนั้นรัศมีโควาเลนต์ (เช่นฟอสฟอรัส, P4, หรือกำมะถัน8) อย่างไรก็ตามระหว่างวิทยุทั้งสองประเภทมีความโดดเด่นมากกว่าชื่อ.
จากซ้ายไปขวาในช่วงเวลาเดียวกันนิวเคลียสจะเพิ่มโปรตอนและอิเล็กตรอน แต่ส่วนหลังจะถูก จำกัด อยู่ที่ระดับพลังงานเดียวกัน (จำนวนควอนตัมหลัก) เป็นผลให้นิวเคลียสออกแรงประจุที่มีประสิทธิภาพเพิ่มขึ้นบนอิเล็กตรอนของวาเลนซ์ซึ่งจะทำสัญญากับรัศมีอะตอม.
ด้วยวิธีนี้ธาตุที่ไม่ใช่โลหะในช่วงเวลาเดียวกันมีแนวโน้มที่จะมีขนาดเล็กกว่าโลหะ (โควาเลนต์) อะตอม (โควาเลนต์).
จากมากไปน้อยโดยกลุ่ม
เมื่อลดระดับลงโดยกลุ่มระดับพลังงานใหม่จะเปิดใช้งานซึ่งช่วยให้อิเล็กตรอนมีพื้นที่มากขึ้น ดังนั้นคลาวด์อิเล็กทรอนิกส์จึงครอบคลุมระยะทางที่ไกลกว่านั้นเส้นขอบเบลอของมันจะเคลื่อนตัวออกห่างจากนิวเคลียสมากขึ้นดังนั้นรัศมีของอะตอมจึงขยายตัว.
Lanthanide หดตัว
อิเล็กตรอนของชั้นในช่วยป้องกันประจุนิวเคลียร์ที่มีประสิทธิภาพบนอิเล็กตรอนของวาเลนซ์ เมื่อวงโคจรที่ประกอบขึ้นเป็นชั้นในนั้นมี "รู" (โหนด) มากมายเช่นเดียวกับวงโคจร f นิวเคลียสจึงหดตัวอย่างรุนแรงในรัศมีของอะตอมเนื่องจากการป้องกันที่ไม่ดีของวงโคจร.
ความจริงเรื่องนี้เป็นหลักฐานในการหดตัวของแลนทาไนด์ในช่วงเวลาที่ 6 ของตารางธาตุ จาก La ถึง Hf มีการหดตัวของรัศมีอะตอมจำนวนมากที่ผลิตโดย orbitals f ซึ่ง "เติม" เป็นหนึ่งผ่านบล็อก f: ของ lanthanoids และ actinoids.
ผลที่คล้ายกันสามารถสังเกตได้ด้วยองค์ประกอบของบล็อก p จากช่วงเวลา 4 เวลานี้ผลิตภัณฑ์ของผลการป้องกันที่อ่อนแอของ orbitals d ที่เติมขึ้นเมื่อข้ามช่วงเวลาของการเปลี่ยนแปลงโลหะ.
ตัวอย่าง
สำหรับช่วงเวลา 2 ของตารางธาตุรัศมีอะตอมมิกขององค์ประกอบคือ
-หลี่: 257 น
-เป็น: 112 น
-B: 88 น
-C: 77 น
-ไม่มี: 74 น
-O: 66 น
-F: 64 น.
โปรดทราบว่าโลหะลิเธียมมีรัศมีอะตอมที่ใหญ่ที่สุด (257 ppm) ในขณะที่ฟลูออรีนตั้งอยู่ที่ด้านขวาสุดของรอบระยะเวลานั้นมีขนาดเล็กที่สุดของพวกเขา (64 ppm) รัศมีอะตอมลดลงจากซ้ายไปขวาในช่วงเวลาเดียวกันและค่าที่อยู่ในรายการจะแสดง.
ลิเธียมโดยการสร้างพันธะโลหะรัศมีของมันคือโลหะ และฟลูออรีนเนื่องจากเป็นพันธะโควาเลนต์ (F-F) รัศมีของมันคือโควาเลนต์.
และถ้าคุณต้องการที่จะแสดงวิทยุปรมาณูในหน่วยของอังสตรอม? เพียงหารด้วย 100: (257/100) = 2.57Å และอื่น ๆ ด้วยค่าที่เหลือ.
การอ้างอิง
- เคมี 301. อะตอมเรเดียม สืบค้นจาก: ch301.cm.utexas.edu
- มูลนิธิ CK-12 (28 มิถุนายน 2016) รัศมีอะตอม ดึงมาจาก: chem.libretexts.org
- แนวโน้มของอะตอมเรดิ นำมาจาก: intro.chem.okstate.edu
- วิทยาลัยชุมชนแคลกามัส (2002) ขนาดอะตอม สืบค้นจาก: dl.clackamas.edu
- Clark J. (สิงหาคม 2555) อะตอมและอิออนรัศมี สืบค้นจาก: chemguide.co.uk
- ตัวสั่นและแอตกินส์ (2008) เคมีอนินทรีย์ (ฉบับที่สี่, หน้า 23, 24, 80, 169) Mc Graw Hill.


