โครงสร้างอะลูมิเนียมซัลเฟต (Al2 (SO4) 3) ชนิดการใช้งานความเป็นพิษ
อะลูมิเนียมซัลเฟต เป็นเกลืออลูมิเนียมอนินทรีย์ของสูตรอัล2(ดังนั้น4)3, ที่มักจะปรากฏเป็นของแข็งสีขาวด้วยคริสตัลเงา สีของสารประกอบจะได้รับอิทธิพลจากความเข้มข้นของเหล็กและสิ่งเจือปนอื่น ๆ อลูมิเนียมซัลเฟตมีสองประเภทหลัก: A และ B.
ในภาพด้านล่างผลึกสีขาวของอะลูมิเนียมไฮเดรตจะถูกแสดง การไม่มีสีน้ำตาลบ่งบอกถึงไอออนของเหล็กภายในโครงผลึกนั้นสามารถสังเกตได้.

อะลูมิเนียมซัลเฟตเป็นเกลือที่ละลายได้ในน้ำและในธรรมชาติจะหาได้ยากในรูปของแอนไฮ มันมักจะถูกไฮเดรตในรูปของ octadecahydrate Aluminium sulfate [Al2(ดังนั้น4)3.18h2O] หรือ hexadecahydrate [Al2(ดังนั้น4)3.16H2O].
ในทำนองเดียวกันมันสามารถสร้างเกลือคู่กับโพแทสเซียมและแอมโมเนียมสารประกอบที่เรียกว่าลัม ในส่วนนี้อาจเกิดจากความสัมพันธ์ของน้ำภายในไฮเดรตเพื่อกักเก็บไอออนอื่น ๆ นอกเหนือจากอลูมิเนียม.
อะลูมิเนียมซัลเฟตสามารถย่อยสลายได้โดยการกระทำของน้ำในอลูมิเนียมไฮดรอกไซด์และกรดซัลฟูริก คุณสมบัตินี้ได้รับอนุญาตให้ใช้เป็นกรดของดิน.
นอกจากนี้ยังเป็นสารประกอบที่เป็นพิษโดยเฉพาะเมื่อสัมผัสกับผง อย่างไรก็ตามมันมีขอบเขตการใช้งานและแอพพลิเคชั่นที่เปลี่ยนไปจากการทำให้บริสุทธิ์ของน้ำด้วยวิธีการจับตัวที่เกิดขึ้นผ่านการใช้งานในหลายอุตสาหกรรมจนกระทั่งการใช้งานมีวัตถุประสงค์เพื่อการบำบัด.
ดัชนี
- 1 โครงสร้าง
- 2 มันคืออะไรสำหรับ (ใช้)
- 2.1 การแข็งตัวหรือการตกตะกอนของน้ำ
- 2.2 ใช้เป็นส่วนผสมของหมึกและในรายละเอียดของกระดาษ
- 2.3 ใช้ในอุตสาหกรรม
- 2.4 การใช้ยาและการรักษา
- 2.5 การใช้งานอื่น ๆ
- 3 การผลิตอะลูมิเนียมซัลเฟต
- 4 ประเภท
- 5 ความเป็นพิษ
- 6 อ้างอิง
โครงสร้าง
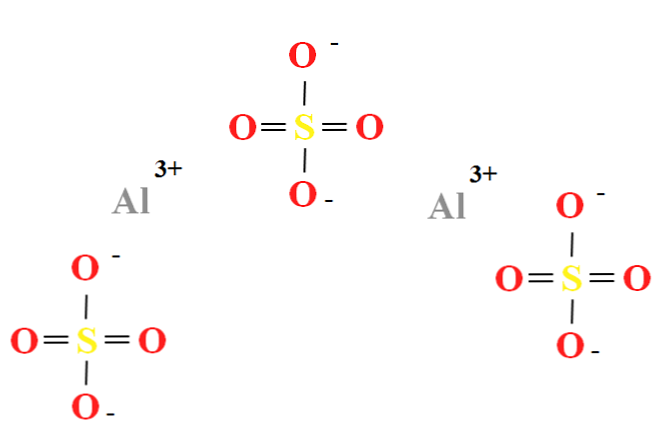
อะลูมิเนียมซัลเฟตมีอัตราส่วนของประจุบวกสองตัว3+ สำหรับทุก ๆ สามแอนไอออนดังนั้น42- (ภาพบนสุด) ซึ่งสามารถสังเกตได้โดยตรงในสูตรทางเคมีของอัล2(ดังนั้น4)3.
โปรดทราบว่าอัล3+ พวกเขาเป็นสีเทาในขณะที่ดังนั้น42- พวกมันเป็นสีเหลือง (สำหรับอะตอมกำมะถัน) และสีแดง (สำหรับอะตอมออกซิเจน).
โครงสร้างที่แสดงนั้นสอดคล้องกับรูปแบบของแอล2(ดังนั้น4)3, เนื่องจากไม่มีโมเลกุลของน้ำทำปฏิกิริยากับไอออน อย่างไรก็ตามในไฮเดรตของคุณน้ำสามารถถูกดึงดูดไปยังศูนย์กลางเชิงบวกของอัล3+, หรือโดยลบดังนั้น tetrahedra42- ผ่านพันธะไฮโดรเจน (HOH-O-SO)32-).
อัล2(ดังนั้น4)3∙ 18H2หรือตัวอย่างเช่นมันมี 18 โมเลกุลของน้ำในโครงสร้างที่เป็นของแข็ง บางคนอาจสัมผัสโดยตรงกับอัล3+ หรือด้วย SO42-. กล่าวอีกนัยหนึ่ง: อลูมิเนียมซัลเฟตสามารถมีน้ำประสานภายในหรือภายนอก.
นอกจากนี้โครงสร้างของมันยังสามารถรองรับไอออนบวกอื่น ๆ เช่น Fe3+, นา+, K+, เป็นต้น แต่สำหรับสิ่งนี้จำเป็นที่จะต้องมีแอนไอออนเพิ่มเติม42-. เพื่ออะไร เพื่อต่อต้านการเพิ่มขึ้นของประจุบวกเนื่องจากสิ่งสกปรกโลหะ.
อะลูมิเนียมซัลเฟตสามารถมีโครงสร้างได้หลายอย่างถึงแม้ว่าไฮเดรตของมันจะมีแนวโน้มที่จะนำระบบผลึก monoclinic.
คุณสมบัติทางกายภาพและทางเคมี
การปรากฏ
มันจะปรากฏเป็นของแข็งที่มีผลึกสีขาวเป็นประกายเม็ดหรือผง.
น้ำหนักโมเลกุล
342.31 g / mol (ปราศจากน้ำ).
กลิ่น
มันไม่มีกลิ่น
รสชาติ
รสหวานฝาดปานกลาง.
จุดหลอมเหลว
770 an C แบบฟอร์ม anhydrous (แบบฟอร์ม octadecahidratada 86.5º C)
การละลายในน้ำ
31.2 g / 100 ml ที่ 0 ° C; 36.4 g / 100 ml ที่ 20 ° C และ 89 g / 100 ml ที่ 100 ° C.
ความหนาแน่น
2.67 ถึง 2.71 g / cm3.
สามารถในการละลาย
ละลายได้เล็กน้อยในแอลกอฮอล์เอทิล.
แรงดันไอน้ำ
เป็นศูนย์.
ความมั่นคง
มีความเสถียรในอากาศ.
การจำแนก
เมื่อถูกความร้อนที่จุดหลอมเหลวประมาณนั้นจะสามารถสลายตัวได้โดยการเปล่งโดยเฉพาะอย่างยิ่งซัลเฟอร์ออกไซด์ซึ่งเป็นก๊าซพิษ.
กัดกร่อน
สารละลายอลูมิเนียมซัลเฟตมีการกัดกร่อนกับอลูมิเนียม สารประกอบยังสามารถกัดกร่อนโลหะในที่ที่มีความชื้น.
pKa
3.3 ถึง 3.6 และค่า pH ของมันอยู่ที่ 2.9 หรือมากกว่าในสารละลาย 5%.
มีไว้สำหรับอะไร (ใช้)
การแข็งตัวหรือการตกตะกอนของน้ำ
-เมื่อผสมกับน้ำ (ดื่มได้, เสิร์ฟหรือขยะ) อลูมิเนียมซัลเฟตทำให้เกิดอะลูมิเนียมไฮดรอกไซด์ซึ่งเกิดสารประกอบเชิงซ้อนกับสารประกอบและอนุภาคในสารละลายที่เร่งการตกตะกอนซึ่งในกรณีที่ไม่มีการรักษาด้วยอลูมิเนียมซัลเฟต เวลานาน.
-อะลูมิเนียมซัลเฟตยังใช้ในการทำความสะอาดน้ำในสระว่ายน้ำ.
-ด้วยการใช้อะลูมิเนียมซัลเฟตจะได้น้ำที่ไม่มีความขุ่นและสีช่วยเพิ่มความสามารถในการทำความสะอาดด้วยน้ำ น่าเสียดายที่วิธีการทำให้บริสุทธิ์นี้สามารถทำให้ความเข้มข้นของอลูมิเนียมเพิ่มขึ้นเล็กน้อยในน้ำ.
-อลูมิเนียมเป็นโลหะที่มีพิษมากซึ่งสะสมอยู่ในผิวหนังสมองและปอดทำให้เกิดความผิดปกติอย่างรุนแรง นอกจากนี้ยังไม่ทราบว่าฟังก์ชั่นตอบสนองในสิ่งมีชีวิต.
-สหภาพยุโรปกำหนดให้ปริมาณสูงสุดของอลูมิเนียมในน้ำไม่เกิน 0.2 มก. / ล. ในขณะเดียวกันหน่วยงานคุ้มครองสิ่งแวดล้อมของสหรัฐอเมริกากำหนดว่าขีด จำกัด การปนเปื้อนของน้ำสูงสุดที่มีอลูมิเนียมจะต้องไม่เกิน 0.05-0.2 mg / l.
-การบำบัดน้ำเสียหรือใช้ร่วมกับอะลูมิเนียมซัลเฟตช่วยให้สามารถกำจัดหรือลดฟอสฟอรัสในตัวพวกมันในเชิงเศรษฐกิจ.
ใช้เป็นหมึกในปริมาณมากและในรายละเอียดของกระดาษ
-อะลูมิเนียมซัลเฟตถูกใช้เป็นสารเติมแต่งสำหรับสีย้อมหรือหมึกช่วยในการยึดติดกับวัสดุที่จะย้อม การดำเนินการแก้ไขของมันเกิดจาก Al (OH)3, ซึ่งความเหนียวของเจลาตินมีส่วนช่วยในการดูดซับสีย้อมบนสิ่งทอ.
-แม้ว่าจะถูกนำมาใช้ตั้งแต่ประมาณ 2,000 ปีก่อนคริสต์ศักราชเพื่อวัตถุประสงค์ที่อธิบายไว้ แต่สีย้อมอินทรีย์เท่านั้นที่จำเป็นต้องมี mordants ในทางตรงกันข้ามสีสังเคราะห์ไม่จำเป็นต้องมีสารเติมแต่งอาหารเพื่อเติมเต็มการทำงานของมัน.
-มันถูกแทนที่จากการผลิตกระดาษ แต่ก็ยังคงใช้ในการผลิตเยื่อกระดาษ กำจัดสิ่งสกปรกรวมทั้งใช้ผูกวัสดุปรับสภาพของประจุและขัดสนขัดสน.
ใช้ในอุตสาหกรรม
-มันถูกใช้ในอุตสาหกรรมการก่อสร้างเพื่อเร่งการตั้งค่าของคอนกรีต นอกจากนี้ยังใช้ในการกันน้ำของอาคาร.
-ในอุตสาหกรรมสบู่และไขมันใช้ในการผลิตกลีเซอรีน.
-มันถูกใช้ในอุตสาหกรรมน้ำมันในการผลิตตัวเร่งปฏิกิริยาสังเคราะห์ที่ใช้ในระหว่างการดำเนินการ.
-มันถูกใช้ในอุตสาหกรรมยาเป็นยาสมานแผลในการเตรียมยาและเครื่องสำอาง.
-แทรกแซงในการผลิตสีย้อมเช่นสีแดงเข้ม มันยังใช้เป็นสีย้อมในการผลิตยางสังเคราะห์ของบิวทาไดอีนสไตรีน.
-ในอุตสาหกรรมการผลิตน้ำตาลจะใช้เป็นเครื่องกรองกากน้ำตาลสำหรับอ้อย.
-มันถูกใช้ในการผลิตยาดับกลิ่น ทำไม? เพราะมันทำให้ท่อของต่อมเหงื่อลดลงจึง จำกัด การสะสมของเหงื่อซึ่งเป็นสื่อที่จำเป็นสำหรับการเจริญเติบโตของแบคทีเรียที่ทำให้เกิดกลิ่น.
-มันถูกใช้ในการฟอกหนังซึ่งเป็นกระบวนการที่จำเป็นสำหรับการใช้งาน นอกจากนี้ยังใช้ในการผลิตปุ๋ย.
-มันถูกใช้เป็นสารเติมแต่งในการจัดทำสีกาวและสารผนึกรวมถึงผลิตภัณฑ์ทำความสะอาดและดูแลสำหรับเฟอร์นิเจอร์.
การใช้ยาและการรักษา
-อะลูมิเนียมซัลเฟตเป็นส่วนประกอบเสริมทางภูมิคุ้มกัน ดังนั้นจึงตอบสนองการทำงานของการประมวลผลแอนติเจนในลักษณะที่เมื่อปล่อยออกมาในบริเวณที่มีการกระทำพวกมันจะผลิตแอนติบอดีที่สร้างแอนติเจนให้กับแอนติเจนที่มากขึ้น.
-adjuvant และ BCG รวมถึง adjuvants อื่น ๆ รวมถึง endogenous เช่น interleukins นั้นไม่เฉพาะเจาะจงสำหรับแอนติเจนทำให้เพิ่มรัศมีของการทำงานของระบบภูมิคุ้มกัน สิ่งนี้ได้อนุญาตให้มีการพัฒนาวัคซีนป้องกันโรคต่าง ๆ.
-การกระทำที่จับตัวเป็นก้อนของอะลูมิเนียมซัลเฟตทำให้สามารถกำจัดไวรัสจำนวนมากในน้ำที่ผ่านการบำบัดเช่น Q beta, MS2, T4 และ P1 ผลการวิจัยพบว่าการบำบัดน้ำด้วยอะลูมิเนียมซัลเฟตทำให้เกิดไวรัสที่ไม่ทำงาน.
-อะลูมิเนียมซัลเฟตใช้ในรูปแบบของแท่งหรือเป็นผงในการรักษาบาดแผลเล็ก ๆ หรือรอยถลอกเล็ก ๆ ที่เกิดขึ้นเมื่อโกนหนวด.
-มันถูกใช้ในการผลิตอะลูมิเนียมอะซิเตทซึ่งเป็นสารประกอบที่ใช้ในการรักษาสภาพของหู มันยังถูกนำมาใช้โดยไม่ประสบความสำเร็จอย่างมีนัยสำคัญในการบรรเทาผลกระทบจากการถูกมดกัดไฟ.
-ใช้สารละลายอะลูมิเนียมซัลเฟตที่ความเข้มข้น 5% ถึง 10% ในการรักษาแผลที่สามารถควบคุมการหลั่งได้.
-การกระทำที่สมานของอลูมิเนียมซัลเฟตทำสัญญาชั้นผิวเผินจับเป็นก้อนโปรตีนและสมานแผล.
การใช้งานอื่น ๆ
-อะลูมิเนียมซัลเฟตช่วยในการควบคุมการเจริญเติบโตของสาหร่ายในบ่อทะเลสาบและลำธารน้ำ มันยังใช้ในการกำจัดหอยหมู่คนอื่น ๆ ทากสเปน.
-ชาวสวนใช้สารนี้ในการทำให้เป็นด่างดินที่เป็นกรด เมื่อสัมผัสกับน้ำอะลูมิเนียมซัลเฟตจะถูกย่อยสลายเป็นอลูมิเนียมไฮดรอกไซด์และกรดซัลฟิวริกเจือจาง จากนั้นอะลูมิเนียมไฮดรอกไซด์ตกตะกอนปล่อยกรดซัลฟิวริกไว้ในสารละลาย.
-ความเป็นกรดของดินเนื่องจากกรดซัลฟิวริกนั้นถูกมองเห็นได้ในแนวความคิดสร้างสรรค์อย่างมากเนื่องจากพืชมีชื่อว่าไฮเดรนเยียซึ่งดอกไม้เปลี่ยนเป็นสีน้ำเงินเมื่อมีดินที่เป็นกรด กล่าวคือพวกมันมีความไวและตอบสนองต่อการเปลี่ยนแปลงค่า pH.
-อะลูมิเนียมซัลเฟตมีส่วนเกี่ยวข้องในการผลิตโฟมเพื่อต่อสู้และควบคุมไฟ อย่างไร? ทำปฏิกิริยากับโซเดียมไบคาร์บอเนตทำให้เกิดการปลดปล่อย CO2. แก๊สนี้บล็อกการเข้าถึง O2 ไปยังเว็บไซต์การเผาไหม้ของวัสดุ; และส่งผลให้หยุดยิงที่กำลังพัฒนา.
ผลิตอลูมิเนียมซัลเฟต
อะลูมิเนียมซัลเฟตถูกสังเคราะห์โดยทำปฏิกิริยากับสารประกอบที่มีอลูมิเนียมเช่นแร่บอกไซต์ด้วยกรดซัลฟิวริกที่อุณหภูมิสูงขึ้น สมการทางเคมีต่อไปนี้แสดงถึงปฏิกิริยา:
ไป2O3 + H2SW4 -> อัล2(ดังนั้น4)3 + 3 ชม2O
อะลูมิเนียมซัลเฟตสามารถเกิดขึ้นได้โดยปฏิกิริยาการทำให้เป็นกลางระหว่างอลูมิเนียมไฮดรอกไซด์และกรดซัลฟิวริกตามปฏิกิริยาต่อไปนี้:
2 อัล (OH)3 + 3 ชม2SW4 + 12 ชม2O -> อัล2(ดังนั้น4)3.18h2O
กรดซัลฟูริกทำปฏิกิริยากับอลูมิเนียมเพื่อสร้างแอมโมเนียมซัลเฟตและปล่อยโมเลกุลไฮโดรเจนในรูปของแก๊ส ปฏิกิริยาที่ได้คือ schematized ดังนี้
2 Al + 3 H2SW4 -> อัล2(ดังนั้น4)3 + 3 ชม2
ชนิด
อลูมิเนียมซัลเฟตแบ่งออกเป็นสองประเภท: ประเภท A และประเภท B ในอลูมิเนียมซัลเฟตประเภท A, ของแข็งเป็นสีขาวและมีความเข้มข้นของเหล็กน้อยกว่า 0.5%.
ในอลูมิเนียมซัลเฟตประเภท B ของแข็งจะเป็นสีน้ำตาลและมีความเข้มข้นของธาตุเหล็กน้อยกว่า 1.5%.
มีอุตสาหกรรมที่ผลิตอลูมิเนียมซัลเฟตที่มีเกณฑ์แตกต่างกันสำหรับการจำแนกประเภทของพวกเขา ดังนั้นอุตสาหกรรมรายงานการเตรียมความพร้อมสำหรับประเภทของอลูมิเนียมซัลเฟตความเข้มข้นสูงสุดของเหล็ก 0.1% เป็นเฟอร์ริกออกไซด์ ในขณะที่สำหรับประเภท B พวกเขาระบุความเข้มข้นของธาตุเหล็กสูงสุด 0.35%.
ความเป็นพิษ
-อะลูมิเนียมซัลเฟตเป็นสารประกอบที่ออกฤทธิ์พิษโดยการสัมผัสกับฝุ่นของมันจึงก่อให้เกิดการระคายเคืองผิวหนังและในกรณีที่การสัมผัสเป็นประจำโรคผิวหนัง.
-ในสายตามันทำให้เกิดการระคายเคืองอย่างรุนแรงแม้จะทำให้เกิดการบาดเจ็บถาวร.
-การสูดดมทำให้เกิดการระคายเคืองของจมูกและลำคอซึ่งอาจทำให้เกิดอาการไอและมีผื่นขึ้น.
-ปริมาณของมันทำให้เกิดการระคายเคืองในกระเพาะอาหารคลื่นไส้และอาเจียน.
-มีพิษถึงแม้ว่าพวกเขาจะไม่โดยตรงเนื่องจากอลูมิเนียมซัลเฟตพวกเขาเป็นทางอ้อมเนื่องจากการใช้งาน นี่เป็นกรณีของพิษบางอย่างของอลูมิเนียมที่เกิดจากการใช้อะลูมิเนียมซัลเฟตในการทำให้บริสุทธิ์ของน้ำ.
-ผู้ป่วยที่ได้รับการล้างไตเรื้อรังโดยใช้เกลือที่เตรียมในน้ำบริสุทธิ์ผ่านการใช้อะลูมิเนียมซัลเฟตจะพบกับความผิดปกติทางสุขภาพที่รุนแรงมาก ในบรรดาความผิดปกติเหล่านี้เรามีโรคโลหิตจางภาวะสมองเสื่อมจากการล้างไตและการเพิ่มขึ้นของโรคกระดูก.
การอ้างอิง
- วิกิพีเดีย (2018) อะลูมิเนียมซัลเฟต นำมาจาก: en.wikipedia.org
- Aris อุตสาหกรรม โซลูชันอลูมิเนียมซัลเฟตประเภท A และ B. นำมาจาก: aris.com.pe
- Christopher Boyd (9 มิถุนายน 2014) การใช้ประโยชน์อุตสาหกรรมชั้นนำสำหรับอลูมิเนียมซัลเฟต นำมาจาก: chemservice.com
- PubChem (2018) อะลูมิเนียมซัลเฟต นำมาจาก: pubchem.ncbi.nlm.nih.gov
- เคมีภัณฑ์ Andesia (20 สิงหาคม 2009) แผ่นเซฟตี้ของซัลเฟตอลูมิเนียม [PDF] นำมาจาก: andesia.com
- หนังสือเคมี (2017) อะลูมิเนียมซัลเฟต นำมาจาก: chemicalbook.com


