โครงสร้างทางเคมีของโพรพิลีนคุณสมบัติและการใช้งาน
โพรพิลีน หรือโพรพีนที่อุณหภูมิห้องและที่ความดันบรรยากาศอยู่ในสถานะก๊าซและเช่นเดียวกับอัลคีนอื่นไม่มีสี มันมีกลิ่นคล้ายกับน้ำมัน แต่มีความเข้มข้นน้อยกว่า มันมีช่วงเวลาไดโพลตั้งแต่แม้ว่ามันจะขาดการเชื่อมโยงขั้วที่แข็งแกร่ง แต่โมเลกุลของมันก็ไม่สมมาตร.
นอกจากนี้โพรพิลีนยังเป็นโครงสร้างไอโซเมอร์ของ cyclopropane (มีสูตรทางเคมีเหมือนกัน C)3H6) มันเกิดขึ้นในธรรมชาติเป็นผลมาจากพืชและกระบวนการหมัก เทียมเกิดขึ้นในระหว่างการประมวลผลของเชื้อเพลิงฟอสซิลเช่นน้ำมันก๊าซธรรมชาติและคาร์บอนน้อย.

ในทำนองเดียวกันเอทิลีนและโพรพิลีนเป็นผลิตภัณฑ์ของการกลั่นปิโตรเลียมในกระบวนการแยกโมเลกุลไฮโดรคาร์บอนขนาดใหญ่เพื่อสร้างไฮโดรคาร์บอนขนาดเล็กในความต้องการสูง.
โพรพิลีนยังสามารถหาได้โดยใช้วิธีการต่าง ๆ :
- การทำปฏิกิริยาเอทิลีนและบิวทีนแบบย้อนกลับได้ซึ่งพันธะคู่ถูกทำลายและปรับรูปแบบใหม่เพื่อให้โพรพิลีน.
- ผ่านกระบวนการดีไฮโดรจิเนชัน (สูญเสียไฮโดรเจน) ของโพรเพน.
- เป็นส่วนหนึ่งของโปรแกรมสำหรับการผลิตโอเลฟินจากเมทานอล (MTO) โพรพิลีนถูกผลิตจากเมทานอล นี่คือตัวเร่งปฏิกิริยาซีโอไลต์ซึ่งส่งเสริมการคายน้ำและนำไปสู่การก่อตัวของเอทิลีนและโพรพิลีน.
3CH3OH (เมทานอล) => CH3CH = CH2 (โพรพิลีน) + 3H2O (น้ำ)
ดัชนี
- 1 โครงสร้างทางเคมี
- 2 คุณสมบัติ
- 2.1 น้ำหนักโมเลกุล
- 2.2 จุดเดือด
- 2.3 จุดหลอมเหลว
- 2.4 จุดวาบไฟ
- 2.5 ความสามารถในการละลาย
- 2.6 การละลายแสดงเป็นมวล
- 2.7 ความหนาแน่น
- 2.8 ความหนาแน่นไอ
- 2.9 ความดันไอ
- 2.10 การส่งสัญญาณอัตโนมัติ
- 2.11 ความหนืด
- 2.12 ความร้อนจากการเผาไหม้
- 2.13 ความร้อนกลายเป็นไอ
- 2.14 แรงตึงผิว
- 2.15 พอลิเมอไรเซชัน
- 2.16 จุดเยือกแข็ง
- 2.17 เกณฑ์กลิ่น
- 3 ใช้
- 3.1 โพรพิลีน
- 3.2 Acrylonitrile
- 3.3 โพรพิลีนออกไซด์
- 3.4 สำหรับการสังเคราะห์แอลกอฮอล์และการใช้งานอื่น ๆ
- 4 อ้างอิง
โครงสร้างทางเคมี
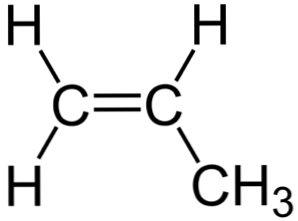
ในภาพด้านบนสามารถมองเห็นโครงสร้างทางเคมีของโพรพิลีนซึ่งมีความไม่สมดุล (ด้านขวาแตกต่างจากด้านซ้าย) โครงกระดูกของคาร์บอนซึ่งไม่รวมถึงอะตอม H สามารถสังเกตได้ว่าเป็นบูมเมอแรง.
บูมเมอแรงนี้นำเสนอความไม่แน่นอนหรือพันธะคู่ที่ด้านใดด้านหนึ่ง (C)1) และดังนั้นจึงค่อนข้างคงที่เนื่องจากการผสมพันธุ์ sp2 ของอะตอมคาร์บอน.
อย่างไรก็ตามอีกด้านหนึ่งถูกครอบครองโดยกลุ่มเมธิล (-CH3) ซึ่งมีการผสมข้ามพันธุ์คือ sp3 และมันก็มีรูปทรงเรขาคณิตแบบจัตุรมุข ดังนั้นเมื่อมองจากด้านหน้าบูมเมอแรงก็จะแบนราบกับอะตอม H ซึ่งยื่นออกมาจากที่109.5ºประมาณนี้.
ในช่วงก๊าซโมเลกุลมีปฏิสัมพันธ์กับผู้อื่นอย่างอ่อนโดยกองกำลังกระจาย นอกจากนี้ยังมีการป้องกันการมีปฏิสัมพันธ์ระหว่างพันธะคู่ (π-π) ของโมเลกุลโพรพิลีนสองตัวโดยกลุ่มเมธิล.
ซึ่งส่งผลในการลดลงของแรงระหว่างโมเลกุลของพวกเขาซึ่งสะท้อนให้เห็นในคุณสมบัติทางกายภาพของพวกเขา เฉพาะที่อุณหภูมิต่ำมากโพรพิลีนสามารถนำโครงสร้างที่เป็นของแข็งมาใช้ซึ่งกลุ่มบูมเมอร์ยังคงถูกจัดกลุ่มด้วยการปฏิสัมพันธ์ที่อ่อนแอ.
สรรพคุณ
มันเป็นก๊าซไม่มีสีมีกลิ่นหอม มันถูกขนส่งในรูปของก๊าซเหลวและเมื่อมันหนีออกมาจากภาชนะที่บรรจุมันจะทำในรูปของก๊าซหรือของเหลว ที่ความเข้มข้นต่ำจะเกิดเป็นส่วนผสมที่ระเบิดได้และติดไฟได้กับอากาศความหนาแน่นของโพรพิลีนจะสูงกว่าของอากาศ.
น้ำหนักโมเลกุล
42,081 กรัม / โมล
จุดเดือด
53.9 ºFถึง 760 mmHg
48 ºCถึง 760 mmHg
จุดหลอมเหลว
301.4 ºF
185 ºC
จุดวาบไฟ
162 ºF
สามารถในการละลาย
44.6 มล. / 100 มล. ในน้ำ.
1,250 มล. / 100 มล. ในเอทานอล.
524.5 มล. / 100 มล. ในกรดอะซิติก.
การละลายแสดงเป็นมวล
200 mg / l 25 ºC
ความหนาแน่น
0.609 mg / ml ที่-52.6º F
0.5139 ที่20º C
ความหนาแน่นของไอ
1.46 ถึง 32 ° F (สัมพันธ์กับอากาศถ่ายเป็นข้อมูลอ้างอิง).
1.49 (อากาศ = 1).
1.91 กิโลกรัม / เมตร3 ถึง 273.15 ºK
แรงดันไอน้ำ
1 mmHg ที่-205.4ºF
760 mmHg ถึง -53.9 ° F
8.69 × 103 mmHg ที่ 25 ºC (ค่าประมาณ).
1,158 kPa ที่ 25 ºC
15.4 atm ที่ 37 ºC
ติดไฟ
851 ºF
455 ºC
ความเหนียว
83.4 micropoise ที่ 16.7 ºC.
ความร้อนจากการเผาไหม้
16,692 BTU / ปอนด์
10.940 แคลอรี่ / กรัม
ความร้อนจากการระเหย
104.62 cal / g (ที่จุดเดือด)
แรงตึงผิว
16.7 dynes / cm ที่ 90 ° C
พอลิเมอ
พอลิเมอร์ที่อุณหภูมิสูงและความดันสูงเมื่อมีตัวเร่งปฏิกิริยา.
จุดเยือกแข็ง
185.25 ° C.
เกณฑ์กลิ่น
10-50 มก. / ม3 (ตรวจสอบ)
100 มก. / ม3 (การรับรู้)
การใช้งาน

มันถูกใช้ในอุตสาหกรรมปิโตรเคมีเป็นเชื้อเพลิงและตัวทำละลาย ในอุตสาหกรรมเคมีมันถูกใช้เป็นวัตถุดิบสำหรับการผลิตและการสังเคราะห์อนุพันธ์มากมาย.
มันมียูทิลิตี้ส่วนใหญ่ในการผลิตโพรพิลีน, acrylonitrile (ACN), โพรพิลีนออกไซด์ (PO), แอลกอฮอล์, cumene และกรดอะคริลิ.
โพรพิลีน
โพรพิลีนเป็นหนึ่งในวัสดุพลาสติกหลักที่ใช้ในอุปกรณ์อิเล็กทรอนิกส์และอุปกรณ์ไฟฟ้าของใช้ในครัวเรือนฝาขวดและกระเป๋าเดินทาง.
วัสดุลามิเนตใช้ในการบรรจุขนมหวานฉลากซีดี ฯลฯ ในขณะที่เส้นใยทำจากโฟลเดอร์และเสื้อผ้า.
Acrylonitrile
อีลาสโตเมอร์โพลีเมอร์และเส้นใยได้มาจากอะคริโลไนไตรล์ เส้นใยเหล่านี้มีไว้สำหรับการผลิตเสื้อผ้าในรูปแบบต่าง ๆ เช่นเสื้อกันหนาวถุงเท้าและเสื้อผ้ากีฬา พวกเขายังใช้ในเฟอร์นิเจอร์บ้านในโฟลเดอร์เบาะเบาะและผ้าห่ม.
โพรพิลีนออกไซด์
โพรพิลีนออกไซด์มีส่วนร่วมในการสังเคราะห์โพลียูรีเทน ใช้ในการผลิตโฟมยืดหยุ่นและโฟมแข็ง โฟมที่มีความยืดหยุ่นถูกนำมาใช้เป็นสารตัวเติมสำหรับเฟอร์นิเจอร์บ้านและในอุตสาหกรรมยานยนต์.
ในทางกลับกันโฟมแข็งส่วนใหญ่จะใช้เป็นวัสดุฉนวนอาคาร.
นอกจากนี้โพรพิลีนออกไซด์ยังใช้ในการผลิตโพรพิลีนไกลคอล สารประกอบนี้ใช้ในการผลิตโพลีเอสเตอร์เรซิ่นที่ไม่อิ่มตัวและเป็นสารป้องกันการแข็งตัว.
นอกจากนี้โพรพิลีนออกไซด์ยังใช้ในการผลิตโพรพิลีนไกลคอลอีเธอร์ อีเธอร์นี้มีการประยุกต์ใช้ในการผลิตสี, เสื้อผ้า, หมึก, เรซินและน้ำยาทำความสะอาด.
สำหรับการสังเคราะห์แอลกอฮอล์และการใช้งานอื่น ๆ
โพรพิลีนช่วยให้ได้รับแอลกอฮอล์ในหมู่พวกเขา isopropanol ใช้เป็นตัวทำละลายในเครื่องสำอางและผลิตภัณฑ์ดูแลส่วนบุคคล นอกจากนี้ยังตอบสนองการทำงานของตัวแทนน้ำยาฆ่าเชื้อ.
- ไอโซโพรพานอลมีส่วนร่วมในการผลิตสีเรซิ่นหมึกและเทปกาว มันยังใช้ในอุตสาหกรรมยา.
- Oxo-alcohol2-ethylhexanol ใช้ในการผลิต phthalates, plasticizers, วัสดุกาวและสี.
- บิวทานอลถูกนำมาใช้ในการผลิตสี, เคลือบ, เรซิ่น, สีย้อม, ยาและโพลีเมอ.
ในทางกลับกัน, Cumene ผลิตจากการรวมกันของโพรพิลีนและเบนซีน Cumene เป็นสารประกอบหลักในการผลิตฟีนอลและอะซิโตนที่ใช้ในผลิตภัณฑ์ต่าง ๆ เช่นโพลีคาร์บอเนตเรซินฟีนอลิกเรซินอีพอกซีและเมทิลเมทาคริเลต.
ในที่สุดกรดอะคริลิค - ผลิตภัณฑ์อื่นที่ได้มาจากโพรพิลีน - ถูกนำมาใช้ในการผลิตอะคริลิก.
การอ้างอิง
- Michal Osmenda (26 ธันวาคม 2550) จุดไฟของฉัน [รูป] สืบค้นเมื่อวันที่ 23 พฤษภาคม 2018 จาก: commons.wikimedia.org
- กลุ่มลินเด้ (2018) โพรพิลีน สืบค้นเมื่อวันที่ 23 พฤษภาคม 2018 จาก: linde-gas.com
- วิกิพีเดีย (2018) รพี สืบค้นเมื่อวันที่ 23 พฤษภาคม 2018 จาก: en.wikipedia.org
- PubChem (2018) โพรพิลีน สืบค้นเมื่อวันที่ 27 พฤษภาคม 2018 จาก: pubchem.ncbi.nlm.nih.gov
- Vesovic Velisa (7 กุมภาพันธ์ 2011) โพรพิลีน สืบค้นเมื่อวันที่ 27 พฤษภาคม 2018 จาก: thermopedia.com
- Jeffrey S. Plotkin (08 สิงหาคม 2016) โพรพิลีนไม่แน่ใจ สืบค้นเมื่อวันที่ 27 พฤษภาคม 2018 จาก: acs.org
- ICIS (6 พฤศจิกายน 2017) การใช้โพรพิลีนและข้อมูลการตลาด สืบค้นเมื่อวันที่ 27 พฤษภาคม 2018 จาก: icis.com


