สูตรแคลเซียมไฮดรอกไซด์คุณสมบัติปฏิกิริยาและการใช้งาน
แคลเซียมไฮดรอกไซด์, ยังเป็นที่รู้จักกันในนาม hydrated lime หรือ slaked lime เป็นสารประกอบอนินทรีย์ของสูตร Ca (OH)2.
แคลเซียมไฮดรอกไซด์มีโครงสร้างพอลิเมอร์เหมือนกับโลหะไฮดรอกไซด์ทุกชนิดเหมือนกับแมกนีเซียมไฮดรอกไซด์ (Mg (OH))2) ยังเป็นที่รู้จักกันในนาม brucita.
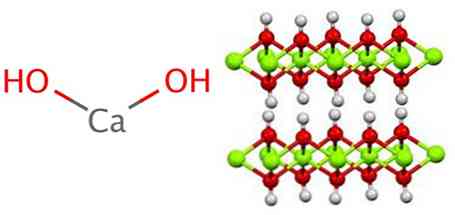
จะเห็นได้ว่าในโครงสร้างนี้มีการก่อตัวของสะพานไฮโดรเจน แคลเซียมไฮดรอกไซด์ถูกสังเคราะห์โดยการทำปฏิกิริยากับแคลเซียมออกไซด์หรือที่รู้จักในชื่อมะนาวหรือปูนขาวกับน้ำตามปฏิกิริยาต่อไปนี้:
CaOH + H2O → Ca (OH)2
มันยังเตรียมในห้องปฏิบัติการโดยปฏิกิริยาระหว่างแคลเซียมคลอไรด์ในน้ำและโซเดียมไฮดรอกไซด์.
แคลเซียมไฮดรอกไซด์เกิดขึ้นตามธรรมชาติ แต่ไม่ค่อยอยู่ในรูปของแร่ธาตุในรูปของพอร์ทไนท์ซึ่งพบได้ในหินภูเขาไฟและหินแปร (สูตรแคลเซียมไฮดรอกไซด์ - การใช้แคลเซียมไฮดรอกไซด์, คุณสมบัติ, โครงสร้างและสูตร, 2005-2017).
สารประกอบนี้ยังมีอยู่ทั่วไปในซีเมนต์น้ำยาและน้ำยาทำความสะอาดอุตสาหกรรม (เช่นผลิตภัณฑ์ก่อสร้าง) น้ำยาลอกพื้นน้ำยาล้างอิฐผลิตภัณฑ์ซีเมนต์หนาและอื่น ๆ อีกมากมาย.
สารละลายน้ำมักเรียกว่าน้ำปูนใส น้ำมะนาวเตรียมโดยการกวนแคลเซียมไฮดรอกไซด์ในน้ำบริสุทธิ์และกรองส่วนเกินของ Ca (OH)2 ไม่ละลาย.
เมื่อแคลเซียมไฮดรอกไซด์ส่วนเกินถูกเติมลงในน้ำมะนาวจะได้รับอนุภาคแขวนลอยของแคลเซียมไฮดรอกไซด์ทำให้มีลักษณะคล้ายน้ำนมซึ่งในกรณีนี้จะมีชื่อสามัญของน้ำนมมะนาว นมของมะนาวหรือสารละลายอิ่มตัวของมะนาว (น้ำมะนาว) มีค่า pH 12.3 เป็นของธรรมชาติพื้นฐาน.
สมบัติทางกายภาพและเคมีของแคลเซียมไฮดรอกไซด์
แคลเซียมไฮดรอกไซด์เป็นผงสีขาวหรือไม่มีสีไม่มีกลิ่น ในสารละลายน้ำ (สารละลายอิ่มตัว) มีลักษณะทางช้างเผือกเนื่องจากมีส่วนเกินของแคลเซียมไฮดรอกไซด์ที่ยังไม่ละลาย.
สารละลายที่ไม่อิ่มตัวมักจะใสและไม่มีสีมีกลิ่นของดินเล็กน้อยและมีรสอัลคาไลน์ที่ขมของแคลเซียมไฮดรอกไซด์ การปรากฏตัวของสารประกอบดังแสดงในรูปที่ 3 (ราชสมาคมเคมี, 2015).

แคลเซียมไฮดรอกไซด์มีน้ำหนักโมเลกุล 74.093 g / mol และความหนาแน่น 2.211 g / cm3 ในสถานะของแข็ง มันมีจุดหลอมเหลว 580 องศาเซนติเกรด ละลายได้ในน้ำไม่ดีสามารถละลายได้ 1.89 กรัมต่อลิตรที่ 0 ° C, 1.73 กรัมต่อลิตรที่ 20 ° C และ 0.66 กรัมต่อลิตรที่ 100 ° C.
มันละลายได้ในกลีเซอรีนและในสารละลายกรด มันไม่ละลายในแอลกอฮอล์ (ศูนย์ข้อมูลเทคโนโลยีชีวภาพแห่งชาติ, S.F. ).
แคลเซียมไฮดรอกไซด์ถูกละลายในน้ำบางส่วนเพื่อผลิตสารละลายที่เรียกว่าน้ำปูนซึ่งเป็นฐานที่พอเหมาะ น้ำมะนาวหรือ Ca (OH)2 (aq) มันทำปฏิกิริยากับกรดในรูปแบบเกลือและสามารถโจมตีโลหะบางชนิดเช่นอลูมิเนียม น้ำมะนาวทำปฏิกิริยากับคาร์บอนไดออกไซด์ได้ง่ายเพื่อสร้างแคลเซียมคาร์บอเนตซึ่งเป็นกระบวนการที่มีประโยชน์ที่เรียกว่าคาร์บอเนต:
Ca (OH)2 + CO2 → CaCO3 + H2O
Nitroparaffins, nitromethane, nitropropane เป็นต้นก่อให้เกิดเกลือที่มีฐานอนินทรีย์เช่นแคลเซียมไฮดรอกไซด์ เกลือที่แห้งเหล่านี้จะระเบิด สารประกอบนี้คล้ายกับโซเดียมไฮดรอกไซด์ (NaOH) หรือโซเดียมออกไซด์ (Na)2O) สิ่งเหล่านี้ทำให้กรดเป็นกลางทำให้เป็นเกลือและน้ำ.
การผสมวัสดุเหล่านี้กับน้ำสามารถสร้างความร้อนในปริมาณที่ไม่ปลอดภัยเนื่องจากฐานละลายหรือเจือจาง ฐานทำปฏิกิริยากับโลหะบางชนิด (เช่นอลูมิเนียมและสังกะสี) เพื่อสร้างออกไซด์ของโลหะหรือไฮดรอกไซด์และสร้างก๊าซไฮโดรเจน.
ฐานสามารถเริ่มปฏิกิริยาการเกิดพอลิเมอไรเซชันในสารประกอบอินทรีย์ที่สามารถปรับเปลี่ยนได้โดยเฉพาะอย่างยิ่งอิพอกไซด์ ก๊าซที่ติดไฟและ / หรือเป็นพิษสามารถเกิดขึ้นได้ด้วยเกลือแอมโมเนียมไนไตรด์ออร์แกนิคฮาโลเจน, โลหะต่างๆ, เปอร์ออกไซด์และไฮโดรเปอร์ออกไซด์ สารประกอบชนิดนี้มักทำหน้าที่เป็นตัวเร่งปฏิกิริยา (แผ่นข้อมูลทางเคมี CALCIUM HYDROXIDE, S.F. ).
ปฏิกิริยาและอันตราย

แคลเซียมไฮดรอกไซด์เป็นสารประกอบที่มีเสถียรภาพแม้ว่าจะเข้ากันไม่ได้กับกรดแก่ มันจัดว่าเป็นสารประกอบที่ก่อให้เกิดการระคายเคืองและท่ามกลางอันตรายที่เราสามารถเน้น:
มันกัดกรอนดวงตา (อาจทําใหกระจกตาเสียหายหรือตาบอด) และผิวหนัง (ทําใหเกิดการอักเสบและแผลพุพอง).
การสูดดมฝุ่นจะทำให้เกิดการระคายเคืองในทางเดินอาหารหรือทางเดินหายใจโดยมีอาการไหม้แสบและไอ การเปิดรับแสงมากเกินไปอย่างรุนแรงสามารถทำให้ปอดถูกทำลาย, ภาวะขาดอากาศหายใจ, หมดสติหรือเสียชีวิต การอักเสบของดวงตามีลักษณะเป็นสีแดง, ระคายเคืองและมีอาการคัน (เอกสารข้อมูลความปลอดภัยของวัสดุแคลเซียมไฮดรอกไซด์, 2013).
การสัมผัสถูกดวงตาซ้ำ ๆ กันในระดับต่ำของฝุ่นสามารถทำให้เกิดการระคายเคืองและการทำลายผิวหนังในท้องถิ่นหรือโรคผิวหนังบนผิวหนัง การสูดดมฝุ่นซ้ําสามารถทําให้เกิดการระคายเคืองต่อระบบทางเดินหายใจหรือปอดเสียหายได้.
หากสารเคมีนี้สัมผัสกับดวงตาพวกเขาควรล้างด้วยน้ำปริมาณมากทันทียกเปลือกตาล่างและเปลือกตาบนเป็นครั้งคราว ต้องพบแพทย์ทันที ไม่ควรใช้คอนแทคเลนส์เมื่อทำงานกับสารเคมีนี้.
หากสารเคมีนี้สัมผัสกับผิวหนังควรล้างผิวหนังที่ปนเปื้อนด้วยสบู่และน้ำทันที หากสารเคมีนี้แทรกซึมเสื้อผ้าให้ถอดเสื้อผ้าออกแล้วล้างผิวหนังด้วยน้ำทันที หากการระคายเคืองยังคงอยู่หลังจากล้างให้ไปพบแพทย์.
หากสูดดมสารเคมีจำนวนมากผู้สัมผัสถูกเคลื่อนย้ายไปยังที่ที่อากาศบริสุทธิ์ทันที หากการหายใจหยุดลงให้ทำการช่วยหายใจแบบปากต่อปากแล้วให้ผู้ป่วยได้รับความอบอุ่นและพักผ่อน ไปพบแพทย์โดยเร็วที่สุด.
หากกลืนกินให้ปรึกษาแพทย์ทันทีและถ้าเป็นไปได้ให้แสดงภาชนะบรรจุหรือฉลาก (แคลเซียมไฮดรอกไซด์เป็นพิษ 2017).
การจัดการและการเก็บรักษา
- สารประกอบควรเก็บไว้ในภาชนะแห้ง.
- อย่ากลืนหรือหายใจเอาฝุ่นเข้าไป.
- ไม่ควรเติมน้ำลงในผลิตภัณฑ์นี้.
- ในกรณีที่ไม่มีการระบายอากาศให้ใช้อุปกรณ์ช่วยหายใจที่เพียงพอ.
- หลีกเลี่ยงการสัมผัสกับผิวหนังและดวงตา.
- เก็บให้ห่างจากกรดที่เข้ากันไม่ได้.
- ปิดภาชนะบรรจุให้แน่น.
- เก็บภาชนะในที่เย็นและมีอากาศถ่ายเทสะดวก อย่าเก็บที่อุณหภูมิสูงกว่า 25 องศาเซลเซียส.
การใช้งานและการใช้งาน

แคลเซียมไฮดรอกไซด์ผลิตในปริมาณมากสามารถจัดการได้ง่ายและราคาถูกโดยทั่วไปดังนั้นจึงมีการใช้งานและการใช้งานที่โดดเด่นมากมาย.
การประยุกต์ใช้แคลเซียมไฮดรอกไซด์ที่สำคัญคือการตกตะกอนในน้ำและบำบัดน้ำเสีย มันเป็นของแข็งที่มีประจุปุยที่ช่วยในการกำจัดอนุภาคขนาดเล็กออกจากน้ำทำให้ผลิตภัณฑ์มีน้ำหนักเบาลง.
แอปพลิเคชั่นนี้เปิดใช้งานโดยต้นทุนต่ำและความเป็นพิษต่ำของแคลเซียมไฮดรอกไซด์ นอกจากนี้ยังใช้ในการบำบัดน้ำจืดเพื่อเพิ่มค่า pH ของน้ำ จุดประสงค์คือท่อจะไม่กัดกร่อนซึ่งน้ำในดินมีสภาพเป็นกรด.
การใช้งานที่ยอดเยี่ยมอีกอย่างหนึ่งคือในอุตสาหกรรมกระดาษซึ่งมันถูกใช้ในการผลิตโซเดียมไฮดรอกไซด์ การแปลงนี้เป็นองค์ประกอบของกระบวนการคราฟท์ที่รู้จักกันซึ่งใช้ในการสกัดเยื่อกระดาษ.
ในระบบช่วยชีวิตเช่นเครื่องดักจับก๊าซคาร์บอนไดออกไซด์โดยเฉพาะในเครื่องช่วยหายใจแบบปิดดำน้ำที่ลิเธียมไฮดรอกไซด์มีฤทธิ์กัดกร่อนมากขึ้นถือว่ามีความเสี่ยงเกินไป.
มันถูกใช้เป็นส่วนผสมในการฟอกและฉาบปูนด้วยปูนขาวที่เรียกว่า ในการก่อสร้างถนนแคลเซียมไฮดรอกไซด์จะช่วยปรับปรุงคุณภาพของดิน.
ตามที่สถาบันสุขภาพแห่งชาติ, แคลเซียมไฮดรอกไซเป็นที่นิยมใช้ในงานทันตกรรมเป็นยาต้านจุลชีพและเป็นสารของทางเลือกในการสร้างชั้นป้องกันที่เรียกว่าอุปสรรค apical.
Apical barrier มักใช้เป็นวิธีหนึ่งในการหลีกเลี่ยงการตายของเยื่อหุ้มปอดในสถานการณ์ที่การผ่าตัดเอ็นโดดอนต์ยากโดยเฉพาะอย่างยิ่ง.
เนื่องจากแคลเซียมไฮดรอกไซด์สามารถช่วยฆ่าเชื้อฟันที่มีการติดเชื้ออยู่แล้วจึงสามารถใช้เป็นการรักษาระยะสั้นเพื่อลดความเจ็บปวดและการอักเสบในการเตรียมการผ่าตัดเอ็นโดดอนต์ (Gottfried Schmalz, 2009).
มันทำหน้าที่เป็นสารเติมแต่งสำหรับน้ำทะเลเพราะจะช่วยลด CO2 ในชั้นบรรยากาศและบรรเทาผลกระทบเรือนกระจก.
ในการผลิตโลหะมะนาวจะถูกฉีดเข้าสู่กระแสของเสียเพื่อทำให้กรดเป็นกลางเช่นฟลูออไรด์และคลอไรด์ก่อนปล่อยสู่บรรยากาศ.
แคลเซียมไฮดรอกไซจะใช้เป็นส่วนผสมที่เป็นด่างในผลิตภัณฑ์ผ่อนคลายเส้นผมบางชนิด.
จากรายงานของศูนย์วิจัยวัสดุคอร์เนลพบว่าแคลเซียมไฮดรอกไซด์สามารถยืดผมหยิกได้เพราะมันจะทำลายพันธะซัลไฟด์ที่เชื่อมต่อซิสเทอีนซึ่งเป็นกรดอะมิโนที่มีความเข้มข้นสูงกว่าในเส้นผมหยิกธรรมชาติ การทำลายพันธะเหล่านี้และปิดผนึกด้วยแคลเซียมไฮดรอกไซด์จะเปลี่ยนแปลงโครงสร้างทางกายภาพของเส้นผมที่ได้รับการรักษาอย่างถาวร.
ในส่วนผสมของบอร์โดซ์แคลเซียมไฮดรอกไซด์จะทำหน้าที่แก้ปัญหาและสร้างยาฆ่าเชื้อราที่ติดทนนาน.
มันถูกใช้ในอุตสาหกรรมการกลั่นน้ำมันสำหรับการผลิตสารเติมแต่งน้ำมัน (ซาลิไซเลต, ซัลเฟต, ฟีนอล), ในอุตสาหกรรมปิโตรเคมีสำหรับการผลิตน้ำมันของแข็งของแบรนด์ต่าง ๆ และในอุตสาหกรรมเคมีสำหรับการผลิตแคลเซียมสเตียเรต . เป็นที่นิยมใช้ในการตรวจสอบก๊าซคาร์บอนไดออกไซด์และการดูดซับก๊าซ.
แคลเซียมไฮดรอกไซถูกนำมาใช้ในการผลิตผ้าเบรคในการจัดทำส่วนผสมแห้งสำหรับการทาสีและตกแต่งและในการผลิตสารผสมสำหรับยาฆ่าแมลง.
มันยังใช้เป็นอาหารเสริมแคลเซียมและบัฟเฟอร์ pH / คาร์บอเนตสำหรับการเพาะเลี้ยงสัตว์น้ำในตู้ปลาในแนวปะการัง.
มันเป็นยาฆ่าแมลงตามธรรมชาติ "ทางเลือก" ซึ่งส่วนใหญ่เป็นแมลงคลานตายโดยการสัมผัสกับมันรวมถึงเห็บหมัดหมัดด้วงและตัวอ่อน (Russiver, 2015).
แคลเซียมไฮดรอกไซด์เป็นสารละลายที่มีประสิทธิภาพสำหรับการแยกเส้นผมออกจากหนังสัตว์ในการเตรียมการผลิตหนัง.
ส่วนผสมของแคลเซียมไฮดรอกไซด์และน้ำอุ่นสร้างอ่างอาบน้ำซึ่งหนังที่สดควรจะแช่นานถึงสี่วันและเขย่าบ่อยๆ กระบวนการนี้จะทำให้เส้นผมและผิวหนังคลายตัวออกไปเท่าที่มันสามารถกำจัดได้ด้วยมือ.
เนื่องจากมีความเป็นพิษต่ำและความนุ่มนวลของคุณสมบัติพื้นฐานจึงทำให้มีการใช้มะนาวที่ได้รับการยอมรับอย่างแพร่หลายในอุตสาหกรรมอาหารเพื่อ:
- เพื่อชี้แจงน้ำดิบของอ้อยหรือหัวบีทน้ำตาลในอุตสาหกรรมน้ำตาล, ประมวลผลน้ำสำหรับเครื่องดื่มแอลกอฮอล์และน้ำอัดลม, ผักดองและอาหารอื่น ๆ.
- ทำให้ tortillas ข้าวโพด (ช่วย cornmeal มารวมกัน) ข้าวโพดที่ปรุงด้วยมะนาวจะถูกแปลงเป็นนิกตามาลซึ่งเพิ่มการดูดซึมของไนอาซินได้อย่างมีนัยสำคัญซึ่งถือว่ามีรสชาติดีขึ้นและย่อยง่ายขึ้น.
- ทำความสะอาดน้ำเกลือของแคลเซียมและแมกนีเซียมคาร์บอเนตในการผลิตเกลือสำหรับใช้ในอาหารและยา.
- เสริมเครื่องดื่มน้ำผลไม้เช่นน้ำส้มและสูตรสำหรับทารก (BAUM, 2013).
การอ้างอิง
- BAUM, J. (2013, 16 สิงหาคม) แคลเซียมไฮดรอกไซด์ใช้ สืบค้นจาก livestrong.com: livestrong.com.
- Calcium hydroxide Formula - แคลเซียมไฮดรอกไซด์ใช้คุณสมบัติโครงสร้างและสูตร (2005-2017) สืบค้นจาก softschools.com.
- พิษของแคลเซียมไฮดรอกไซด์ (2017, 7 กุมภาพันธ์) เรียกดูจาก medlineplus.gov.
- เอกสารข้อมูลทางเคมี CALCIUM HYDROXIDE ( S.F. ) สืบค้นจาก cameochemicals.noaa.gov.
- Gottfried Schmalz, D. A. (2009) ความเข้ากันได้ทางชีวภาพของวัสดุทางทันตกรรม เบอร์ลิน: สปริงเกอร์.
- เอกสารข้อมูลความปลอดภัยของวัสดุแคลเซียมไฮดรอกไซด์ (2013, 21 พฤษภาคม) สืบค้นจาก sciencelab: sciencelab.com.
- ศูนย์ข้อมูลเทคโนโลยีชีวภาพแห่งชาติ. ( S.F. ) PubChem ฐานข้อมูลแบบผสม; CID = 6093208 สืบค้นจาก pubchem.ncbi.nlm.nih.gov.
- ราชสมาคมเคมี (2015) แคลเซียมไฮดรอกไซด์ สืบค้นจาก ChemSpider: chemspider.com.
- Russiver, M. (2015, 17 สิงหาคม) แคลเซียมไฮดรอกไซด์ใช้ทำอะไร? สืบค้นจาก quora: quora.com.


