คุณสมบัติของโซเดียมไฮไดรด์ (NaH), ปฏิกิริยา, อันตรายและการใช้งาน
โซเดียมไฮไดรด์ เป็นสารประกอบอนินทรีย์ของสูตร NaH มันมีพันธะไอออนิกระหว่างโซเดียมและไฮไดรด์ โครงสร้างของมันแสดงในรูปที่ 1 มันเป็นตัวแทนของเกลือไฮไดรด์ซึ่งหมายความว่ามันเป็นไฮไดรด์ที่คล้ายกับเกลือประกอบด้วย Na + และ H- ions ตรงกันข้ามกับโมเลกุลไฮไดรด์เช่นโบรอนมีเทนแอมโมเนีย และน้ำ.
โครงสร้างผลึกมีการประสานงานหมายเลข 6 ซึ่งแต่ละโมเลกุลโซเดียมล้อมรอบด้วย 8 hydride ไอออนที่มีรูปร่างแปดด้านและมีภาพประกอบในรูปที่ 2 (Mark Winter [The University of Sheffield and WebElements Ltd, 1993-2016).
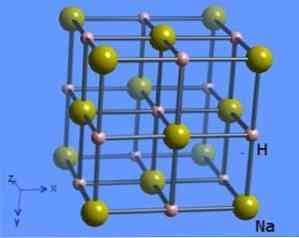
สารประกอบนี้จัดทำขึ้นโดยปฏิกิริยาโดยตรงระหว่างโซเดียมและก๊าซไฮโดรเจน (สูตรโซเดียมไฮไดรด์ - โซเดียมไฮไดรด์ใช้คุณสมบัติโครงสร้างและสูตร 2005-2017) ดังต่อไปนี้:
H2 + 2Na → 2NaH
โซเดียมไฮไดรด์ถูกขายในเชิงพาณิชย์ในรูปแบบการกระจาย 60% w / w (เปอร์เซ็นต์น้ำหนักต่อน้ำหนัก) ในน้ำมันแร่เพื่อการจัดการที่ปลอดภัย (SODIUM HYDRIDE, s.f. ).
ดัชนี
- 1 คุณสมบัติทางกายภาพและทางเคมีของโซเดียมไฮไดรด์
- 2 ปฏิกิริยาและอันตราย
- 3 ใช้
- 4 อ้างอิง
สมบัติทางกายภาพและทางเคมีของโซเดียมไฮไดรด์
โซเดียมไฮไดรด์เป็นของแข็งสีขาวเมื่อบริสุทธิ์แม้ว่าโดยทั่วไปจะได้เป็นสีเทาหรือสีเงิน มันปรากฏในรูปที่ 3.

NaH มีน้ำหนักโมเลกุล 23.99771 g / mol ความหนาแน่น 1.396 g / ml และจุดหลอมละลายที่ 800 ° C (ราชสมาคมเคมีปี 2558) มันไม่ละลายในแอมโมเนียเบนซีนคาร์บอนเตตระคลอไรด์และซัลไฟด์คาร์บอน (ศูนย์ข้อมูลเทคโนโลยีชีวภาพแห่งชาติ, s.f. ).
สารประกอบไม่เสถียรอย่างยิ่ง Pure NaH สามารถติดไฟในอากาศได้อย่างง่ายดาย เมื่อสัมผัสกับน้ำที่มีอยู่ในอากาศมันจะปล่อยไฮโดรเจนที่ติดไฟได้ง่ายออกมา.
เมื่อเปิดสู่อากาศและความชื้น NaH จะถูกไฮโดรไลซ์เข้าสู่ฐานการกัดกร่อนที่แข็งแกร่งของโซเดียมไฮดรอกไซด์ (NaOH) ตามปฏิกิริยา:
NaH + H2O → NaOH + H2
ในปฏิกิริยานี้จะสามารถสังเกตได้ว่าโซเดียมไฮไดรด์จะทำงานเหมือนฐาน นี้เกิดจากอิเล็กโตรเนกาติวีตี้.
โซเดียมมีอิเลคโตรเนกาติวีตี้ต่ำกว่าอย่างมีนัยสำคัญ (≈1.0) มากกว่าไฮโดรเจน (≈2.1) ซึ่งหมายความว่าไฮโดรเจนจะแยกความหนาแน่นของอิเล็กตรอนเข้าหาตัวเองเคลื่อนห่างจากโซเดียมเพื่อสร้างโซเดียมไอออนบวกและประจุลบ ของไฮไดรด์.
สำหรับสารประกอบที่เป็นกรดBrønstedนั้นจำเป็นต้องแยกความหนาแน่นของอิเล็กตรอนออกจากไฮโดรเจนนั่นคือเชื่อมต่อกับอะตอมของอิเล็กตรอนเช่นออกซิเจนฟลูออรีนไนโตรเจน ฯลฯ เท่านั้นจึงจะสามารถอธิบายอย่างเป็นทางการว่า H + และสามารถแยกออกจากกันได้.
ไฮไดรด์อธิบายได้ดีกว่าในฐานะ H- และมีอิเล็กตรอนอิสระหนึ่งคู่ เช่นนี้มันเป็นฐานBrønstedไม่ใช่กรด ในความเป็นจริงถ้าคุณขยายนิยามของBrønsted acid / base ในแบบที่ Lewis ทำคุณจะได้ข้อสรุปว่าโซเดียม (Na +) เป็นกรดชนิดที่นี่.
ผลิตภัณฑ์ปฏิกิริยากรด / เบสBrønstedของ H- เบสและกรด H + กลายเป็น H2 เนื่องจากไฮโดรเจนกรดถูกสกัดโดยตรงจากน้ำก๊าซไฮโดรเจนสามารถทำให้เกิดฟองได้โดยแทนที่สภาวะสมดุลแม้ว่าปฏิกิริยาจะไม่ได้รับความนิยมทางอุณหพลศาสตร์.
สามารถเหลือ OH- ไอออนที่สามารถเขียนด้วยส่วนที่เหลือของ Na + ไอออนบวกเพื่อให้โซเดียมไฮดรอกไซ (ทำไมโซเดียมไฮไดรด์ที่เป็นของแข็งและไม่เป็นกรดเมื่อทำปฏิกิริยากับน้ำ?, 2016).
ปฏิกิริยาและอันตราย
สารประกอบนี้เป็นสารลดแรงทรงพลัง โจมตี SiO2 ในแก้ว มันจุดชนวนเมื่อสัมผัสกับก๊าซ F2, Cl2, Br2 และ I2 (หลังที่อุณหภูมิสูงกว่า 100 ° C) โดยเฉพาะอย่างยิ่งในที่ที่มีความชื้นเพื่อสร้าง HF, HCl, HBr และ HI.
ทำปฏิกิริยากับกำมะถันเพื่อให้ Na2S และ H2S มันสามารถทำปฏิกิริยาระเบิดได้กับ dimethyl sulfoxide ทำปฏิกิริยาอย่างแรงกับอะเซทิลีนแม้ที่อุณหภูมิ -60 องศาเซลเซียสมันสามารถติดไฟได้เองในฟลูออรีน.
มันเริ่มต้นปฏิกิริยาพอลิเมอไรเซชันในเอทิล -2,2,3-trifluoropropionate ซึ่งเอสเตอร์สลายตัวอย่างรุนแรง การปรากฏตัวของปฏิกิริยาของ diethyl succinate และ ethyl trifluoroacetate ทำให้เกิดการระเบิด (SODIUM HYDRIDE, 2016).
โซเดียมไฮไดรด์ถือเป็นการกัดกร่อนต่อผิวหนังหรือดวงตาเนื่องจากศักยภาพของการเกิดปฏิกิริยากัดกร่อนกับน้ำ.
ในกรณีที่สัมผัสกับดวงตาพวกเขาควรล้างด้วยน้ำปริมาณมากภายใต้เปลือกตาเป็นเวลาอย่างน้อย 15 นาทีและไปพบแพทย์ทันที.
ในกรณีที่สัมผัสกับผิวหนังให้รีบแปรงและล้างบริเวณที่สัมผัสด้วยน้ำ ไปพบแพทย์หากยังมีอาการระคายเคือง.
มันเป็นอันตรายโดยการกลืนกินเนื่องจากปฏิกิริยากับน้ำ ห้ามทำให้อาเจียน คุณควรไปพบแพทย์ทันทีและนำเหยื่อไปยังศูนย์การแพทย์.
การกระจายตัวของโซเดียมไฮไดรด์ในน้ำมันไม่ใช่ฝุ่น อย่างไรก็ตามวัสดุที่ทำปฏิกิริยาสามารถปล่อยหมอกที่มีฤทธิ์กัดกร่อนได้ดี ในกรณีที่สูดดมให้ล้างปากด้วยน้ำแล้วส่งผู้ป่วยไปยังที่ที่มีอากาศบริสุทธิ์ ควรไปพบแพทย์ (Rhom and Hass Inc. , 2007).
การใช้งาน
การใช้หลักของโซเดียมไฮไดรด์คือการทำปฏิกิริยาควบแน่นและปฏิกิริยาอัลคิเลชั่นซึ่งพัฒนาผ่านการก่อตัวของคาร์บาเนียน (เร่งปฏิกิริยาโดยฐาน).
โซเดียมไฮไดรด์ในน้ำมันมีลักษณะคล้ายโซเดียมและโซเดียมโลหะแอลกอฮอเรตในความสามารถในการทำหน้าที่เป็นตัวแทน deprotonating ใน acetoacetic ester, Claisen, Stobbe, Dieckmann และปฏิกิริยาอื่น ๆ ที่เกี่ยวข้อง มันมีข้อได้เปรียบเหนือตัวแทนกลั่นตัวอื่น ๆ ในที่:
- มันเป็นฐานที่แข็งแกร่งกว่าซึ่งส่งผลให้เกิดการ deprotonation โดยตรง.
- ไม่ต้องการส่วนเกิน.
- H2 ที่ผลิตออกมานั้นจะทำการวัดขอบเขตของปฏิกิริยา.
- ปฏิกิริยารองเช่นการลดลงจะถูกกำจัด.
Alkylations ของเอมีนอะโรมาติกและเฮเทอโรไซคลิกเช่น 2-aminopyridine และ phenothiazine สามารถทำได้อย่างง่ายดายที่ผลผลิตสูงโดยใช้ส่วนผสมของโทลูอีน ความเข้มข้นของไดเมทิลฟอร์มไมด์เป็นตัวแปรที่ใช้ควบคุมอัตราการเกิดปฏิกิริยา (HINCKLEY, 1957).
การใช้โซเดียมไฮไดรด์สำหรับเก็บไฮโดรเจนเพื่อใช้ในยานพาหนะเซลล์เชื้อเพลิงได้รับการเสนอโดยไฮไดรด์จะถูกห่อหุ้มด้วยเม็ดพลาสติกที่ถูกบดในที่ที่มีน้ำเพื่อปลดปล่อยไฮโดรเจน.
การอ้างอิง
- HINCKLEY, M. D. (1957) การผลิตการจัดการและการใช้โซเดียมไฮไดรด์ ความก้าวหน้าในวิชาเคมีเล่ม 19, 106-117.
- Mark Winter [มหาวิทยาลัยเชฟฟิลด์และ WebElements Ltd, U. (1993-2016) โซเดียม: โซเดียมไฮไดรด์ สืบค้นจาก WebElements: webelements.com.
- ศูนย์ข้อมูลเทคโนโลยีชีวภาพแห่งชาติ. ( N.d. ) PubChem ฐานข้อมูลแบบผสม; CID = 24758 ดึงจาก PubChem: pubchem.ncbi.nlm.nih.gov.
- inc. Rhom และ Hass (2007, ธันวาคม) Sodium Hydride การกระจายตัว 60% ในน้ำมัน ดึงมาจาก dow.com.
- ราชสมาคมเคมี (2015) โซเดียมไฮไดรด์ สืบค้นจาก ChemSpider: chemspider.com.
- โซเดียมไฮไดรด์ (2016) สืบค้นจาก cameochemicals: cameochemicals.noaa.gov.
- สูตรโซเดียมไฮไดรด์ - โซเดียมไฮไดรด์ใช้คุณสมบัติโครงสร้างและสูตร (2005-2017) สืบค้นจาก Softschools.com: softschools.com.
- โซเดียมไฮไดรด์ ( N.d. ) สืบค้นจาก chemicalland21: chemicalland21.com.
- เหตุใดโซเดียมไฮไดรด์จึงเป็นของแข็งและไม่ใช่กรดเมื่อทำปฏิกิริยากับน้ำ (2016, 20 เมษายน) ดึงจาก stackexchange: เคมี.stackexchange.com.


