โครงสร้างโซเดียมคลอไรด์ (NaCl) คุณสมบัติการใช้งานความเป็นพิษ
โซเดียมคลอไรด์, เรียกอีกอย่างว่าเกลือหรือเกลือตั้งโต๊ะเป็นเกลืออนินทรีย์พื้นฐานของโซเดียมโลหะอัลคาไลและคลอรีนฮาโลเจน มันเป็นองค์ประกอบที่ใหญ่ที่สุดของเกลือที่กินได้และรูปแบบแร่ของมันเป็นที่รู้จักในฐานะฮาไลต์ สูตรโมเลกุลของมันคือ NaCl และอธิบายอัตราส่วนสโตอิชิโอเมตริกของไอออน (Na)+ Cl-) และไม่ใช่ของโมเลกุลที่ไม่ต่อเนื่อง (Na-Cl)
โซเดียมคลอไรด์เป็นของแข็งสีขาวผลึกที่เกิดขึ้นจากการรวมกันของโซเดียมโลหะสีขาวเงินซึ่งทำปฏิกิริยาอย่างรุนแรงกับน้ำและองค์ประกอบคลอรีนเป็นพิษก๊าซกัดกร่อนสีเขียวอ่อน.

ในภาพด้านบนจะมีส่วนของผลึก NaCl ปรากฏขึ้น เป็นไปได้อย่างไรที่ทั้งสององค์ประกอบมีความอันตรายเท่า Na และ Cl2, เกลือบริโภคได้จะเกิดขึ้นได้ไหม? ประการแรกสมการทางเคมีสำหรับการก่อตัวคือ:
2Na + s2(g) => 2NaCl (s)
คำตอบอยู่ในลักษณะของลิงก์ใน NaCl เป็นไอออนิกสมบัติของนา+ และ Cl- แตกต่างจากอะตอมที่เป็นกลาง.
โซเดียมเป็นองค์ประกอบสำคัญ แต่อยู่ในรูปแบบไอออนิก นา+ เป็นไอออนบวกของเซลล์นอกเซลล์ที่มีความเข้มข้นประมาณ 140 mEq / lt และรวมกับแอนไอออน- และ HCO3- (ไบคาร์บอเนต) ส่วนใหญ่มีหน้าที่รับผิดชอบต่อคุณค่าของออสโมลาริตี้และปริมาณนอกเซลล์.
นอกจากนี้แล้ว+ มีหน้าที่ในการสร้างและการนำกระแสแรงกระตุ้นเส้นประสาทในซอนประสาทเช่นเดียวกับการเริ่มต้นการหดตัวของกล้ามเนื้อ.
NaCl ถูกใช้มาตั้งแต่สมัยโบราณเพื่อปรุงแต่งอาหารและเพื่อรักษาเนื้อสัตว์เนื่องจากความสามารถในการกำจัดแบคทีเรียและป้องกันการเน่าเสีย.
นอกจากนี้ยังจำเป็นสำหรับการผลิตโซเดียมไฮดรอกไซด์ (NaOH) และคลอรีนโมเลกุล2) โดยทำปฏิกิริยากับน้ำภายใต้ไฮโดรไลซิส:
2H2O (l) + 2 NaCl (s) => 2NaOH (ac) + Cl2(g) + H2(G)
ในแคโทด (-) H จะสะสม2 (g) และ NaOH ในขณะเดียวกัน Cl จะสะสมที่ขั้วบวก (+)2 (G) โซเดียมไฮดรอกไซด์ถูกใช้ในการผลิตสบู่และคลอรีนในการผลิตพลาสติก PVC.
ดัชนี
- 1 โครงสร้างของโซเดียมคลอไรด์
- 1.1 Unitary Cell
- 2 คุณสมบัติ
- 2.1 สูตรโมเลกุล
- 2.2 น้ำหนักโมเลกุล
- 2.3 ลักษณะทางกายภาพ
- 2.4 สี
- 2.5 รสชาติ
- 2.6 จุดเดือด
- 2.7 จุดหลอมเหลว
- 2.8 การละลายในน้ำ
- 2.9 การละลายในตัวทำละลายอินทรีย์
- 2.10 ความหนาแน่น
- 2.11 ความดันไอ
- 2.12 ความเสถียร
- 2.13 การสลายตัว
- 2.14 ความหนืด
- 2.15 การกัดกร่อน
- 2.16 pH
- 3 ใช้
- 3.1 ในอาหาร
- 3.2 ใช้ในอุตสาหกรรม
- 3.3 ที่บ้าน
- 3.4 การใช้งานอื่น ๆ
- 3.5 การใช้การบำบัด
- 4 ความเป็นพิษ
- 4.1 การกลืนกิน
- 4.2 การระคายเคืองและการสัมผัสทางกายภาพ
- 5 อ้างอิง
โครงสร้างของโซเดียมคลอไรด์
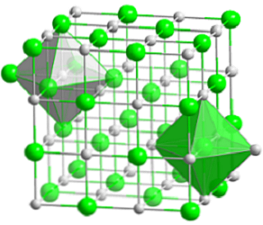
โครงสร้างลูกบาศก์ขนาดกะทัดรัดของโซเดียมคลอไรด์แสดงอยู่ในภาพด้านบน ทรงกลมสีเขียวขนาดใหญ่ตรงกับประจุลบของแอนไอออน-, ในขณะที่สีขาวเพื่อนาไพเพอร์+. สังเกตว่าคริสตัล NaCl ประกอบด้วยเครือข่ายของไอออนที่จัดโดยการเกิดไฟฟ้าสถิตในอัตราส่วน 1: 1.
แม้ว่าแท่งจะแสดงในภาพ แต่พันธะไม่ใช่โควาเลนต์ แต่เป็นอิออน การใช้แท่งมีประโยชน์เมื่อแสดงรูปทรงเรขาคณิตของการประสานงานรอบ ๆ ไอออน ตัวอย่างเช่นในกรณีของ NaCl แต่ละ Na+ ล้อมรอบด้วยหก Cl- (รูปแปดด้านสีขาว) และแต่ละ Cl- หกนา+ (รูปแปดด้านสีเขียว).
ดังนั้นจึงมีการประสานงาน (6,6) ซึ่งมีตัวเลขระบุจำนวนเพื่อนบ้านที่ล้อมรอบแต่ละไอออน หมายเลขด้านขวาหมายถึงเพื่อนบ้านของนา+, ขณะที่คนที่อยู่ทางซ้ายมือ Cl-.
การเป็นตัวแทนอื่น ๆ ละเว้นการใช้บาร์เพื่อเน้นหลุมแปดด้านที่มีโครงสร้างซึ่งเป็นผลมาจากพื้นที่คั่นระหว่างหกแอนไอออน- (หรือนาไพเพอร์+) แพ็คเกจ ข้อตกลงนี้มีการสังเกตในโมโนอื่น (MX) หรือเกลืออนินทรีย์ polyatomic และเรียกว่าเกลืออัญมณี.
เซลล์รวม
เซลล์หน่วยของเกลือสินเธาว์เป็นลูกบาศก์ แต่ลูกบาศก์ใดที่เป็นตัวแทนของมันในภาพด้านบน? รูปแปดด้านให้คำตอบ ทั้งสองครอบคลุมทั้งหมดสี่ก้อนเล็ก ๆ.
ก้อนเหล่านี้มีบางส่วนของไอออนในแนวตั้งขอบและใบหน้า สังเกตอย่างระมัดระวังไอออนไอออน+ มันตั้งอยู่ในใจกลางและสิบสองของพวกเขาในขอบ ไอออนบนขอบหนึ่งสามารถใช้สี่ลูกบาศก์ร่วมกันได้ มีไอออนอยู่ 4 ตัว+ (12 × 1/4 + 1 = 4).
สำหรับ Cl ไอออน-, แปดอยู่ในจุดยอดและหกในขอบ เมื่อไอออนที่อยู่ที่จุดยอดแบ่งปันพื้นที่กับแปดลูกบาศก์อื่น ๆ และที่ขอบที่มีหกพวกเขามี 4 Cl ไอออน- (8 × 1/8 + 6 × 1/2 = 4).
ผลลัพธ์ก่อนหน้านี้มีการตีความดังนี้: ในเซลล์หน่วยของ NaCl มีประจุบวกสี่ Na+ และแอนไอออนสี่ Cl-; สัดส่วนที่ตรงกับสูตรทางเคมี (นา+ สำหรับแต่ละ Cl-).
สรรพคุณ
สูตรโมเลกุล
โซเดียมคลอไรด์.
น้ำหนักโมเลกุล
58.44 กรัม / โมล.
คำอธิบายทางกายภาพ
ของแข็งผลึก.
สี
ผลึกไม่มีสีโปร่งใสหรือผงผลึกสีขาว.
รสชาติ
รสเค็ม.
จุดเดือด
2,575 ºFถึง 760 mmHg.
1,465 ºC.
จุดหลอมเหลว
1,474 ºF (800,7 ºC).
ทั้งจุดเดือดและจุดหลอมเหลวสะท้อนถึงความร้อนที่จำเป็นในการเอาชนะพลังงานไขว้กันเหมือนผลึก ดังนั้นการวัดเหล่านี้ยืนยันว่าตัวละครไอออนิกของ NaCl.
การละลายในน้ำ
มากกว่าหรือเท่ากับ 100 mg / ml ที่ 68 ° F.
36.0 g / 100 ml ที่ 25 ºC.
ในความเป็นจริงมันเป็นเกลือดูดความชื้นซึ่งเก็บความชื้นจากสภาพแวดล้อม.
การละลายในตัวทำละลายอินทรีย์
0.065 กรัม / 100 มิลลิลิตรของเอทานอลที่ 25 ° C; กลีเซอรีน 10 กรัม / 100 กรัมที่ 25 ° C; 2.15 กรัม / 100 มิลลิลิตรของแอมโมเนียมเหลวที่ 40 ° C; 1.4 g / 100 mL ของเมทานอลที่ 25 ° C; 7.15 g / 100 ของ ethylene glycol ที่ 25 ° C และ 5.21 g / 100 g ของกรด formic ที่ 25 ° C.
ความหนาแน่น
2,165 g / cm3 ที่ 77 ºC.
แรงดันไอน้ำ
1 mmHg ถึง 1,589 ºF.
ความมั่นคง
มีความเสถียรภายใต้สภาวะการเก็บรักษาที่แนะนำ.
การจำแนก
เมื่อถูกความร้อนจนถึงอุณหภูมิสูงมันจะสลายตัวไอระเหยของกรดไฮโดรคลอริกและไดออกไซด์ออกซิไดซ์.
ความเหนียว
ความหนืดของสารละลายอิ่มตัว 1.93 mPa-s.
การกร่อน
มันกัดกร่อนโลหะหลายชนิด.
พีเอช
6.7 ถึง 7.3 ในสารละลายที่เป็นน้ำ.
การใช้งาน
ในอาหาร
-โซเดียมคลอไรด์ถูกใช้มาตั้งแต่สมัยโบราณเพื่อปรับปรุงรสชาติของอาหารและการอนุรักษ์ การล้างเกลือของเนื้อสัตว์เป็นวิธีการป้องกันไม่ให้แบคทีเรียออกฤทธิ์เนื่องจากมันทำให้การสลายโปรตีนล่าช้า.
-ในทางกลับกันเกลือจะเพิ่มปริมาณออสโมลาริตีรอบเนื้อสัตว์ซึ่งทำให้เกิดการดูดซึมโดยการออสโมซิสของน้ำของแบคทีเรียทำให้เกิดการกำจัด.
ใช้ในอุตสาหกรรม
อุตสาหกรรมอาหาร
-ในอุตสาหกรรมอาหารนั้นเกลือถูกใช้เป็นสารปรุงแต่งกลิ่นรสสารเติมแต่งในการควบคุมการหมักสารควบคุมพื้นผิวและผู้พัฒนาสี ตัวอย่างเช่นเกลือถูกเพิ่มเพื่อเน้นสีในเบคอนแฮมและผลิตภัณฑ์จากเนื้อสัตว์อื่น ๆ.
-เกลือทำหน้าที่เป็นสารยึดเกาะในการผลิตไส้กรอก มันก่อให้เกิดการก่อตัวของเจลสารประสานที่ประกอบด้วยเนื้อสัตว์ไขมันและความชื้น.
-ในการแปรรูปแป้งเพื่อทำขนมปังจะมีการเติมเกลือในระหว่างการปรุงเพื่อควบคุมอัตราการหมักของแป้งขนมปัง นอกจากนี้ยังใช้ในการเสริมความแข็งแรงให้กับกลูเตนและใช้เป็นสารเพิ่มรสชาติ.
-มันถูกใช้ในการผลิตอาหารเช้าซีเรียลแป้งผสมหรือเตรียมมันฝรั่งทอดอาหารสำหรับสุนัขและแมว ฯลฯ.
การสังเคราะห์ผลิตภัณฑ์เคมี
-โซเดียมคลอไรด์ใช้เป็นวัตถุดิบในการผลิตโซเดียมไฮดรอกไซด์และคลอรีนซึ่งในทางกลับกันมีประโยชน์ในอุตสาหกรรมเคมีหลายแห่ง.
-เกลือถูกใช้ในกระบวนการแปรรูปโลหะชนิดต่าง ๆ เช่นอลูมิเนียมทองแดงเหล็กและวานาเดียม นอกจากนี้ยังใช้ในการทำโซเดียมคลอเรตซึ่งใช้ในการสังเคราะห์คลอรีนไดออกไซด์ซึ่งเป็นสารฟอกขาวที่ใช้ออกซิเจน คลอรีนไดออกไซด์เป็นอันตรายต่อสิ่งแวดล้อมน้อยกว่าสารฟอกขาวชนิดอื่น.
ในอุตสาหกรรมเครื่องหนัง
-เกลือใช้ในการยับยั้งการทำงานของแบคทีเรียภายในผิวหนังรวมถึงช่วยในการคืนความชุ่มชื้น.
ในอุตสาหกรรมสิ่งทอ
-เกลือถูกใช้เป็นสารกันบูดในการย้อมผ้า มันถูกใช้เป็นน้ำเกลือล้างออกเพื่อลบสารปนเปื้อนอินทรีย์และเพื่อสร้างประจุบวกบนพื้นผิวของผ้าที่ช่วยให้การรวมกลุ่มของสีย้อมที่มีประจุลบ.
ในอุตสาหกรรมน้ำมัน
-ในการสำรวจน้ำมันและก๊าซเกลือเป็นส่วนประกอบที่สำคัญของการขุดเจาะน้ำมัน ใช้ในการจับตัวและเพิ่มความหนาแน่นของของเหลวเจาะซึ่งช่วยให้เอาชนะแรงดันสูงของก๊าซในหลุมที่จะเข้าถึง นอกจากนี้เกลือยังคงความอิ่มตัวของของเหลวที่ขุดได้.
-เกลือช่วยในการกระชับดินที่ถนนถูกสร้างขึ้น ลดการเคลื่อนที่ที่เกิดจากดินใต้ผิวดินโดยการเปลี่ยนแปลงของความชื้นและปริมาณการใช้ยานยนต์.
ที่บ้าน
เกลือถูกใช้โดยการถูในการทำความสะอาดพื้นผิวหม้อและกระทะ นอกจากนี้ในการป้องกันเชื้อราและเป็นตัวกำจัดคราบ นอกจากนี้ยังใช้ในแชมพูและยาสีฟันหลายยี่ห้อ.
การใช้งานอื่น ๆ
บนถนน
-ในความคาดหมายของถนนหิมะปกคลุมไปด้วยน้ำเกลือซึ่งป้องกันไม่ให้สหภาพน้ำแข็งกับพื้นผิวของถนน สำหรับการละลายจะใช้ส่วนผสมของน้ำเกลือและเกลือและส่วนประกอบทางเคมีอื่น ๆ เช่นแมกนีเซียมหรือแคลเซียมคลอไรด์จะถูกเพิ่มเข้าไปในบางครั้ง การใช้เกลือและน้ำเกลือไม่มีประสิทธิภาพที่อุณหภูมิต่ำกว่า-10ºC.
เมื่อเพิ่มเกลือจะมีการลดลงของจุด cryoscopic ซึ่งเป็นคุณสมบัติการรวมตัวกันของการแก้ปัญหาซึ่งเป็นอุปสรรคต่อการก่อตัวของน้ำแข็ง.
-เนื่องจากสภาพของมันดูดความชื้นจึงใช้เกลือเป็นสารดูดความชื้นราคาถูก.
ในเรซินที่ใช้สำหรับทำน้ำให้อ่อน
น้ำกระด้างมีไอออนของแคลเซียมและแมกนีเซียมที่ขัดขวางการทำงานของสบู่และผลิตสารที่เป็นด่างในอุปกรณ์และท่อต่าง ๆ ในการทำให้น้ำอ่อนเรซินเรซินแลกเปลี่ยนไอออนจะใช้ เกลือถูกใช้ในการเตรียมและการงอกใหม่ของเรซิน.
เมื่อเครื่องดับเพลิง
โซเดียมคลอไรด์ถูกใช้ในเครื่องดับเพลิงเพื่อต่อสู้กับไฟซึ่งมีโลหะที่ติดไฟได้เช่นแมกนีเซียมโพแทสเซียมโซเดียมและอัลลอยด์ NK.
เกลือทำหน้าที่เป็นตัวระบายความร้อนและยังเป็นเครื่องบดที่ จำกัด การเข้าถึงของออกซิเจนที่จะยิง.
ในการใส่แว่นตา
ผลึกโซเดียมคลอไรด์ถูกนำมาใช้ในส่วนประกอบทางแสงเช่นหน้าต่างและปริซึมโดยเฉพาะอย่างยิ่งสำหรับแสงอินฟราเรด อย่างไรก็ตามเนื่องจากเกลือมีการดูดความชื้นสูงจึงเกิดน้ำค้างแข็งชนิดหนึ่งซึ่งครอบคลุมเลนส์ ด้วยเหตุผลนี้เลนส์โซเดียมคลอไรด์จึงถูกแทนที่ด้วยซิงค์ซีลีน (ZnSe).
การรักษาใช้
เพื่อเสริมการขาดเกลือในร่างกาย
-เมื่อมีการสูญเสียร่างกายของนา+, จะต้องถูกแทนที่เพื่อรักษา osmolarity extracellular การนำประสาทและการหดตัวของกล้ามเนื้อ.
-NaCl ใช้ในการรักษาและป้องกันการขาดโซเดียมและคลอรีนเนื่องจากเหงื่อออกมากเกินไปในช่วงที่มีอุณหภูมิสูง นอกจากนี้ยังใช้ในการขับปัสสาวะมากเกินไปหรือ จำกัด การบริโภคเกลือมากเกินไป.
-การให้ทางหลอดเลือดดำของสารละลาย NaCl 045% ถูกใช้ในการจัดการโรคเบาหวาน hyperosmolar มันตอบสนองฟังก์ชั่น rehydrating และทำหน้าที่ในการประเมินสถานะของการทำงานของไต.
-การฉีดสารละลาย hypertonic ที่มีความเข้มข้น NaCl มากกว่า 0.9% w / v,
-พวกเขาจะใช้เมื่อมีการลดลงอย่างรุนแรงของนา+, การฟื้นฟูไอออนที่จำเป็น ภาวะนี้อาจเป็นผลมาจากการรักษาด้วยอิเล็กโทรไลต์ฟรีหรือด้วยความเข้มข้นของนา+.
Hyponatremia อาจเกิดจากการดื่มน้ำมากเกินไปไม่ได้ควบคุมโดยการทำงานของไตไม่เพียงพอ.
ในการรักษาและการใช้งานที่ผิดปกติ
-โซลูชั่นการสูดดม NaCl จะใช้ในการเจือจางยาที่ใช้ในระหว่างกระบวนการพ่นยา นอกจากนี้ยังใช้สำหรับล้างหลอดลมและการชลประทาน สารละลายน้ำเกลือ 0.9% ใช้ในสเปรย์พ่นจมูก.
-สารละลาย NaCl 20% ใช้สำหรับการติดตั้งภายในช่องท้องผ่านช่องท้องทำให้เกิดการทำแท้งช้าในช่วงไตรมาสที่สองของการตั้งครรภ์.
-โซเดียมคลอไรด์สามารถใช้เป็นยาฆ่าเชื้อโรคในท้องถิ่น ด้วยความสามารถในการออสโมติกจึงสามารถขจัดไวรัสและแบคทีเรียออกจากร่างกายในสภาวะที่ไม่ถูกเผาไหม้ ดังนั้นจึงใช้เป็นยาฆ่าเชื้อโรคที่เจ็บปวดในการฆ่าเชื้อบาดแผล.
ความเป็นพิษ
การนำเข้าไปในร่างกาย
มันจะมีผลที่เป็นอันตรายต่อสุขภาพหากการบริโภคสูงและเป็นเวลานาน ภายใต้สถานการณ์เหล่านี้ภาวะไขมันในเลือดสูงจะเกิดขึ้นกับการเพิ่มขึ้นของปริมาณนอกเซลล์ที่จะนำไปสู่ความดันโลหิตสูง.
การระคายเคืองและการสัมผัสทางกายภาพ
มันมีพิษเฉพาะเมื่อสูดดมสูงมาก เมื่อสัมผัสกับผิวหนังในรูปแบบที่มากเกินไปอาจทำให้ผิวแห้ง ในที่สุดมันทำให้เกิดการระคายเคืองชั่วขณะเมื่อสัมผัสกับดวงตา.
การอ้างอิง
- ตัวสั่นและแอตกินส์ (2008) เคมีอนินทรีย์ (ฉบับที่สี่, หน้า 84, 90, 93, 263) Mc Graw Hill.
- Whitten, Davis, Peck & Stanley เคมี (8th ed.) CENGAGE Learning, หน้า 482-483.
- โซเดียมคลอไรด์ (2018) โซเดียมคลอไรด์: ประโยชน์, การใช้, สรรพคุณ, ความเสี่ยง นำมาจาก: clorurodesodio.org
- PubChem (2018) โซเดียมคลอไรด์ สืบค้นจาก: pubchem.ncbi.nlm.nih.gov
- วิกิพีเดีย (2018) โซเดียมคลอไรด์ นำมาจาก: en.wikipedia.org
- องค์ประกอบอเมริกัน (2018) โซเดียมคลอไรด์ นำมาจาก: americanelements.com


