โครงสร้างของ Hydrobromic acid (HBr) คุณสมบัติการก่อตัวการใช้งาน
กรด Hydrobromic เป็นสารประกอบอนินทรีย์ซึ่งเป็นผลมาจากสารละลายของก๊าซที่เรียกว่าไฮโดรเจนโบรไมด์ สูตรทางเคมีของมันคือ HBr และสามารถพิจารณาในรูปแบบที่แตกต่างกันเทียบเท่า: เป็นโมเลกุลไฮไดรด์หรือไฮโดรเจนเฮไลด์ในน้ำ นั่นคือไฮดราไซด์.
ในสมการทางเคมีควรเขียนเป็น HBr (ac) เพื่อระบุว่าเป็นกรด hydrobromic ไม่ใช่แก๊ส กรดนี้เป็นหนึ่งในกรดไฮโดรคลอริกที่เป็นที่รู้จักมากที่สุด คำอธิบายสำหรับสิ่งนี้อยู่ในลักษณะของพันธะโควาเลนต์.
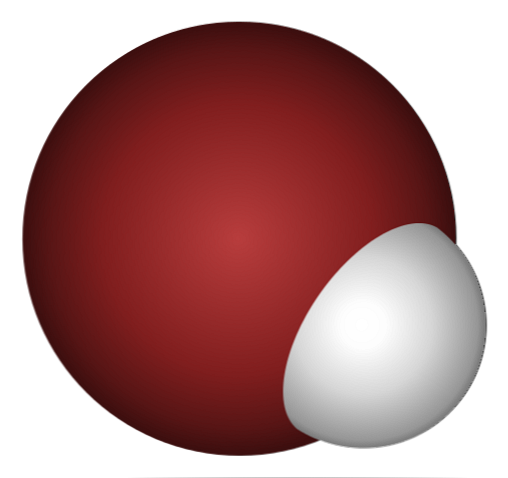
ทำไม HBr จึงเป็นกรดและยิ่งละลายในน้ำมากขึ้น? เนื่องจากพันธะโควาเลนต์ H-Br นั้นอ่อนแอมากเนื่องจากการทับซ้อนของวงโคจร 1s ของ H และ 4p ของ Br.
ไม่น่าแปลกใจถ้าคุณดูภาพด้านบนอย่างใกล้ชิดโดยที่ชัดเจนว่าโบรมีนอะตอม (สีน้ำตาล) มีขนาดใหญ่กว่าอะตอมไฮโดรเจน (สีขาว).
ดังนั้นการรบกวนใด ๆ ที่ทำให้เกิดการสลายของพันธะ H-Br ปล่อยไอออน H+. จากนั้นกรดไฮโดรโครมิกเป็นกรดBrönstedเนื่องจากมีการถ่ายโอนโปรตอนหรือไฮโดรเจนไอออน ความแข็งแรงของมันเป็นเช่นนั้นจะใช้ในการสังเคราะห์สารประกอบ organobrominated หลาย (เช่น 1-Bromo ethane, CH3CH2bR).
Hydrobromic acid คือหลังจาก hydric, HI หนึ่งในไฮโดรไซด์ที่แข็งแกร่งและมีประโยชน์มากที่สุดสำหรับการย่อยตัวอย่างของแข็งบางชนิด.
ดัชนี
- 1 โครงสร้างของกรด hydrobromic
- 1.1 ความเป็นกรด
- 2 คุณสมบัติทางกายภาพและทางเคมี
- 2.1 สูตรโมเลกุล
- 2.2 น้ำหนักโมเลกุล
- 2.3 ลักษณะทางกายภาพ
- 2.4 กลิ่น
- 2.5 เกณฑ์กลิ่น
- 2.6 ความหนาแน่น
- 2.7 จุดหลอมเหลว
- 2.8 จุดเดือด
- 2.9 การละลายในน้ำ
- 2.10 ความหนาแน่นไอ
- 2.11 pKa ความเป็นกรด
- 2.12 ความจุแคลอรี่
- 2.13 เอนทัลปีฟันกรามมาตรฐาน
- 2.14 เอนโทรปีของมาตรฐานกราม
- 2.15 จุดวาบไฟ
- 3 ศัพท์
- 4 มันเกิดขึ้นได้อย่างไร?
- 4.1 ส่วนผสมของไฮโดรเจนและโบรมีนในน้ำ
- 4.2 ฟอสฟอรัสทริโมโตไมด์
- 4.3 ซัลเฟอร์ไดออกไซด์และโบรมีน
- 5 ใช้
- 5.1 การเตรียมโบรไมด์
- 5.2 การสังเคราะห์อัลคิลเฮไลด์
- 5.3 ตัวเร่งปฏิกิริยา
- 6 อ้างอิง
โครงสร้างของกรด hydrobromic
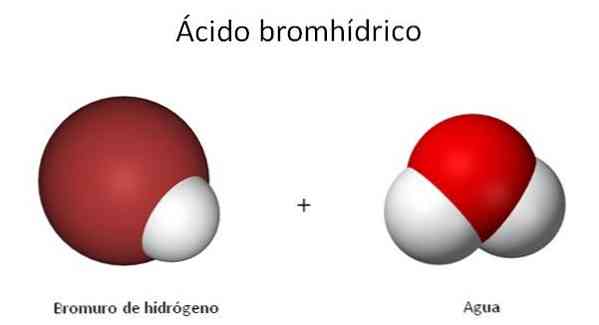
โครงสร้างของ H-Br แสดงอยู่ในภาพซึ่งมีคุณสมบัติและคุณสมบัติแม้กระทั่งของก๊าซมีความสัมพันธ์อย่างใกล้ชิดกับสารละลายน้ำ นั่นเป็นสาเหตุที่ทำให้เกิดความสับสนว่าสารประกอบใดในสองชนิดนี้ที่ถูกกล่าวถึง: HBr หรือ HBr (ac).
โครงสร้างของ HBr (ac) นั้นแตกต่างจาก HBr เพราะตอนนี้โมเลกุลของน้ำกำลังแก้โมเลกุลไดอะตอมมิกนี้ เมื่ออยู่ใกล้พอ H จะถูกถ่ายโอน+ ถึงโมเลกุลของ H2หรือตามที่ระบุในสมการทางเคมีต่อไปนี้:
HBr + H2O => Br-- + H3O+
ดังนั้นโครงสร้างของกรด hydrobromic ประกอบด้วย Br ions-- และเอช3O+ การโต้ตอบกับไฟฟ้าสถิต ตอนนี้มันแตกต่างจากพันธะโควาเลนต์ของ H-Br เล็กน้อย.
ความเป็นกรดที่ดีของมันเกิดจากประจุลบขนาดใหญ่- แทบจะไม่สามารถโต้ตอบกับ H3O+, ไม่สามารถป้องกันเขาจากการถ่ายโอน H+ ไปยังสารเคมีอื่นที่อยู่รอบ ๆ.
ความเปรี้ยว
ตัวอย่างเช่น Cl- และ F- แม้ว่าพวกเขาจะไม่ก่อพันธะโควาเลนต์กับ H3O+, พวกมันสามารถโต้ตอบผ่านแรงระหว่างโมเลกุลอื่น ๆ เช่นสะพานไฮโดรเจน (ซึ่งมีเพียงเอฟเท่านั้น)- สามารถยอมรับได้) สะพานไฮโดรเจน F--H-OH2+ "ขัดขวาง" การบริจาคของ H+.
ด้วยเหตุนี้เองกรดไฮโดรฟลูออริกจึงเป็นกรดอ่อนกว่า ในน้ำ กว่ากรดไฮโดรโบรมิก ตั้งแต่การโต้ตอบไอออนิกซ์ Br- H3O+ ไม่รบกวนการถ่ายโอนของ H+.
อย่างไรก็ตามถึงแม้ว่าน้ำจะมีอยู่ใน HBr (ac) พฤติกรรมของมันในตอนท้ายของบัญชีจะคล้ายกับโมเลกุลของ H-Br; นั่นคือ H+ มันถูกถ่ายโอนจาก HBr หรือ Br-H3O+.
คุณสมบัติทางกายภาพและทางเคมี
สูตรโมเลกุล
HBr.
น้ำหนักโมเลกุล
80,972 g / mol โปรดทราบว่าตามที่กล่าวไว้ในส่วนก่อนหน้านี้มีการพิจารณาเฉพาะ HBr ไม่ใช่โมเลกุลของน้ำ หากนำน้ำหนักโมเลกุลมาจากสูตร Br-H3O+ มันจะมีค่าประมาณ 99 g / mol โดยประมาณ.
ลักษณะทางกายภาพ
ของเหลวสีเหลืองหรือสีซีดซึ่งจะขึ้นอยู่กับความเข้มข้นของ HBr ที่ละลาย ยิ่งมีสีเหลืองมากเท่าไหร่ก็ยิ่งเข้มข้นและอันตรายมากเท่านั้น.
กลิ่น
ฉุนเฉียว.
เกณฑ์กลิ่น
6.67 mg / m3.
ความหนาแน่น
1.49 กรัม / ซม3 (สารละลายที่ 48% w / w) ค่านี้เช่นเดียวกับจุดหลอมเหลวและจุดเดือดขึ้นอยู่กับปริมาณของ HBr ที่ละลายในน้ำ.
จุดหลอมเหลว
-11ºC (12ºF, 393ºK) (สารละลายน้ำที่ 49% w / w).
จุดเดือด
122 ° C (252 ° F. 393 ° K) ที่ 700 mmHg (สารละลายน้ำ 47-49% w / w).
การละลายในน้ำ
-221 g / 100 ml (ที่ 0 ºC).
-204 กรัม / 100 มล. (15 ºC).
-130 g / 100 ml (100 ºC).
ค่าเหล่านี้หมายถึงก๊าซ HBr ไม่ใช่กรด hydrobromic ดังที่สามารถเห็นได้การเพิ่มอุณหภูมิจะลดการละลายของ HBr พฤติกรรมที่เป็นธรรมชาติในก๊าซ ดังนั้นหากจำเป็นต้องใช้สารละลายเข้มข้น HBr (ac) จะเป็นการดีกว่าถ้าใช้งานในอุณหภูมิต่ำ.
หากทำงานที่อุณหภูมิสูง HBr จะหนีออกมาในรูปของโมเลกุลไดอะตอมอะตอมดังนั้นก๊าซจะต้องปิดผนึกเครื่องปฏิกรณ์เพื่อป้องกันการรั่วไหล.
ความหนาแน่นของไอ
2.71 (สัมพันธ์กับอากาศ = 1).
ความเป็นกรด pKa
-9.0 ค่าคงที่เป็นลบอย่างนี้จึงบ่งบอกถึงความแข็งแกร่งของกรด.
ความจุแคลอรี่
29.1 kJ / mol.
เอนทัลปีกรามมาตรฐาน
198.7 kJ / mol (298 ºK).
เอนโทรปีของโมลาร์มาตรฐาน
-36.3 kJ / mol.
จุดติดไฟ
ไม่ติดไฟ.
ศัพท์เฉพาะ
ชื่อของมันคือ 'กรดไฮโดรโครมิก' ประกอบด้วยข้อเท็จจริงสองประการ: การปรากฏตัวของน้ำและโบรมีนนั้นมีความจุของ -1 ในสารประกอบ ในภาษาอังกฤษจะเห็นได้ชัดกว่า: กรดไฮโดรโบรมิกซึ่งคำนำหน้า 'ไฮโดร' (หรือไฮโดร) หมายถึงน้ำ แม้ว่าจริงๆแล้วมันสามารถอ้างถึงไฮโดรเจน.
โบรมีนมีความจุของ -1 เพราะมันถูกผูกไว้กับอะตอมไฮโดรเจนน้อยกว่า electronegative; แต่ถ้ามันมีการเชื่อมโยงหรือมีปฏิสัมพันธ์กับอะตอมออกซิเจนก็สามารถมีวาเลนซ์จำนวนมากเช่น: +2, +3, +5 และ +7 ด้วย H สามารถนำเวเลนซ์เดียวมาใช้และนั่นคือสาเหตุที่คำต่อท้าย -ico ถูกเพิ่มเข้ากับชื่อ.
ในขณะที่ HBr (g) ไฮโดรเจนโบรไมด์นั้นปราศจากน้ำ นั่นคือมันไม่มีน้ำ ดังนั้นจึงมีชื่ออยู่ภายใต้มาตรฐานระบบการตั้งชื่ออื่น ๆ ที่สอดคล้องกับไฮโดรเจนเฮไลด์.
มันเกิดขึ้นได้อย่างไร?
มีวิธีการสังเคราะห์หลายวิธีในการเตรียมกรดไฮโดรโครมิก บางส่วนของพวกเขาคือ:
ส่วนผสมของไฮโดรเจนและโบรมีนในน้ำ
กรดนี้สามารถรับได้จากส่วนผสมโดยตรงของไฮโดรเจนและโบรมีนในเครื่องปฏิกรณ์ที่เต็มไปด้วยน้ำโดยไม่ต้องอธิบายรายละเอียดทางเทคนิค.
H2 + br2 => HBr
ด้วยวิธีนี้เมื่อ HBr ก่อตัวมันจะละลายในน้ำ สิ่งนี้สามารถลากมันในการกลั่นดังนั้นวิธีการแก้ปัญหาสามารถสกัดด้วยความเข้มข้นที่แตกต่างกัน ไฮโดรเจนเป็นก๊าซและโบรมีนเป็นของเหลวสีแดงเข้ม.
ฟอสฟอรัสไทม์
ในกระบวนการที่ซับซ้อนยิ่งขึ้นทรายผสมฟอสฟอรัสแดงและโบรมีนจะถูกผสม กับดักน้ำจะถูกวางไว้ในห้องอาบน้ำแข็งเพื่อป้องกัน HBr จากการหลบหนีและการก่อตัวแทนที่จะเป็นกรดไฮโดรโครมิก ปฏิกิริยาคือ:
2P + 3Br2 => 2PBr3
PBR3 + 3H2O => 3HBr + H3PO3
ซัลเฟอร์ไดออกไซด์และโบรมีน
อีกวิธีในการเตรียมตัวคือทำปฏิกิริยาโบรมีนกับซัลเฟอร์ไดออกไซด์ในน้ำ:
br2 + SW2 + 2H2O => 2HBr + H2SW4
นี่คือปฏิกิริยารีดอกซ์ The Br2 มันลดลงจะได้รับอิเล็กตรอนโดยการเชื่อมโยงกับไฮโดรเจน ในขณะที่ SO2 มันออกซิไดซ์, มันสูญเสียอิเล็กตรอน, เมื่อมันเกิดพันธะโควาเลนต์มากขึ้นกับ oxygens อื่น ๆ , เช่นเดียวกับในกรดซัลฟูริก.
การใช้งาน
การเตรียมโบรไมด์
เกลือโบรไมด์สามารถเตรียมได้ถ้า HBr (ac) ทำปฏิกิริยากับไฮดรอกไซด์โลหะ ตัวอย่างเช่นการผลิตแคลเซียมโบรไมด์ถือว่าเป็น:
Ca (OH)2 + 2HBr => CaBr2 + H2O
อีกตัวอย่างหนึ่งคือโซเดียมโบรไมด์:
NaOH + HBr => NaBr + H2O
ดังนั้นสามารถเตรียมโบรไมด์อนินทรีย์ได้.
การสังเคราะห์อัลคิลเฮไลด์
แล้วโบรไมด์อินทรีย์ล่ะ เหล่านี้คือสารประกอบออร์กาโนโบรมิเนต: RBr หรือ ArBr.
การคายน้ำของแอลกอฮอล์
วัตถุดิบที่จะได้มานั้นสามารถเป็นแอลกอฮอล์ได้ เมื่อเกิดการรวมตัวกันของความเป็นกรดของ HBr พวกมันจะกลายเป็นน้ำซึ่งเป็นกลุ่มที่ส่งออกได้ดีและแทนที่อะตอมที่มีขนาดใหญ่ของ Br จะถูกรวมเข้าด้วยกัน
ROH + HBr => RBr + H2O
การคายน้ำจะดำเนินการที่อุณหภูมิสูงกว่า 100 ° C เพื่ออำนวยความสะดวกในการแตกของพันธะ R-OH2+.
นอกจากนี้เพื่อ alkenes และ alkynes
โมเลกุล HBr สามารถเพิ่มได้จากสารละลายที่เป็นพันธะสองหรือสามของอัลคีนหรือแอลคีน:
R2C = CR2 + HBr => RHC-CRBr
RC≡CR + HBr => RHC = CRBr
สามารถรับผลิตภัณฑ์หลายชนิดได้ แต่ภายใต้เงื่อนไขที่เรียบง่ายผลิตภัณฑ์จะถูกสร้างขึ้นเป็นครั้งแรกโดยที่โบรมีนเชื่อมโยงกับคาร์บอนทุติยภูมิหรือตติยภูมิสี่ขั้น.
เฮไลด์เหล่านี้เข้ามามีส่วนในการสังเคราะห์สารประกอบอินทรีย์อื่น ๆ และขอบเขตการใช้งานนั้นกว้างขวางมาก นอกจากนี้บางคนสามารถใช้ในการสังเคราะห์หรือออกแบบยาใหม่.
ไม่มีตัวตน
จากอีเทอร์สามารถได้อัลคิลเฮไลด์สองตัวพร้อมกันแต่ละอันถือโซ่ด้านใดด้านหนึ่ง R หรือ R 'ของอีเธอร์เริ่มต้น R-O-R' มันเกิดขึ้นคล้ายกับการขาดน้ำของแอลกอฮอล์ แต่กลไกการเกิดปฏิกิริยานั้นแตกต่างกัน.
ปฏิกิริยาสามารถเกิดขึ้นได้ด้วยสมการทางเคมีต่อไปนี้:
ROR '+ 2HBr => RBr + R'Br
และน้ำก็จะถูกปล่อยออกมา.
ตัวเร่ง
ความเป็นกรดของมันเป็นเช่นนั้นสามารถใช้เป็นตัวเร่งปฏิกิริยากรดที่มีประสิทธิภาพ แทนที่จะเพิ่ม Br anion- ไปที่โครงสร้างโมเลกุลเปิดทางให้โมเลกุลอื่น ๆ ทำ.
การอ้างอิง
- Graham Solomons T.W. , Craig B. Fryhle (2011) เคมีอินทรีย์ เอมีน (10TH ฉบับที่.) ไวลีย์พลัส.
- Carey F. (2008) เคมีอินทรีย์ (ฉบับที่หก) Mc Graw Hill.
- Steven A. Hardinger (2017) คำศัพท์ที่แสดงภาพประกอบของเคมีอินทรีย์: กรด Hydrobromic สืบค้นจาก: chem.ucla.edu
- วิกิพีเดีย (2018) กรด Hydrobromic สืบค้นจาก: en.wikipedia.org
- PubChem (2018) กรด Hydrobromic สืบค้นจาก: pubchem.ncbi.nlm.nih.gov
- สถาบันแห่งชาติเพื่อความปลอดภัยและสุขอนามัยในการทำงาน (2011) ไฮโดรเจนโบรไมด์ [PDF] ดึงจาก: insht.es
- PrepChem (2016) การเตรียมกรดไฮโดรโครมิก ดึงมาจาก: prepchem.com


