โครงสร้างเอทิลอะซิเตทคุณสมบัติการสังเคราะห์การใช้และความเสี่ยง
ethyl acetate หรือ ethyl ethanoate (ชื่อ IUPAC) เป็นสารประกอบอินทรีย์ที่มีสูตรทางเคมีคือ CH3COOC2H5. ประกอบด้วยเอสเตอร์ซึ่งส่วนประกอบของแอลกอฮอล์มาจากเอทานอลในขณะที่ส่วนประกอบของคาร์บอกซิลิกมาจากกรดอะซิติก.
มันเป็นของเหลวภายใต้สภาวะปกติของอุณหภูมิและความดันนำเสนอกลิ่นหอมของผลไม้ สถานที่ให้บริการนี้เข้ากันอย่างสมบูรณ์แบบกับสิ่งที่คาดหวังของเอสเตอร์; ซึ่งอันที่จริงแล้วลักษณะทางเคมีของเอทิลอะซิเตท ด้วยเหตุนี้จึงพบใช้ในผลิตภัณฑ์อาหารและเครื่องดื่มแอลกอฮอล์.
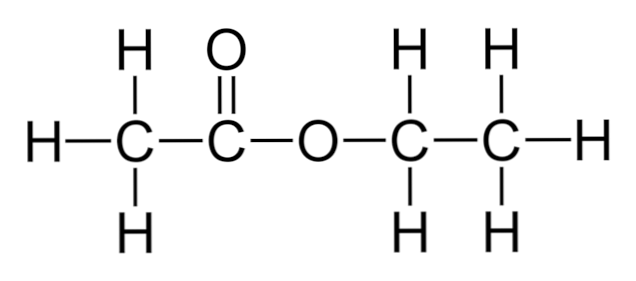
ในภาพด้านบนโครงกระดูกโครงสร้างของเอทิลอะซิเตตแสดงขึ้น หมายเหตุทางด้านซ้ายส่วนประกอบกรดคาร์บอกซิลิกและส่วนประกอบส่วนประกอบแอลกอฮอล์ทางด้านขวา จากมุมมองเชิงโครงสร้างคาดว่าสารนี้จะทำงานเหมือนลูกผสมระหว่างน้ำส้มสายชูกับแอลกอฮอล์ แม้กระนั้นมันแสดงคุณสมบัติของมันเอง.
นี่คือสิ่งที่ลูกผสมที่เรียกว่าเอสเทอร์แตกต่างกัน Ethyl acetate ไม่สามารถทำปฏิกิริยาเป็นกรดและไม่สามารถทำให้ขาดน้ำในกรณีที่ไม่มีกลุ่ม OH แต่จะผ่านการไฮโดรไลซิสพื้นฐานเมื่อมีฐานที่แข็งแกร่งเช่นโซเดียมไฮดรอกไซด์ NaOH.
ปฏิกิริยาไฮโดรไลซิสนี้ใช้ในการสอนในห้องปฏิบัติการสำหรับการทดลองเกี่ยวกับจลนพลศาสตร์เคมี โดยที่ปฏิกิริยานอกเหนือจากนั้นเป็นลำดับที่สอง เมื่อการไฮโดรไลซิสเกิดขึ้นจริงเอทิลเอทาโนอาเททจะกลับไปที่ส่วนประกอบเริ่มต้น: กรด (ถูกทำลายโดย NaOH) และแอลกอฮอล์.
ในโครงกระดูกของโครงสร้างพบว่าไฮโดรเจนอะตอมมีคุณสมบัติเหนือกว่าออกซิเจน สิ่งนี้มีอิทธิพลต่อความสามารถในการโต้ตอบกับสิ่งมีชีวิตที่ไม่ใช่ขั้วเช่นไขมัน นอกจากนี้ยังใช้ในการละลายสารประกอบเช่นเรซินสีย้อมและในของแข็งอินทรีย์ทั่วไป.
แม้จะมีกลิ่นหอมการสัมผัสกับของเหลวนี้เป็นเวลานานสร้างผลกระทบเชิงลบ (เช่นสารประกอบทางเคมีเกือบทั้งหมด) ในร่างกาย.
ดัชนี
- 1 โครงสร้างของเอทิลอะซิเตท
- 1.1 ขาดอะตอมของผู้บริจาคไฮโดรเจน
- 2 คุณสมบัติทางกายภาพและทางเคมี
- 2.1 ชื่อ
- 2.2 สูตรโมเลกุล
- 2.3 น้ำหนักโมเลกุล
- 2.4 ลักษณะทางกายภาพ
- 2.5 สี
- 2.6 กลิ่น
- 2.7 รสชาติ
- 2.8 เกณฑ์กลิ่น
- 2.9 จุดเดือด
- 2.10 จุดหลอมเหลว
- 2.11 การละลายในน้ำ
- 2.12 ความสามารถในการละลายในตัวทำละลายอินทรีย์
- 2.13 ความหนาแน่น
- 2.14 ความหนาแน่นไอ
- 2.15 ความเสถียร
- 2.16 ความดันไอ
- 2.17 ความหนืด
- 2.18 ความร้อนจากการเผาไหม้
- 2.19 ความร้อนกลายเป็นไอ
- 2.20 แรงตึงผิว
- 2.21 ดัชนีการหักเหของแสง
- 2.22 อุณหภูมิการจัดเก็บ
- 2.23 pKa
- 3 สรุป
- 3.1 ปฏิกิริยาของฟิชเชอร์
- 3.2 ปฏิกิริยาของ Tishchenko
- 3.3 วิธีการอื่น
- 4 ใช้
- 4.1 ตัวทำละลาย
- 4.2 รสชาติประดิษฐ์
- 4.3 การวิเคราะห์
- 4.4 การสังเคราะห์สารอินทรีย์
- 4.5 Chromatography
- 4.6 กีฏวิทยา
- 5 ความเสี่ยง
- 6 อ้างอิง
โครงสร้างของ ethyl acetate
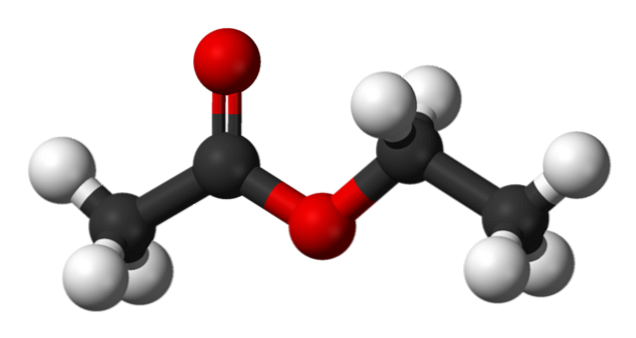
ในภาพด้านบนโครงสร้างของเอทิลอะซิเตตแสดงด้วยแบบจำลองของทรงกลมและแท่ง ในรูปแบบนี้อะตอมของออกซิเจนที่มีทรงกลมสีแดงจะถูกเน้น ทางด้านซ้ายของมันคือส่วนที่ได้จากกรดและทางด้านขวาของมันคือส่วนที่ได้จากแอลกอฮอล์ (กลุ่ม alkoxy, -OR).
กลุ่มคาร์บอนิลได้รับการชื่นชมจากพันธะ C = O (บาร์คู่) โครงสร้างรอบ ๆ กลุ่มนี้และออกซิเจนที่อยู่ติดกันนั้นแบนเนื่องจากมีการกระจายตัวของโหลดโดยเรโซแนนซ์ระหว่าง oxygens ทั้งสอง ความจริงที่อธิบายถึงความเป็นกรดที่ค่อนข้างต่ำของα-hydrogens (ของกลุ่ม -CH3, เชื่อมโยงกับ C = O).
โมเลกุลโดยการหมุนพันธะสองตัวนั้นจะช่วยโดยตรงกับการโต้ตอบกับโมเลกุลอื่น ๆ การปรากฏตัวของอะตอมออกซิเจนสองอะตอมและความไม่สมดุลของโครงสร้างทำให้เกิดช่วงเวลาไดโพลถาวร ซึ่งในทางกลับกันมีหน้าที่รับผิดชอบในการสื่อสารไดโพล - ไดโพล.
ยกตัวอย่างเช่นความหนาแน่นทางอิเล็กทรอนิกส์นั้นใกล้กับอะตอมออกซิเจนสองอะตอมซึ่งลดลงอย่างมากในกลุ่ม -CH3, และค่อย ๆ อยู่ในกลุ่ม OCH2CH3.
เนื่องจากปฏิกิริยาเหล่านี้โมเลกุลของเอทิลอะซิเตตจะกลายเป็นของเหลวภายใต้สภาวะปกติซึ่งมีจุดเดือดสูงมาก (77ºC).
ขาดอะตอมผู้บริจาคของพันธะไฮโดรเจน
หากคุณมองดูโครงสร้างอย่างใกล้ชิดคุณจะสังเกตเห็นว่าไม่มีอะตอมที่สามารถบริจาคสะพานไฮโดรเจนได้ อย่างไรก็ตามอะตอมของออกซิเจนเป็นตัวรับและเอทิลอะซิเตตละลายได้ในน้ำและมีปฏิกิริยากับสารประกอบขั้วและผู้บริจาคพันธะไฮโดรเจน (เช่นน้ำตาล).
นอกจากนี้ยังช่วยให้คุณสามารถโต้ตอบกับเอทานอลได้อย่างยอดเยี่ยม ซึ่งเป็นเหตุผลว่าทำไมการปรากฏตัวในเครื่องดื่มแอลกอฮอล์จึงไม่น่าแปลกใจ.
ในทางกลับกันกลุ่มอัลคาซี่ของมันทำให้สามารถโต้ตอบกับสารประกอบอะพอลล่าบางอย่างเช่นคลอโรฟอร์ม, CH3Cl.
คุณสมบัติทางกายภาพและทางเคมี
ชื่อ
-Ethyl acetate
-Ethylate ethanoate
-กรดอะซิติกเอสเตอร์
-Acetoxietano
สูตรโมเลกุล
C4H8O2 หรือ CH3COOC2H5
น้ำหนักโมเลกุล
88,106 กรัม / โมล.
คำอธิบายทางกายภาพ
ของเหลวใสไม่มีสี.
สี
ของเหลวไม่มีสี.
กลิ่น
ลักษณะของอีเทอร์คล้ายกับกลิ่นของสับปะรด.
รสชาติ
ก็ดีเมื่อเจือจางเพิ่มรสชาติผลไม้เบียร์.
เกณฑ์กลิ่น
3.9 ppm 0.0196 mg / m3 (กลิ่นต่ำ); 665 มก. / ม3 (กลิ่นสูง).
ตรวจพบกลิ่นที่ 7 - 50 ppm (เฉลี่ย = 8 ppm).
จุดเดือด
171 ° F ถึง 760 mmHg (77.1 ° C).
จุดหลอมเหลว
-118.5 ºF (-83.8 ºC).
การละลายในน้ำ
80 กรัม / ลิตร.
การละลายในตัวทำละลายอินทรีย์
สามารถผสมกับเอทานอลและเอทิลอีเทอร์ได้ ละลายได้ดีในอะซิโตนและเบนซีน สามารถผสมกับคลอโรฟอร์ม, น้ำมันคงที่และระเหยได้และยังมีตัวทำละลายออกซิเจนและคลอรีน.
ความหนาแน่น
0.9003 g / cm3.
ความหนาแน่นของไอ
3.04 (ในอัตราส่วนอากาศ: 1).
ความมั่นคง
มันสลายตัวช้าพร้อมกับความชื้น พลาสติกชนิดต่างๆและตัวออกซิไดซ์ที่แรง ส่วนผสมกับน้ำสามารถระเบิดได้.
แรงดันไอน้ำ
93.2 mmHg ที่ 25 ºC
ความเหนียว
0.423 mPoise ที่ 25 ºC.
ความร้อนจากการเผาไหม้
2,238.1 kJ / mol.
ความร้อนจากการระเหย
35.60 kJ / mol ที่ 25 ºC.
แรงตึงผิว
24 dynes / cm ที่ 20 ºC.
ดัชนีหักเห
1,373 ที่ 20 ºC / D.
อุณหภูมิการเก็บรักษา
2 - 8 ºC.
pKa
16 - 18 ที่ 25 ºC.
การสังเคราะห์
ปฏิกิริยาของฟิชเชอร์
เอทิลอะซิเตทถูกสังเคราะห์ทางอุตสาหกรรมโดยปฏิกิริยาฟิชเชอร์ซึ่งเอธานอลจะถูกทำให้เป็นกรดด้วยกรดอะซิติก ปฏิกิริยาจะเกิดขึ้นที่อุณหภูมิห้อง.
CH3CH2OH + CH3COOH <=> CH3ชส์2CH3 + H2O
ปฏิกิริยาจะถูกเร่งโดยการเร่งปฏิกิริยาของกรด สมดุลเคลื่อนไปทางขวานั่นคือไปสู่การผลิตเอทิลอะซิเตตผ่านการกำจัดน้ำ ตามกฎแห่งมวลชน.
ปฏิกิริยาของ Tishchenko
เอทิลอะซิเตทยังเตรียมทางอุตสาหกรรมโดยใช้ปฏิกิริยา Tishchenko, รวมกันสองสิ่งเทียบเท่าของอะซีตัลดีไฮด์กับการใช้อัลคอกไซด์เป็นตัวเร่งปฏิกิริยา.
2 CH3CHO => CH3ชส์2CH3
วิธีอื่น ๆ
-Ethyl acetate ถูกสังเคราะห์เป็น coproduct ในปฏิกิริยาออกซิเดชันของบิวเทนกับกรดอะซิติกในปฏิกิริยาที่เกิดขึ้นที่อุณหภูมิ 175 ° C และความดัน 50 atm ไอออนโคบอลต์และโครเมียมถูกใช้เป็นตัวเร่งปฏิกิริยา.
-เอทิลอะซิเตทเป็นตัวเชื่อมระหว่างเอทานอลของโพลีไวนิลอะซิเตตกับโพลีไวนิลแอลกอฮอล์.
-เอทิลอะซิเตตยังถูกผลิตขึ้นในอุตสาหกรรมด้วยการกำจัดสารเอธานอลออกซิเดชั่นปฏิกิริยาที่ถูกเร่งโดยการใช้ทองแดงที่อุณหภูมิสูง แต่ต่ำกว่า 250 องศาเซลเซียส.
การใช้งาน
ตัวทำละลาย
Ethyl acetate ใช้เป็นตัวทำละลายและเจือจางใช้ในการทำความสะอาดแผงวงจร มันถูกใช้เป็นตัวทำละลายในการผลิตสารสกัดฮ็อพดัดแปลงและในการกำจัดคาเฟอีนของใบชาและกาแฟ มันถูกใช้ในหมึกที่ใช้ทำเครื่องหมายผักและผลไม้.
Ethyl acetate ใช้ในอุตสาหกรรมสิ่งทอเป็นสารทำความสะอาด มันถูกใช้ในการสอบเทียบเครื่องวัดอุณหภูมิที่ใช้ในการแยกน้ำตาล ในอุตสาหกรรมสีจะใช้เป็นตัวทำละลายและเจือจางของวัสดุที่ใช้.
รสชาติประดิษฐ์
มันถูกใช้ในการทำอย่างละเอียดของรสชาติผลไม้; ตัวอย่างเช่น: กล้วยลูกแพร์พีชและสับปะรดรวมถึงกลิ่นหอมขององุ่นเป็นต้น.
การวิเคราะห์
มันถูกใช้ในการหาบิสมัทโบรอนทองคำโมลิบดีนัมและทองคำขาวรวมทั้งตัวทำละลายแทลเลียม Ethyl acetate มีความสามารถในการแยกสารประกอบและองค์ประกอบต่าง ๆ ที่มีอยู่ในสารละลายเช่นฟอสฟอรัสโคบอลต์ทังสเตนและสารหนู.
สารอินทรีย์สังเคราะห์
เอทิลอะซิเตทใช้ในอุตสาหกรรมเป็นตัวลดความหนืดสำหรับเรซิ่นที่ใช้ในสูตรโฟโต มันถูกใช้ในการผลิต acetamide, acetyl acetate และ methyl heptanone.
โค
ในห้องปฏิบัติการจะใช้เอทิลอะซิเตทเป็นเฟสเคลื่อนที่ของคอลัมน์โครมาโตกราฟฟีและเป็นตัวทำละลายสกัด โดยการให้เอทิลอะซิเตตมีจุดเดือดค่อนข้างต่ำทำให้ระเหยได้ง่ายซึ่งช่วยให้มีสมาธิกับสารที่ละลายในตัวทำละลาย.
กีฏวิทยา
เอทิลอะซิเตตใช้ในกีฏวิทยาในการกำจัดแมลงที่ขาดอากาศในภาชนะซึ่งทำให้สามารถรวบรวมและศึกษาได้ ไอระเหยของเอทิลอะซิเตทฆ่าแมลงโดยไม่ทำลายและป้องกันการชุบแข็ง.
ความเสี่ยง
-แอลดี50 ของ ethyl acetate ในหนูแสดงความเป็นพิษต่ำ อย่างไรก็ตามมันสามารถทำให้ระคายเคืองผิวหนังตาผิวหนังจมูกและลำคอ.
-การสัมผัสในระดับสูงอาจทำให้เกิดอาการวิงเวียนศีรษะและเป็นลม นอกจากนี้การได้รับสารเป็นเวลานานสามารถส่งผลกระทบต่อตับและไต.
-การสูดดมเอทิลอะซิเตตที่ความเข้มข้น 20,000 - 43,000 ppm สามารถทำให้เกิดอาการบวมน้ำที่ปอดและการตกเลือด.
-OSHA ได้กำหนดขีด จำกัด การเปิดรับแสงไว้ที่ 400 ppm ในอากาศโดยเฉลี่ยในระหว่างการทำงาน 8 ชั่วโมง.
การอ้างอิง
- Steven A. Hardinger (2017) คำศัพท์ที่แสดงภาพประกอบของเคมีอินทรีย์: เอทิลอะซิเตท (EtOAc) สืบค้นจาก: chem.ucla.edu
- Graham Solomons T.W. , Craig B. Fryhle (2011) เคมีอินทรีย์ เอมีน (10TH ฉบับที่.) ไวลีย์พลัส.
- Morrison, R. T. และ Boyd, R. N. (1990) เคมีอินทรีย์ (5ขอบคุณ Edition) กองบรรณาธิการ Addison-Wesley Iberoamericana.
- วิกิพีเดีย (2019) Ethyl acetate สืบค้นจาก: en.wikipedia.org
- ฝ้าย S. (s.f. ) Ethyl acetate ดึงจาก: chm.bris.ac.uk
- PubChem (2019) Ethyl acetate สืบค้นจาก: pubchem.ncbi.nlm.nih.gov
- นิวส์เคมี (2018) การใช้งานและการใช้งานของ ethyl acetate ดึงมาจาก: foodsweeteners.com
- มลรัฐนิวเจอร์ซีย์กรมอนามัยบริการอาวุโส (2002) Ethyl acetate [PDF] ดึงจาก: nj.gov


