คุณสมบัติลักษณะของสสาร (ทางกายภาพและเคมี)
คุณสมบัติลักษณะของสสาร เป็นคุณสมบัติทางเคมีหรือทางกายภาพที่สามารถช่วยระบุหรือแยกแยะสารหนึ่งจากอีกสารหนึ่ง คุณสมบัติทางกายภาพเป็นลักษณะของสารที่สังเกตได้ด้วยประสาทสัมผัส คุณสมบัติทางเคมีเป็นลักษณะที่อธิบายว่าสารเปลี่ยนจากสารหนึ่งไปเป็นอีกสารหนึ่งในระหว่างปฏิกิริยาทางเคมีอย่างไร.
คุณสมบัติทางกายภาพของสารบางอย่างคือความหนาแน่นความสามารถในการละลายจุดหลอมเหลวสีและมวล คุณสมบัติทางเคมีของวัสดุนั้นรวมถึงความสามารถในการติดไฟปฏิกิริยากับกรดและการกัดกร่อน ตัวอย่างของคุณสมบัติของสสารสามารถช่วยระบุองค์ประกอบคือการเปรียบเทียบความหนาแน่นขององค์ประกอบต่าง ๆ.
องค์ประกอบเช่นทองมีความหนาแน่น 19.3 กรัมต่อลูกบาศก์เซนติเมตรในขณะที่ความหนาแน่นของกำมะถัน 1.96 กรัมต่อลูกบาศก์เซนติเมตร ในทำนองเดียวกันจุดหลอมเหลวของสารเช่นน้ำและไอโซโพรพิลแอลกอฮอล์นั้นแตกต่างกัน.
คุณสมบัติทางกายภาพของสสาร
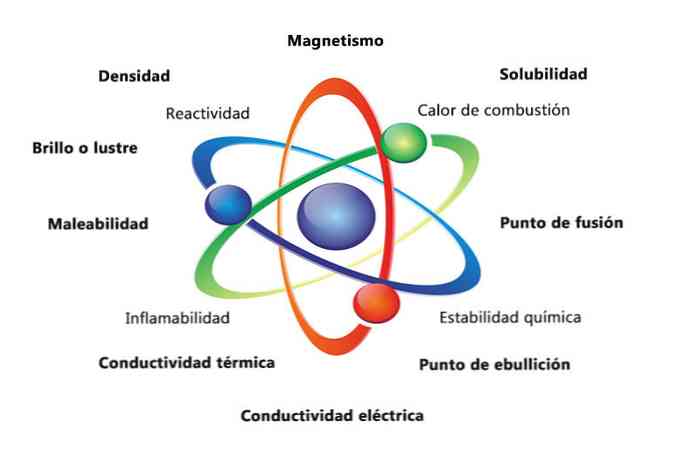
คุณสมบัติทางกายภาพของสสารนั้นเป็นคุณสมบัติที่สามารถวัดหรือสังเกตได้โดยไม่ต้องเปลี่ยนลักษณะทางเคมีของสาร ตัวอย่างคุณสมบัติทางกายภาพ ได้แก่ :
- ความหนาแน่น: จำนวนสสารที่มีวัตถุคำนวณโดยการหารมวลตามปริมาตร.
- Magnetism: แรงดึงดูดระหว่างแม่เหล็กกับวัตถุแม่เหล็ก.
- การละลาย: การวัดว่าสารสามารถละลายในสารอื่นได้ดีเพียงใด.
- จุดหลอมเหลว: อุณหภูมิที่สารเปลี่ยนจากของแข็งเป็นของเหลว.
- จุดเดือด: อุณหภูมิที่สารเปลี่ยนจากของเหลวเป็นแก๊ส.
- การนำไฟฟ้า: เป็นการวัดว่ากระแสไฟฟ้าเคลื่อนที่ผ่านสารได้ดีเพียงใด.
- การนำความร้อน: ความเร็วที่สารถ่ายโอนความร้อน.
- การอ่อนตัว: เป็นความสามารถของสารที่จะรีดหรือบดด้วยวิธีต่าง ๆ.
- เงาหรือเงา: เป็นวิธีที่วัตถุสะท้อนแสงได้อย่างง่ายดาย.
คุณสมบัติทางเคมีของสสาร
คุณสมบัติทางเคมีอธิบายถึงความสามารถของสารในการแปลงสภาพตัวเองเป็นสารใหม่ที่มีคุณสมบัติแตกต่างกัน ด้านล่างเป็นตัวอย่างคุณสมบัติทางเคมีหลายประการ:
- Heat of combustion: เป็นพลังงานที่ปล่อยออกมาเมื่อสารประกอบผ่านการเผาไหม้ที่สมบูรณ์ด้วยออกซิเจน.
- ความเสถียรทางเคมี: หมายถึงว่าสารประกอบจะทำปฏิกิริยากับน้ำหรืออากาศ (สารที่มีความเสถียรทางเคมีจะไม่ตอบสนอง).
- ความไวไฟ: ความสามารถของสารประกอบในการเผาไหม้เมื่อสัมผัสกับเปลวไฟ.
- การเกิดปฏิกิริยา: ความสามารถในการโต้ตอบกับสารอื่นและสร้างสารใหม่หนึ่งชนิดหรือมากกว่า.
สถานะทางกายภาพของสสาร
สสารคืออะไรก็ตามที่ใช้พื้นที่ซึ่งมีมวลและสามารถรับรู้ได้จากความรู้สึกของเรา สสารสามารถจำแนกตามสถานะทางกายภาพของมัน: ของแข็งของเหลวและก๊าซ.
1- ของแข็งและคุณสมบัติของพวกเขา
ของแข็งทั้งหมดมีมวลครอบครองพื้นที่มีปริมาตรและรูปร่างที่กำหนดอย่าลื่นไถลผ่านพื้นที่และไม่สามารถบีบอัดหรือมีรูปแบบที่แข็ง ตัวอย่างที่เรามี: ไม้หนังสือฟองน้ำโลหะหิน ฯลฯ.
ในของแข็งอนุภาคขนาดเล็กของสสารอยู่ใกล้กันมากและสัมผัสกัน อนุภาคอยู่ชิดกันจนไม่สามารถเคลื่อนที่ได้มากมีช่องว่างเล็ก ๆ น้อย ๆ ระหว่างพวกมัน.
2- ของเหลวและคุณสมบัติของพวกเขา
ของเหลวทั้งหมดมีมวลครอบครองพื้นที่มีปริมาตรที่กำหนด แต่ไม่ใช่รูปร่างที่กำหนด (เนื่องจากปรับให้เข้ากับภาชนะที่บรรจุ) จึงสามารถบีบอัดให้มีขนาดเล็กมากและสามารถเลื่อนผ่านช่องว่างได้ ตัวอย่างที่เรามี: น้ำน้ำมันก๊าดน้ำมัน ฯลฯ.
ในของเหลวอนุภาคเล็ก ๆ ของสสารจะอยู่ห่างจากกันและกันเล็กน้อยมีช่องว่างระหว่างพวกเขา (เทียบกับของแข็ง) และพวกเขาไม่ได้สัมผัสกัน ดังนั้นอนุภาคสามารถเคลื่อนที่ระหว่างช่องว่างผลักและชนกับอนุภาคอื่น ๆ เปลี่ยนทิศทางตลอดเวลา.
3- ก๊าซและคุณสมบัติของพวกเขา
ก๊าซทุกชนิดมีมวลครอบครองพื้นที่ไม่มีปริมาตรหรือรูปร่างที่กำหนดสามารถบีบอัดได้ในระดับที่ดีและสามารถกระจายสู่อวกาศได้ ตัวอย่างที่เรามี: ไฮโดรเจนออกซิเจนไนโตรเจนคาร์บอนไดออกไซด์ไอน้ำ ฯลฯ.
ในก๊าซอนุภาคเล็ก ๆ ของสสารแยกออกจากกันมีช่องว่างระหว่างพวกมันมากกว่าเมื่อเทียบกับของเหลวและพวกมันไม่ได้สัมผัสซึ่งกันและกัน อนุภาคมีอิสระในการเคลื่อนที่สูงสุดดังนั้นพวกมันจึงผลักและชนกับอนุภาคอื่น ๆ ที่มีการเปลี่ยนแปลงทิศทางตลอดเวลา.
การเปลี่ยนแปลงสถานะของสสาร
สสารสามารถเปลี่ยนจากสถานะของแข็งเป็นสถานะของเหลวและในทางกลับกันและจากสถานะของเหลวเป็นสถานะก๊าซและในทางกลับกัน การแปลงนี้ใช้ชื่อของการเปลี่ยนแปลงสถานะของสสารและเกิดขึ้นจากการเปลี่ยนแปลงของอุณหภูมิ:
การรวมกัน
การเปลี่ยนสถานะของวัสดุจากของแข็งเป็นของเหลวโดยการเพิ่มอุณหภูมิ เมื่อสารที่เป็นของแข็งถูกให้ความร้อนความร้อนจะทำให้อนุภาคสั่นสะเทือนอย่างแรงยิ่งขึ้น.
เมื่อถึงจุดหลอมเหลวอนุภาคของแข็งมีพลังงานจลน์เพียงพอที่จะเอาชนะกองกำลังแรงดึงดูดที่ดึงดูดพวกมันไว้ในตำแหน่งคงที่และพวกมันก็แตกเป็นกลุ่มของเหลวกลุ่มเล็ก ๆ.
การต้มหรือการระเหย
การเปลี่ยนสถานะของของเหลวให้เป็นก๊าซโดยการเพิ่มอุณหภูมิ เมื่อสารเหลวได้รับความร้อนความร้อนจะทำให้อนุภาคเคลื่อนที่เร็วขึ้น.
เมื่อถึงจุดเดือดอนุภาคของเหลวจะมีพลังงานจลน์เพียงพอที่จะเอาชนะแรงดึงดูดที่ดึงดูดพวกมันไว้ในตำแหน่งคงที่และแยกออกเป็นอนุภาคก๊าซแต่ละชนิด.
การแช่แข็งหรือแข็งตัว
การเปลี่ยนสถานะของของเหลวให้เป็นของแข็งโดยการลดอุณหภูมิ เมื่อสารของเหลวเย็นตัวอนุภาคของมันจะสูญเสียพลังงานจลน์จำนวนมาก เมื่อถึงจุดเยือกแข็งอนุภาคจะหยุดเคลื่อนที่และสั่นสะเทือนในตำแหน่งที่แน่นอนกลายเป็นอนุภาคของแข็ง.
เหลวหรือการควบแน่น
การเปลี่ยนสถานะของสสารแก๊สเป็นของเหลวโดยการลดอุณหภูมิ เมื่อสารที่เป็นแก๊สเย็นลงอนุภาคของมันจะสูญเสียพลังงานจลน์จำนวนมากซึ่งทำให้พวกมันดึงดูดซึ่งกันและกันกลายเป็นอนุภาคของเหลว.
การระเหิด
วัสดุบางอย่างเปลี่ยนโดยตรงจากสถานะของแข็งของพวกเขาเพื่อสถานะก๊าซหรือในทางกลับกันโดยไม่ต้องผ่านสถานะของเหลว เมื่อสารของแข็งเหล่านี้ถูกทำให้ร้อนอนุภาคของมันจะเคลื่อนที่อย่างรวดเร็วจนแยกไอน้ำหรือก๊าซที่ก่อตัวขึ้นอย่างสมบูรณ์และในทางกลับกันเมื่อกระบวนการเกิดขึ้นจากก๊าซกับของแข็ง.
การอ้างอิง
- De Podesta, M. การทำความเข้าใจคุณสมบัติของสสาร, รุ่นที่ 2 บริเตนใหญ่: เทย์เลอร์ & ฟรานซิส.
- Goel A. รัฐของสสาร นิวเดลี: Discovery Publishing House.
- Moore J, Stanitski C. วิทยาศาสตร์ระดับโมเลกุล, รุ่นที่ 5 Stamford: การเรียนรู้ Cengage.
- Ramakrishna A. ธรรมชาติของสสารฉบับที่ 1 นิวเดลี: Goyal Brothers Prakashan.
- Reger D, Goode S, Ball D. Chemistry หลักการและการปฏิบัติรุ่นที่ 3 แคนาดา: Brooks / Cole, Cengage Learning.
- Shapere D. Matter (ฟิสิกส์) ดึงมาจาก: accessscience.com.
- Singh L, Kaur M. Matter ในสภาพแวดล้อมของเรา อินเดีย: โรงเรียนส. จัน.


