สมบัติโพแทสเซียมไอโอเดตโครงสร้างการใช้ประโยชน์และความเสี่ยง
โพแทสเซียมไอโอเดต หรือโพแทสเซียมไอโอเดตเป็นสารประกอบอนินทรีย์ของไอโอดีนโดยเฉพาะเกลือซึ่งมีสูตรทางเคมีคือ KIO3. ไอโอดีนซึ่งเป็นองค์ประกอบของกลุ่มฮาโลเจน (F, Cl, Br, I, As) มีหมายเลขออกซิเดชันในเกลือนี้เป็น +5; ด้วยเหตุนี้จึงเป็นสารออกซิไดซ์ที่แรง KIO3 แยกออกจากกันในน้ำเพื่อสร้างไอออน K+ และ IO3-.
มันถูกสังเคราะห์โดยทำปฏิกิริยาโพแทสเซียมไฮดรอกไซด์กับกรดไอโอดีน: HIO3(aq) + KOH (s) => KIO3(aq) + H2O (l) นอกจากนี้ยังสามารถสังเคราะห์ได้โดยทำปฏิกิริยาโมเลกุลไอโอดีนกับโพแทสเซียมไฮดรอกไซด์: 3I2(s) + 6KOH (s) => KIO3(aq) + 5KI (aq) + 3H2O (l).

ดัชนี
- 1 คุณสมบัติทางกายภาพและทางเคมี
- 1.1 ตัวแทนออกซิไดซ์
- 2 โครงสร้างทางเคมี
- 3 การใช้และการใช้โพแทสเซียมไอโอเดต
- 3.1 การใช้การรักษา
- 3.2 ใช้ในอุตสาหกรรม
- 3.3 การใช้การวิเคราะห์
- 3.4 ใช้ในเทคโนโลยีเลเซอร์
- 4 ความเสี่ยงต่อสุขภาพของโพแทสเซียมไอโอเดต
- 5 อ้างอิง
คุณสมบัติทางกายภาพและทางเคมี
มันเป็นของแข็งสีขาวไม่มีกลิ่นมีผลึกดีและโครงสร้างผลึกของชนิด monoclinic มีความหนาแน่น 3.98 g / mL น้ำหนักโมเลกุล 214 g / mol และมีแถบดูดซับในสเปกตรัมอินฟราเรด (IR).
มันมีจุดหลอมเหลว: 833 ºK (560 ºC) สอดคล้องกับการปฏิสัมพันธ์ระหว่างไอออนไอออนที่แข็งแกร่งระหว่างไอออน K+ และ IO3-. ที่อุณหภูมิสูงกว่าจะเกิดปฏิกิริยาการสลายตัวของความร้อนปล่อยโมเลกุลออกซิเจนและโพแทสเซียมไอโอไดด์:
2KIO3(s) => 2KI (s) + 3O2(G)
ในน้ำมีความสามารถในการละลายที่แตกต่างกันจาก 4.74g / 100mL เป็น0ºCสูงถึง 32.3 g / 100mL ที่100ºCทำให้เกิดสารละลายที่ไม่มีสี นอกจากนี้ยังไม่ละลายในแอลกอฮอล์และกรดไนตริก แต่ละลายได้ในกรดซัลฟิวริกเจือจาง.
ความเป็นมิตรต่อน้ำของมันไม่สามารถประเมินได้ซึ่งอธิบายว่าทำไมมันจึงไม่ดูดความชื้นและไม่มีอยู่ในรูปของเกลือไฮเดรต (KIO)3·ชั่วโมง2O).
ตัวแทนออกซิไดซ์
โพแทสเซียมไอโอเดตตามสูตรทางเคมีของมันมีสามอะตอมออกซิเจน นี่เป็นองค์ประกอบที่มีอิเลคโตรเนกาติตี้อย่างแรงและเนื่องจากคุณสมบัตินี้มัน "ปล่อง" การขาดทางอิเล็กทรอนิกส์ในเมฆที่ล้อมรอบไอโอดีน.
การขาดนี้ - หรือการบริจาคตามที่กรณีสามารถคำนวณได้เป็นเลขออกซิเดชันของไอโอดีน (± 1, +2, +3, +5, +7), เป็น +5 สำหรับกรณีของเกลือนี้.
สิ่งนี้หมายความว่าอย่างไร ก่อนที่สปีชีส์ใดที่สามารถให้อิเล็กตรอนได้ไอโอดีนจะยอมรับพวกมันในรูปแบบไอออนิก (IO)3-) เป็นโมเลกุลไอโอดีนและมีเลขออกซิเดชันเท่ากับ 0.
จากคำอธิบายนี้สามารถสรุปได้ว่าโพแทสเซียมไอโอเดตเป็นสารประกอบออกซิไดซ์ที่ทำปฏิกิริยาอย่างรุนแรงกับตัวรีดิวซ์ในปฏิกิริยารีดอกซ์หลาย ๆ สิ่งเหล่านี้เป็นที่รู้จักกันในชื่อนาฬิกาไอโอดีน.
นาฬิกาไอโอดีนประกอบด้วยกระบวนการรีดอกซ์ของขั้นตอนช้าและเร็วซึ่งขั้นตอนอย่างรวดเร็วถูกทำเครื่องหมายด้วยโซลูชัน KIO3 ในกรดซัลฟิวริกที่เติมแป้ง ถัดไปแป้ง - ผลิตครั้งเดียวและยึดระหว่างชนิดโครงสร้างของมัน I3-- จะเปลี่ยนวิธีแก้ปัญหาจากไม่มีสีถึงสีน้ำเงินเข้ม.
IO3- + 3 HSO3- →ฉัน- + 3 HSO4-
IO3- + 5 ฉัน- + 6 ชม+ → 32 + 3 ชม2O
ผม2 + HSO3- + H2O → 2 ฉัน- + HSO4- + 2 ชั่วโมง+ (สีน้ำเงินเข้มเนื่องจากเอฟเฟกต์ของแป้ง)
โครงสร้างทางเคมี
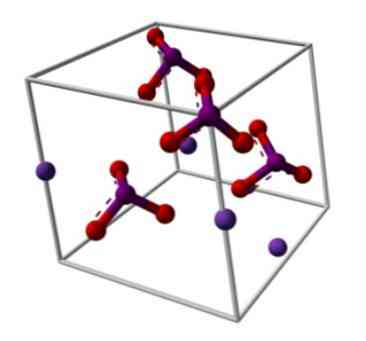
โครงสร้างทางเคมีของโพแทสเซียมไอโอเดตแสดงไว้ในภาพด้านบน แอนไอออน3- ถูกแทนด้วย "ขาตั้ง" ของทรงกลมสีแดงและสีม่วงในขณะที่ไอออน K+ มันเป็นตัวแทนของทรงกลมสีม่วง.
แต่ขาตั้งเหล่านี้หมายความว่าอย่างไร รูปทรงเรขาคณิตที่ถูกต้องของแอนไอออนเหล่านี้เป็นปิรามิดในรูปสามเหลี่ยมซึ่ง oxygens ประกอบขึ้นเป็นฐานรูปสามเหลี่ยมและอิเลคตรอนคู่ที่ไม่ได้ใช้ร่วมกันในไอโอดีนชี้ขึ้นไปครอบครองพื้นที่และบังคับให้การเชื่อมโยง IO ลดลง ลิงก์ I = O.
เรขาคณิตโมเลกุลนี้สอดคล้องกับการผสมพันธุ์ sp3 ของอะตอมไอโอดีนกลาง อย่างไรก็ตามอีกมุมมองหนึ่งชี้ให้เห็นว่าหนึ่งในอะตอมของออกซิเจนสร้างพันธะกับวงโคจรของไอโอดีนในความเป็นจริงคือการผสมพันธุ์ sp3d2 (ไอโอดีนสามารถมีวงโคจร "d" ของมันที่ขยายขอบเขตวาเลนซ์ได้).
ผลึกของเกลือนี้สามารถผ่านการเปลี่ยนสถานะของโครงสร้าง (การเตรียมอื่นนอกเหนือจาก monoclinic) ซึ่งเป็นผลมาจากสภาพร่างกายที่แตกต่างกัน.
การใช้และการใช้โพแทสเซียมไอโอเดต
ใช้รักษาโรค
โพแทสเซียมไอโอเดตมักจะใช้เพื่อป้องกันการสะสมของกัมมันตภาพรังสีในต่อมไทรอยด์ในรูปแบบของ 131ฉันเมื่อไอโซโทปนี้ถูกใช้ในการหาปริมาณไอโอดีนที่ต่อมไทรอยด์เป็นส่วนประกอบของการทำงานของต่อมไทรอยด์.
ในทำนองเดียวกันโพแทสเซียมไอโอเดตใช้เป็นยาฆ่าเชื้อเฉพาะที่ (0.5%) ในการติดเชื้อเยื่อเมือก.
ใช้ในอุตสาหกรรม
มันถูกเพิ่มเข้าไปในอาหารสัตว์เลี้ยงในฟาร์มเป็นอาหารเสริมไอโอดีน ดังนั้นในอุตสาหกรรมโพแทสเซียมไอโอเดตจะใช้ในการปรับปรุงคุณภาพของแป้ง.
ใช้การวิเคราะห์
ในการวิเคราะห์ทางเคมีต้องขอบคุณความเสถียรมันถูกใช้เป็นมาตรฐานหลักในมาตรฐานของสารละลายโซเดียมไธโอซัลเฟตมาตรฐาน (Na2S2O3) เพื่อกำหนดความเข้มข้นของไอโอดีนในตัวอย่าง.
ซึ่งหมายความว่าปริมาณไอโอดีนนั้นสามารถทราบได้ด้วยเทคนิคการวิเคราะห์ปริมาตร (การไตเตรท) ในปฏิกิริยานี้โพแทสเซียมไอโอเดตจะออกซิไดซ์ไอออนไอโอไดด์อย่างรวดเร็ว-, โดยสมการทางเคมีต่อไปนี้:
IO3- + 5I- + 6H+ => 3I2 + 3H2O
ไอโอดีนฉัน2, มีบรรดาศักดิ์เป็นคำตอบของนา2S2O3 สำหรับมาตรฐาน.
ใช้ในเทคโนโลยีเลเซอร์
การศึกษาได้แสดงให้เห็นและยืนยันคุณสมบัติที่น่าสนใจของ piezoelectric, pyroelectric, electro-optical, ferroelectric และในทัศนศาสตร์ที่ไม่ใช่เชิงเส้นของผลึก KIO3. ซึ่งส่งผลให้มีศักยภาพที่ดีในด้านอิเล็กทรอนิกส์และเทคโนโลยีเลเซอร์สำหรับวัสดุที่ทำด้วยสารนี้.
ความเสี่ยงต่อสุขภาพของโพแทสเซียมไอโอเดต
ในปริมาณที่สูงอาจทำให้เกิดการระคายเคืองในเยื่อบุในช่องปาก, ผิวหนัง, ดวงตาและระบบทางเดินหายใจ.
การทดลองความเป็นพิษของโพแทสเซียมไอโอเดตในสัตว์ได้รับอนุญาตให้สังเกตว่าในการอดอาหารสุนัขในปริมาณ 0.2-0.25 กรัม / กิโลกรัมของน้ำหนักตัวที่ให้มาทางปากสารประกอบที่ทำให้เกิดการอาเจียน.
หากมีการหลีกเลี่ยงการอาเจียนมันจะทำให้สถานการณ์แย่ลงในสัตว์เพราะมันทำให้เกิดอาการเบื่ออาหารและการนอนกรนก่อนตาย การชันสูตรพลิกศพของเขาได้รับอนุญาตให้สังเกตรอยโรคเน่าในตับไตและเยื่อบุลำไส้.
เนื่องจากพลังงานในการออกซิไดซ์จึงมีความเสี่ยงต่อไฟไหม้เมื่อสัมผัสกับวัสดุที่ติดไฟได้.
การอ้างอิง
- วัน, R. , & Underwood, A. เคมีเชิงวิเคราะห์เชิงปริมาณ (ฉบับที่ห้า) PEARSON Prentice Hall, p-364.
- Muth, D. (2008) เลเซอร์ [รูป] ดึงมาจาก: flickr.com
- ChemicalBook (2017). โพแทสเซียมไอโอเดต. สืบค้นเมื่อวันที่ 25 มีนาคม 2018 จาก ChemicalBook: chemicalbook.com
- PubChem (2018) โพแทสเซียมไอโอเดต สืบค้นเมื่อวันที่ 25 มีนาคม 2018 จาก PubChem: pubchem.ncbi.nlm.nih.gov
- เมอร์ค (2018) โพแทสเซียมไอโอเดต สืบค้นเมื่อวันที่ 25 มีนาคม 2018 จากเมอร์ค:
- merckmillipore.com
- วิกิพีเดีย (2017) โพแทสเซียมไอโอเดต สืบค้นเมื่อวันที่ 25 มีนาคม 2018 จาก Wikipedia: en.wikipedia.org
- M M Abdel Kader และคณะ (2013) ชาร์จกลไกการเคลื่อนที่และการเปลี่ยนเฟสที่อุณหภูมิต่ำใน KIO3. J. Phys.: Conf. Ser. 423 012036


