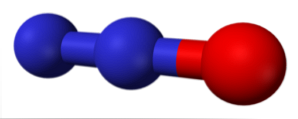
ไนโตรเจนออกไซด์ (NOx) สูตรและ Nomenclatures ที่แตกต่างกัน
ไนโตรเจนออกไซด์ พวกมันเป็นสารประกอบอนินทรีย์ที่เป็นก๊าซที่มีพันธะระหว่างอะตอมไนโตรเจนและออกซิเจน สูตรทางเคมีของกลุ่มคือหมายเลขx, แสดงว่าออกไซด์มีสัดส่วนของออกซิเจนและไนโตรเจนต่างกัน.
ไนโตรเจนเป็นผู้นำกลุ่มที่ 15 ของตารางธาตุในขณะที่กลุ่มออกซิเจน 16; องค์ประกอบทั้งสองเป็นสมาชิกของช่วงเวลาที่ 2 ความใกล้ชิดนี้เป็นเหตุผลว่าทำไมพันธบัตร N-O จึงเป็นโควาเลนต์ในออกไซด์ ด้วยวิธีนี้พันธะในไนโตรเจนออกไซด์จะมีโควาเลนต์.
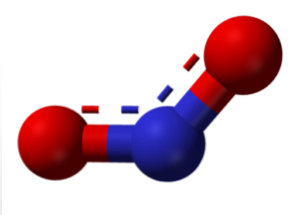
การเชื่อมโยงทั้งหมดนี้สามารถอธิบายได้โดยใช้ทฤษฎีการโคจรของโมเลกุลซึ่งเผยให้เห็น paramagnetism (อิเล็กตรอน unpaired ในการโคจรของโมเลกุลสุดท้าย) ของสารประกอบเหล่านี้ สารประกอบที่พบมากที่สุดคือไนตริกออกไซด์และไนโตรเจนไดออกไซด์.
โมเลกุลในภาพด้านบนสอดคล้องกับโครงสร้างเชิงมุมในเฟสก๊าซของไนโตรเจนไดออกไซด์2) ในทางตรงกันข้ามไนตริกออกไซด์ (NO) มีโครงสร้างเชิงเส้น (พิจารณาจากการผสมพันธุ์ sp สำหรับอะตอมทั้งสอง).
ไนโตรเจนออกไซด์เป็นก๊าซที่เกิดจากกิจกรรมของมนุษย์มากมายไม่ว่าจะเป็นการขับยานพาหนะหรือสูบบุหรี่ไปจนถึงกระบวนการทางอุตสาหกรรมซึ่งก่อให้เกิดขยะ อย่างไรก็ตามไม่มีการผลิตตามธรรมชาติโดยปฏิกิริยาของเอนไซม์และฟ้าผ่าในพายุฝนฟ้าคะนอง: N2(g) + O2(g) => 2NO (g)
อุณหภูมิสูงของรังสีจะทำลายสิ่งกีดขวางที่มีพลังซึ่งป้องกันไม่ให้ปฏิกิริยานี้เกิดขึ้นภายใต้สภาวะปกติ กำแพงพลังงานอะไร ที่เกิดจากพันธะสามตัวN≡Nทำให้โมเลกุล N2 ก๊าซเฉื่อยจากบรรยากาศ.
ดัชนี
- 1 หมายเลขออกซิเดชันสำหรับไนโตรเจนและออกซิเจนในออกไซด์
- 2 สูตรและการตั้งชื่อที่แตกต่างกัน
- 2.1 ไนตรัสออกไซด์ (N2O)
- 2.2 ไนตริกออกไซด์ (NO)
- 2.3 ไนโตรเจนออกไซด์ (N2O3)
- 2.4 ไดออกไซด์และไนโตรเจนเทตรอกไซด์ (NO2, N2O4)
- 2.5 Dinitrogen pentoxide (N2O5)
- 3 อ้างอิง
หมายเลขออกซิเดชันสำหรับไนโตรเจนและออกซิเจนในออกไซด์
การกำหนดค่าอิเล็กทรอนิกส์สำหรับออกซิเจนคือ [เขา] 2 วินาที22p4, ต้องการอิเล็กตรอนเพียงสองตัวเพื่อทำให้อ็อคเต็ตของเปลือกวาเลนซ์สมบูรณ์ นั่นคือมันสามารถรับอิเล็กตรอนสองตัวและมีเลขออกซิเดชันเท่ากับ -2.
ในทางตรงกันข้ามการตั้งค่าอิเล็กทรอนิกส์สำหรับไนโตรเจนคือ [เขา] 2 วินาที22p3, ความสามารถในการรับอิเล็กตรอนได้มากถึงสามเพื่อเติมเต็มความจุของอ็อกเทต ตัวอย่างเช่นในกรณีของแอมโมเนีย (NH3) มีหมายเลขออกซิเดชันเท่ากับ -3 แต่ออกซิเจนนั้นมีอิเลคโตรเนกาติตีมากกว่าไฮโดรเจนและ "บังคับ" ไนโตรเจนให้แบ่งอิเล็กตรอน.
ไนโตรเจนสามารถแบ่งอิเล็กตรอนได้กี่อิเล็กตรอน หากคุณแบ่งปันอิเล็กตรอนของเปลือกวาเลนซ์ของคุณทีละตัวคุณจะถึงขีด จำกัด ของอิเล็กตรอนห้าตัวซึ่งสอดคล้องกับหมายเลขออกซิเดชันที่ +5.
ดังนั้นขึ้นอยู่กับจำนวนพันธะที่เกิดขึ้นกับออกซิเจนจำนวนการเกิดออกซิเดชันของไนโตรเจนจะแตกต่างกันตั้งแต่ +1 ถึง +5.
สูตรและการตั้งชื่อต่างกัน
ไนโตรเจนออกไซด์ในการเพิ่มลำดับหมายเลขออกซิเดชันของไนโตรเจนคือ:
- ยังไม่มีข้อความ2หรือไนตรัสออกไซด์ (+1)
- NO, ไนตริกออกไซด์ (+2)
- ยังไม่มีข้อความ2O3, ไดนิโตเจนออกไซด์ (+3)
- NO2, ไนโตรเจนไดออกไซด์ (+4)
- ยังไม่มีข้อความ2O5, ไดนิโตเจน pentoxide (+5)
ไนตรัสออกไซด์ (N.)2O)
ไนตรัสออกไซด์ (หรือที่รู้จักกันอย่างแพร่หลายว่าแก๊สหัวเราะ) เป็นก๊าซไม่มีสีมีกลิ่นหวานเล็กน้อยและมีปฏิกิริยาเล็กน้อย มันสามารถมองเห็นเป็นโมเลกุล N2 (ทรงกลมสีน้ำเงิน) ที่เพิ่มอะตอมออกซิเจนที่ปลายด้านหนึ่ง มันถูกจัดทำขึ้นโดยการสลายตัวทางความร้อนของเกลือไนเตรตและใช้เป็นยาสลบและยาแก้ปวด.
ไนโตรเจนมีเลขออกซิเดชันของ +1 ในออกไซด์นี้ซึ่งหมายความว่ามันจะไม่ออกซิไดซ์มากและความต้องการอิเล็กตรอนไม่น่าสนใจ อย่างไรก็ตามคุณจะต้องได้รับอิเล็กตรอนสองตัว (หนึ่งตัวสำหรับแต่ละไนโตรเจน) เพื่อที่จะกลายเป็นโมเลกุลของไนโตรเจนที่เสถียร.
ในการแก้ปัญหาพื้นฐานและกรดปฏิกิริยาคือ:
ยังไม่มีข้อความ2O (g) + 2H+(ac) + 2e- => N2(g) + H2O (l)
ยังไม่มีข้อความ2O (g) + H2O (l) + 2e- => N2(g) + 2OH-(Aq)
ปฏิกิริยาเหล่านี้ถึงแม้ว่าอุณหพลศาสตร์จะได้รับการสนับสนุนจากการก่อตัวของโมเลกุลที่เสถียร N2, เกิดขึ้นอย่างช้าๆและรีเอเจนต์ที่บริจาคคู่อิเลคตรอนจะต้องเป็นตัวลดแรงที่มีความแข็งแรงมาก.
ไนตริกออกไซด์ (NO)
ออกไซด์นี้ประกอบด้วยก๊าซไม่มีสีปฏิกิริยาและพาราแมกเนติก เช่นเดียวกับไนตรัสออกไซด์มันมีโครงสร้างโมเลกุลเชิงเส้น แต่ด้วยความแตกต่างอย่างมากที่พันธะ N = O ก็มีลักษณะเป็นพันธะสามเท่า.
NO ถูกออกซิไดซ์อย่างรวดเร็วในอากาศเพื่อผลิต NO2, และสร้างวงโคจรโมเลกุลที่เสถียรมากขึ้นด้วยอะตอมไนโตรเจนที่ออกซิไดซ์มากขึ้น (+4).
2NO (g) + O2(g) => 2NO2(G)
การศึกษาทางชีวเคมีและสรีรวิทยาอยู่เบื้องหลังบทบาทที่เป็นพิษเป็นภัยของออกไซด์นี้ในสิ่งมีชีวิต.
มันไม่สามารถสร้างพันธะ N-N กับโมเลกุลอีกอันของ NO เนื่องจากการแยกตัวของอิเล็กตรอนที่ไม่มีคู่ในวงโคจรของโมเลกุลซึ่งถูกชี้นำมากขึ้นต่ออะตอมออกซิเจน (เนื่องจากอิเล็กตรอนสูง) ตรงกันข้ามเกิดขึ้นกับไม่มี2, ที่สามารถสร้างก๊าซหรี่แสงได้.
ไนโตรเจนออกไซด์ (N2O3)
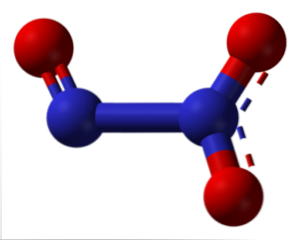
เส้นประของโครงสร้างบ่งบอกถึงการสั่นพ้องสองครั้ง เช่นเดียวกับอะตอมทั้งหมดพวกมันมี sp hybridization2, โมเลกุลนั้นแบนและปฏิสัมพันธ์ของโมเลกุลนั้นมีประสิทธิภาพเพียงพอสำหรับไนโตรเจนออกไซด์จะมีอยู่ในรูปของของแข็งสีน้ำเงินต่ำกว่า-101ºC ที่อุณหภูมิสูงขึ้นมันจะละลายและแยกตัวออกเป็น NO และ NO2.
ทำไมถึงแยกจากกัน? เนื่องจากเลขออกซิเดชัน +2 และ +4 มีความเสถียรมากกว่า +3 จึงมีอยู่ในออกไซด์สำหรับอะตอมไนโตรเจนทั้งสอง สิ่งนี้สามารถอธิบายได้อีกครั้งโดยความเสถียรของโมเลกุลออร์บิทัลอันเป็นผลมาจากความไม่สมส่วน.
ในภาพด้านซ้ายของ N2O3 สอดคล้องกับ NO ในขณะที่ด้านขวาไปที่ NO2. เหตุผลมันเกิดจากการรวมตัวกันของออกไซด์ก่อนหน้านี้ที่อุณหภูมิเย็นจัด (-20ºC) The N2O3 เป็นกรดไนตรัสแอนไฮไดรด์ (HNO)2).
ไดออกไซด์และไนโตรเจนเทตรอกไซด์ (NO2, ยังไม่มีข้อความ2O4)
NO2 มันเป็นก๊าซสีน้ำตาลหรือสีน้ำตาลปฏิกิริยาและพาราแมกเนติก เนื่องจากมันมีอิเล็กตรอนที่ไม่มีการจับคู่มันจึงลดขนาด (ผูก) กับโมเลกุลของก๊าซอื่น2 เพื่อสร้างไนโตรเจน tetroxide ก๊าซไม่มีสีสร้างสมดุลระหว่างสารเคมีทั้งสองชนิด:
2NO2(G) <=> ยังไม่มีข้อความ2O4(G)
มันเป็นสารออกซิไดซ์ที่เป็นพิษและหลากหลายที่มีความสามารถในการแบ่งสัดส่วนปฏิกิริยารีดอกซ์ในไอออน (oxoanions)2- และไม่3- (สร้างฝนกรด) หรือในหมายเลข.
ในทำนองเดียวกันไม่มี2 มีส่วนร่วมในปฏิกิริยาบรรยากาศที่ซับซ้อนซึ่งก่อให้เกิดการเปลี่ยนแปลงของความเข้มข้นของโอโซน (OR3) ในระดับพื้นโลกและในสตราโตสเฟียร์.
Dinitrogen pentoxide (N2O5)
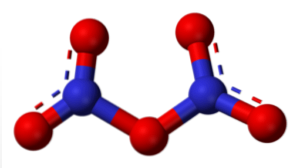
เมื่อถูกไฮเดรตมันจะสร้าง HNO3, และที่ความเข้มข้นที่สูงขึ้นของกรดออกซิเจนส่วนใหญ่จะถูกโปรตอนด้วยประจุบวกบางส่วน -O+-H เร่งปฏิกิริยารีดอกซ์
การอ้างอิง
- askIITians ((2006-2018)). askIITians. สืบค้นเมื่อวันที่ 29 มีนาคม 2018 จาก askIITians: askiitians.com
- สารานุกรม Britannica, Inc. (2018). สารานุกรมบริแทนนิกา. สืบค้นเมื่อ 29 มีนาคม 2018 จาก Encyclopaedia Britannica: britannica.com
- เมืองท็อกซ์ (2017). เมืองท็อกซ์. สืบค้นเมื่อวันที่ 29 มีนาคม 2018 จาก Tox Town: toxtown.nlm.nih.gov
- ศาสตราจารย์แพทริเซียแชปลีย์ (2010) ไนโตรเจนออกไซด์ในบรรยากาศ มหาวิทยาลัยอิลลินอยส์ สืบค้นเมื่อวันที่ 29 มีนาคม 2018 จาก: butane.chem.uiuc.edu
- ตัวสั่นและแอตกินส์ (2008) เคมีอนินทรีย์ ใน องค์ประกอบของกลุ่ม 15. (ฉบับที่สี่, หน้า 361-366) Mc Graw Hill