ปฏิกิริยาสะพอนิฟิเคชันและสารที่สามารถรับได้
สะพอ มันคือการย่อยสลายพื้นฐานของเอสเตอร์ ซึ่งหมายความว่าเอสเตอร์ทำปฏิกิริยากับเบส (NaOH หรือ KOH) ย้อนกลับไม่ได้ผลิตแอลกอฮอล์และคาร์บอกซีเลตของโซเดียมหรือโพแทสเซียม คำนี้หมายถึง "การผลิตสบู่" และอันที่จริงแล้วเป็นหนึ่งในปฏิกิริยาเคมีที่เก่าแก่ที่สุดที่มนุษย์ใช้.
ในสมัยบาบิโลนด้วยความช่วยเหลือจากเถ้าถ่านที่เก็บจากไม้และพืชและไขมันจากสัตว์พวกเขาได้สร้างศิลปะการทำสบู่ให้สมบูรณ์ ทำไมสัตว์อ้วน เหตุผลคือมันอุดมไปด้วย glycerol tryters (ไตรกลีเซอไรด์) และขี้เถ้าไม้เป็นแหล่งโพแทสเซียมซึ่งเป็นโลหะพื้นฐาน.
มิเช่นนั้นปฏิกิริยาจะเกิดผลตอบแทนที่ต่ำกว่า แต่ก็เพียงพอที่จะสะท้อนถึงผลกระทบต่อสีและพื้นผิวบางส่วน ดังกล่าวเป็นกรณีของภาพวาดสีน้ำมันที่เม็ดสีผสมกับน้ำมัน (แหล่งที่มาของเอสเทอร์).
ดัชนี
- 1 ปฏิกิริยาสะพอนิฟิเคชัน
- 1.1 กลไก
- 1.2 จลนพลศาสตร์
- 2 สารที่สามารถรับได้โดยสะพอนิฟิเคชัน
- 2.1 การกระทำของตัวทำละลายสบู่
- 3 อ้างอิง
ปฏิกิริยาสะพอนิฟิเคชัน
กลไก
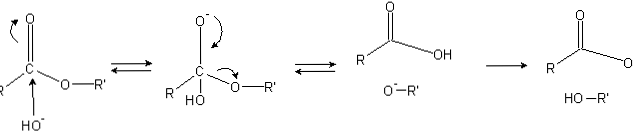
เอสเทอร์มีกลุ่มอะซิล (O = C-R) ซึ่งมีความไวต่อการถูกโจมตีจากนิวคลีโอฟิลเช่น OH-.
เนื่องจากออกซิเจนอะตอม "ขโมย" ความหนาแน่นทางอิเล็กทรอนิกส์จากอะตอมคาร์บอนมันมีประจุบางส่วนดังนั้นในกรณีของเอสเทอร์.
ดังนั้นประจุบวกนี้จึงดึงดูดสปีชีส์ลบที่สามารถส่งอิเล็กตรอนไปยังอะตอมของคาร์บอนโดยเกิดการโจมตีของนิวคลีโอฟิลลิค (ด้านซ้ายของภาพ) เป็นผลให้เกิด tetrahedral ตัวกลาง (โมเลกุลที่สองจากซ้ายไปขวา) เกิดขึ้น.
ประจุลบของออกซิเจนของตัวกลางเตตระฮีดรัลนั้นเป็นผลผลิตของ OH- ที่ล้อมรอบ จากนั้นประจุลบนี้จะถูกแยกออกเพื่อสร้างกลุ่มคาร์บอนิล "บังคับ" แล้วทำลายพันธะ C-OR นอกจากนี้การย้ายตำแหน่งนี้สร้างกรดคาร์บอกซิลิก RCOOH และ alkoxide ion R'O-.
ในที่สุดเมื่อตัวกลางเกิดปฏิกิริยาเป็นสารพื้นฐาน alkoxide จะลดลงหนึ่งโมเลกุลของน้ำและกรดคาร์บอกซิลิกจะทำปฏิกิริยากับ OH อื่น- ของกลางสร้างผลิตภัณฑ์ของ saponification.
จลนศาสตร์
ความเร็วของปฏิกิริยาสะพอนิฟิเคชันนั้นแปรผันตามความเข้มข้นของสารตั้งต้น กล่าวอีกนัยหนึ่งการเพิ่มความเข้มข้นของเอสเตอร์ (RCOOR ') หรือฐาน (NaOH) ปฏิกิริยาจะดำเนินต่อไปในอัตราที่สูงขึ้น.
นอกจากนี้ยังมีการแปลดังนี้อัตราการสะพอนิฟิเคชันเป็นคำสั่งแรกที่เกี่ยวข้องกับเอสเตอร์และคำสั่งแรกที่เกี่ยวข้องกับฐาน ด้านบนสามารถแสดงด้วยสมการทางคณิตศาสตร์ต่อไปนี้:
ความเร็ว = k [RCOOR '] [NaOH]
เมื่อ k คือสัมประสิทธิ์คงที่หรือความเร็วซึ่งแตกต่างกันไปตามหน้าที่ของอุณหภูมิหรือความดัน นั่นคือยิ่งความร้อนสูงเท่าไหร่ความเร็วในการสะพอนิฟิเคชั่นก็จะยิ่งมากขึ้นเท่านั้น ด้วยเหตุนี้สื่อจึงเดือด.
เนื่องจากรีเอเจนต์ทั้งคู่เป็นอันดับแรกจลนศาสตร์ปฏิกิริยาโดยรวมจึงเป็นลำดับที่สอง.
ในกลไกปฏิกิริยาของ saponification การก่อตัวของ tetrahedral ตัวกลางจำเป็นต้องมีการโจมตี nucleophilic ซึ่งเกี่ยวข้องกับทั้งเอสเตอร์และฐาน.
ดังนั้นจลนพลศาสตร์อันดับที่สองจึงสะท้อนให้เห็นในความเป็นจริงนี้เพราะพวกมันเข้าไปแทรกแซงในขั้นตอนดีเทอร์มิแนนต์ (ช้า) ของปฏิกิริยา.
สารที่สามารถหาได้โดยสะพอนิฟิเคชัน

ผลิตภัณฑ์หลักของซาพอนิฟิเคชันคือแอลกอฮอล์และเกลือของกรดคาร์บอกซิลิก ในกรดขนาดกลาง RCOOH ที่เกี่ยวข้องซึ่งได้จากการสะพอนิฟิเคชั่นของไขมันและน้ำมันซึ่งเป็นที่รู้จักกันว่ากรดไขมันจะได้รับ.
ด้วยวิธีนี้สบู่ประกอบด้วยเกลือของกรดไขมันที่เกิดจากสะพอนิฟิ คุณออกไปกับแคทอะไรบ้าง? พวกเขาสามารถนา+, K+, มก.2+, ความเชื่อ3+, ฯลฯ.
เกลือเหล่านี้ละลายได้ในน้ำ แต่เกิดการตกตะกอนจากการกระทำของ NaCl ที่เติมลงในส่วนผสมซึ่งจะทำให้สบู่ระเหยและแยกออกจากเฟสของน้ำ ปฏิกิริยาสะพอนิฟิเคชันสำหรับไตรกลีเซอไรด์มีดังนี้:
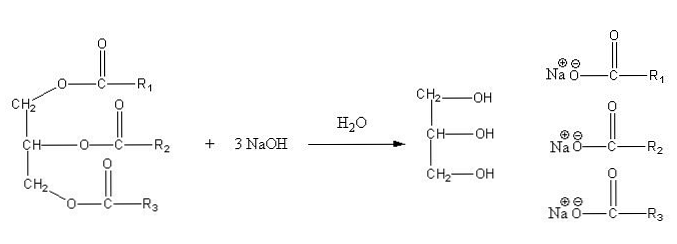
กลีเซอรีนเป็นแอลกอฮอล์ "E" และสบู่เป็นเกลือของกรดไขมันที่เกิดขึ้นทั้งหมด ที่นี่แต่ละ sidechain -R มีความยาวและระดับความไม่ลงรอยกันต่างกัน ดังนั้นโซ่เหล่านี้สร้างความแตกต่างระหว่างไขมันและน้ำมันพืช.
กุญแจสำคัญในการผลิตสบู่นั้นอยู่ในการเลือกไขมันและน้ำมันที่ดีที่สุดหรือเฉพาะเจาะจงมากขึ้นในการเลือกแหล่งของไตรกลีเซอไรด์ที่แตกต่างกัน.
มวลสบู่สีขาวนี้อาจมีสีย้อมและสารประกอบอินทรีย์อื่น ๆ ในโครงสร้างทำให้มีกลิ่นหอมและสีสดใส จากที่นี่ช่วงของความเป็นไปได้ถูกทำให้เชื่องโดยศิลปะและอาชีพในการค้านี้.
อย่างไรก็ตามปฏิกิริยาสะพอนิฟิเคชันยังเป็นเส้นทางสังเคราะห์ของกรดคาร์บอกซิลิกและแอลกอฮอล์ที่ไม่จำเป็นต้องเกี่ยวข้องกับกลีเซอรีนหรือสบู่.
ตัวอย่างเช่นการไฮโดรไลซิสพื้นฐานของเอสเตอร์ใด ๆ เช่นเอทิลอะซิเตตอย่างง่ายจะผลิตกรดอะซิติกและเอทานอล.
การกระทำของตัวทำละลายสบู่

เกลือของกรดไขมันนั้นละลายได้ในน้ำ แต่ไม่ใช่ในลักษณะเดียวกับไอออนที่ถูกละลาย นั่นคือล้อมรอบด้วยทรงกลมน้ำ ในกรณีของสบู่โซ่ข้างของพวกเขา -R ป้องกันพวกเขาในทางทฤษฎีจากการละลายในน้ำ.
ดังนั้นเพื่อต่อสู้กับตำแหน่งที่รู้สึกไม่สบายตัวนี้พวกมันจะเน้นในลักษณะที่โซ่เหล่านี้สัมผัสกันก่อตัวเป็นนิวเคลียสของเซลล์ออพติคอลขณะที่หัวขั้วโลกปลาย (-COO)- นา+) โต้ตอบกับโมเลกุลของน้ำและสร้าง "ขั้วเปลือกหอย".
ภาพด้านบนแสดงในภาพด้านบนซึ่งโครงสร้างประเภทนี้เรียกว่าไมเซลล์.
"หางสีดำ" ตรงกับโซ่ที่ไม่ชอบน้ำกลายเป็นพันกันในแกนอินทรีย์ที่ได้รับการคุ้มครองโดยทรงกลมสีเทา ทรงกลมสีเทาเหล่านี้ประกอบเป็นโล่ขั้วโลกหัว -COO- นา+.
จากนั้น micelles จะเป็นกลุ่ม (clusters) ของเกลือของกรดไขมัน ภายในสิ่งเหล่านี้สามารถห่อหุ้มไขมันซึ่งไม่ละลายในน้ำ.
พวกเขาจะทำอย่างไร ทั้งไขมันและโซ่ -R นั้นไม่ชอบน้ำดังนั้นทั้งคู่จึงมีความสัมพันธ์ที่ดีต่อกัน.
เมื่อไมเลสล้อมรอบไขมันน้ำจะทำปฏิกิริยากับเปลือกขั้วโลกทำให้สามารถละลายสบู่ได้ ในทำนองเดียวกัน micelles มีประจุลบทำให้เกิดการผลักกันซึ่งกันและกันและทำให้เกิดการกระจายตัวของไขมัน.
การอ้างอิง
- Anne Marie Helmenstine, Ph.D. (3 ตุลาคม 2017) คำจำกัดความของปฏิกิริยาสะพอนิฟิเคชันและปฏิกิริยา สืบค้นเมื่อวันที่ 24 เมษายน 2018 จาก: thoughtco.com
- Francis A. Carey เคมีอินทรีย์ กรดคาร์บอกซิลิก (รุ่นที่หก, หน้า 863-866) Mc Graw Hill.
- Graham Solomons T.W. , Craig B. Fryhle เคมีอินทรีย์ ไขมัน (ฉบับที่ 10, หน้า 1056-1058) ไวลีย์พลัส.
- วิกิพีเดีย (2018) saponification สืบค้นเมื่อวันที่ 24 เมษายน 2018 จาก: en.wikipedia.org
- Boyd C. (27 กุมภาพันธ์ 2558) ทำความเข้าใจเกี่ยวกับเคมีและประวัติของสบู่ สืบค้นเมื่อวันที่ 24 เมษายน 2018 จาก: chemservice.com
- Luca Laghi (27 มีนาคม 2550) saponification สืบค้นเมื่อวันที่ 24 เมษายน 2018 จาก: commons.wikimedia.org
- ถัก Amanda (12 พฤษภาคม 2558) Micelle (ระดับสีเทา) สืบค้นเมื่อวันที่ 24 เมษายน 2018 จาก: commons.wikimedia.org


