กฎหมายของประวัติศาสตร์ Boyle-Mariotte, การแสดงออกทางคณิตศาสตร์, ตัวอย่าง
กฎหมายของ บอยล์ คือสิ่งที่แสดงออกถึงความสัมพันธ์ระหว่างแรงดันที่กระทำโดยหรือกับก๊าซและปริมาตรที่ถูกครอบครองโดยมัน; รักษาอุณหภูมิของก๊าซให้คงที่ตลอดจนปริมาณ (จำนวนโมล).
กฎหมายฉบับนี้ร่วมกับเรื่องของ Charles, Gay-Lussac, Charles และ Avogadro อธิบายถึงพฤติกรรมของก๊าซอุดมคติ โดยเฉพาะในภาชนะปิดซึ่งมีการเปลี่ยนแปลงของปริมาตรที่กระทำโดยแรงทางกล.
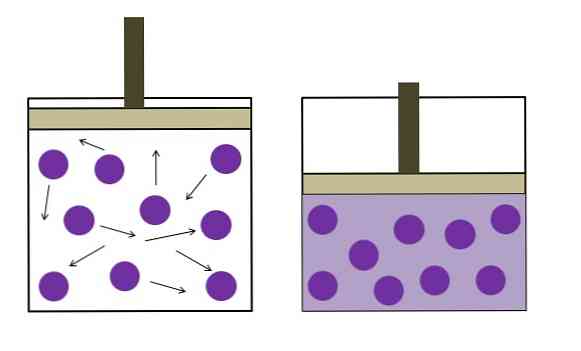
ภาพด้านบนสรุปกฎหมาย Boyle-Mariotte สั้น ๆ.
จุดสีม่วงแสดงถึงโมเลกุลหรืออะตอมของก๊าซซึ่งชนกับผนังด้านในของภาชนะบรรจุ (ซ้าย) โดยการลดพื้นที่ว่างหรือปริมาตรของภาชนะบรรจุที่ครอบครองโดยก๊าซนี้การชนเพิ่มขึ้นซึ่งแปลเป็นการเพิ่มความดัน (ขวา).
นี่แสดงให้เห็นว่าแรงดัน P และปริมาตร V ของก๊าซเป็นสัดส่วนผกผันหากบรรจุภัณฑ์ปิดผนึกอย่างแน่นหนา มิฉะนั้นความดันที่สูงขึ้นจะเท่ากับการขยายตัวที่มากขึ้นของภาชนะบรรจุ.
หากพล็อต V ถูกสร้างขึ้นกับ P โดยมีข้อมูลของ V และ P บนแกน Y และ X ตามลำดับจะพบเส้นโค้งแบบอะซิมโทติค ขนาดเล็กกว่าคือ V ยิ่งเพิ่ม P มากขึ้น นั่นคือเส้นโค้งจะขยายไปถึงค่าสูงของ P บนแกน X.
แน่นอนอุณหภูมิคงที่ แต่ถ้าทำการทดลองเดียวกันที่อุณหภูมิแตกต่างกันตำแหน่งสัมพัทธ์ของเส้นโค้งเหล่านี้ V vs P จะเปลี่ยนไปในแกนคาร์ทีเซียน การเปลี่ยนแปลงจะชัดเจนยิ่งขึ้นหากมีการพล็อตบนแกนสามมิติโดยมีค่าคงที่ T บนแกน Z.
ดัชนี
- 1 ประวัติกฎหมายของ Boyle
- 1.1 ความเป็นมา
- 1.2 การทดลองกับปรอท
- 1.3 Edme Mariotte
- 1.4 การเสริมสร้างกฎหมาย
- 2 กฎหมายนี้ประกอบด้วยอะไร??
- 3 การแสดงออกทางคณิตศาสตร์
- 4 มีไว้เพื่ออะไร? กฎหมายของ Boyle แก้ปัญหาอะไรได้บ้าง?
- 4.1 เครื่องทำไอน้ำ
- 4.2 จิบเครื่องดื่ม
- 4.3 ระบบทางเดินหายใจ
- 5 ตัวอย่าง (การทดลอง)
- 5.1 การทดลอง 1
- 5.2 การทดลอง 2
- 6 อ้างอิง
ประวัติกฎหมายของบอยล์
พื้นหลัง
เนื่องจากนักวิทยาศาสตร์กาลิเลโอกาลิลีแสดงความเชื่อของเขาในการมีอยู่ของความว่างเปล่า (1638) นักวิทยาศาสตร์เริ่มศึกษาคุณสมบัติของอากาศและช่องว่างบางส่วน.
นักเคมีชาวแองโกล - ไอริชโรเบิร์ตบอยล์เริ่มศึกษาคุณสมบัติของอากาศในปี 1638 จากการเรียนรู้ว่า Otto von Guericke วิศวกรชาวเยอรมันและนักฟิสิกส์ได้สร้างปั๊มลมขึ้น.
ทดลองกับสารปรอท
เพื่อศึกษาความดันอากาศ Boyle ใช้หลอดแก้วในรูปของ "J" ซึ่งการก่อสร้างนั้นมาจาก Robert Hooke ผู้ช่วยของ Boyle ปลายแขนสั้นถูกผนึกในขณะที่ปลายแขนยาวของหลอดถูกเปิดเพื่อวางปรอท.
จากจุดเริ่มต้น Boyle ต้องการศึกษาความยืดหยุ่นของอากาศคุณภาพและปริมาณ ด้วยการเทปรอทผ่านปลายเปิดของหลอดรูปตัว "J" Boyle อนุมานได้ว่าอากาศในแขนสั้นของหลอดหดตัวภายใต้แรงดันของปรอท.
ผล
ยิ่งมีปริมาณปรอทเพิ่มขึ้นในหลอดมากเท่าไหร่ความดันก็ยิ่งมากขึ้นเท่านั้นและปริมาตรก็จะลดลง Boyle ได้รับกราฟชนิดเอ็กซ์โปเนนเชียลลบของปริมาณอากาศเป็นฟังก์ชันของความดัน.
ในขณะที่ถ้าคุณพล็อตปริมาตรของอากาศกับค่าผกผันของความดันคุณมีเส้นตรงของความชันเป็นบวก.
ในปี ค.ศ. 1662 บอยล์ได้ตีพิมพ์กฎทางกายภาพข้อแรกที่ได้รับในรูปแบบของสมการ ในกรณีนี้ความดันและปริมาตร.
Boyle ชี้ให้เห็นว่ามีความสัมพันธ์แบบผกผันระหว่างแรงดันที่กระทำกับก๊าซและปริมาตรที่ครอบครองโดยก๊าซนั้นอัตราส่วนนี้ค่อนข้างจะเป็นจริงสำหรับก๊าซจริง ก๊าซส่วนใหญ่ทำตัวเหมือนก๊าซในอุดมคติที่ความดันและอุณหภูมิปานกลาง.
ด้วยความกดดันที่สูงขึ้นและอุณหภูมิที่ลดลงความเบี่ยงเบนจากพฤติกรรมของก๊าซที่แท้จริงของอุดมคติก็ยิ่งชัดเจนขึ้น.
Edme Mariotte
นักฟิสิกส์ชาวฝรั่งเศส Edme Mariotte (1620-1684) ค้นพบกฎหมายเดียวกันในปี 1679 โดยอิสระ แต่มีข้อดีที่แสดงให้เห็นว่าปริมาตรแปรผันตามอุณหภูมิ นั่นเป็นเหตุผลที่เรียกว่ากฎหมายของ Mariotte หรือกฎหมายของ Boyle และ Mariotte.
เสริมสร้างกฎหมาย
Daniel Bernoulli (1737) เสริมกฎหมายของ Boyle โดยชี้ให้เห็นว่าแรงดันของก๊าซเกิดจากผลกระทบของอนุภาคก๊าซบนผนังของภาชนะบรรจุ.
ในปี 1845 John Waterston ตีพิมพ์บทความทางวิทยาศาสตร์ซึ่งเขามุ่งเน้นไปที่หลักการสำคัญของทฤษฎีจลน์ของก๊าซ.
ต่อมา Rudolf Clausius, James Maxwell และ Ludqwig Boltzmann ได้รวมทฤษฎีจลน์ของแก๊สซึ่งเกี่ยวข้องกับแรงดันที่กระทำโดยแก๊สกับความเร็วของอนุภาคของก๊าซที่เคลื่อนที่.
ยิ่งปริมาตรของภาชนะบรรจุน้อยลงก๊าซยิ่งมีความถี่ของผลกระทบของอนุภาคที่ก่อตัวกับผนังของภาชนะบรรจุมากขึ้นเท่านั้น และยิ่งความดันมากขึ้นจากก๊าซ.
กฎหมายนี้ประกอบด้วยอะไรบ้าง??
การทดลองดำเนินการโดย Boyle ชี้ให้เห็นว่ามีความสัมพันธ์แบบผกผันระหว่างปริมาตรที่ครอบครองโดยก๊าซและแรงดันที่กระทำต่อมัน อย่างไรก็ตามความสัมพันธ์ดังกล่าวไม่ได้เป็นเส้นตรงทั้งหมดตามที่ระบุโดยกราฟของการเปลี่ยนแปลงปริมาณตามความดันที่เกิดจาก Boyle.
ในกฎของบอยล์ชี้ให้เห็นว่าปริมาตรที่ถูกครอบครองโดยแก๊สนั้นแปรผกผันกับความดัน นอกจากนี้ยังแสดงให้เห็นว่าผลิตภัณฑ์ของความดันของก๊าซโดยปริมาตรคงที่.
การแสดงออกทางคณิตศาสตร์
ในการรับการแสดงออกทางคณิตศาสตร์ของกฎหมาย Boyle-Mariotte เราเริ่มต้นจาก:
V α 1 / P
โดยที่มันบ่งบอกว่าปริมาตรที่ครอบครองโดยแก๊สจะแปรผกผันกับความดัน อย่างไรก็ตามมีค่าคงที่ที่กำหนดว่าสัดส่วนของความสัมพันธ์นี้ผกผันกันอย่างไร.
V = k / P
โดยที่ k คือค่าคงที่ของสัดส่วน การล้าง k คุณมี:
VP = k
ผลิตภัณฑ์ของความดันของก๊าซโดยปริมาตรคงที่ แล้ว:
V1P1 = k และ V2P2 = k
และจากนี้ก็สามารถสรุปได้ว่า:
V1P1 = V2P2
หลังเป็นสำนวนหรือสมการสุดท้ายสำหรับกฎของ Boyle.
มีไว้เพื่ออะไร? กฎหมายของ Boyle แก้ปัญหาอะไรได้บ้าง?
เครื่องอบไอน้ำ

กฎหมายของ Boyle-Mariotte ใช้กับการทำงานของเครื่องยนต์ไอน้ำ เป็นเครื่องยนต์สันดาปภายนอกที่ใช้การแปลงพลังงานความร้อนจากปริมาณน้ำเป็นพลังงานกล.
น้ำถูกทำให้ร้อนในหม้อไอน้ำที่ปิดผนึกอย่างแน่นหนาและไอน้ำที่ผลิตออกแรงกดดันตามกฎหมาย Boyle-Mariote ที่สร้างการขยายปริมาตรของกระบอกสูบโดยการกดลูกสูบ.
การเคลื่อนที่เชิงเส้นของลูกสูบถูกเปลี่ยนเป็นการเคลื่อนที่แบบหมุนโดยใช้ระบบของข้อเหวี่ยงและข้อเหวี่ยงซึ่งสามารถขับเคลื่อนล้อของหัวรถจักรหรือหัวโรเตอร์ของเครื่องกำเนิดไฟฟ้า.
ปัจจุบันเครื่องยนต์ไอน้ำทางเลือกเป็นเครื่องยนต์ที่ใช้แล้วเนื่องจากถูกแทนที่ด้วยมอเตอร์ไฟฟ้าและเครื่องยนต์สันดาปภายในในยานพาหนะขนส่ง.
จิบเครื่องดื่ม
การกระทำของการดูดเครื่องดื่มหรือน้ำผลไม้จากขวดผ่านหลอดพลาสติกที่เกี่ยวข้องกับกฎหมาย Boyle-Mariotte เมื่ออากาศถูกดูดออกจากหลอดโดยใช้ปากก็จะมีแรงดันภายในหลอดลดลง.
แรงดันตกนี้ทำให้การเคลื่อนที่ของของเหลวในหลอดสูงขึ้นทำให้สามารถกลืนเข้าไปได้ หลักการเดียวกันนี้ทำงานในการสกัดเลือดโดยใช้เข็มฉีดยา.
ระบบทางเดินหายใจ
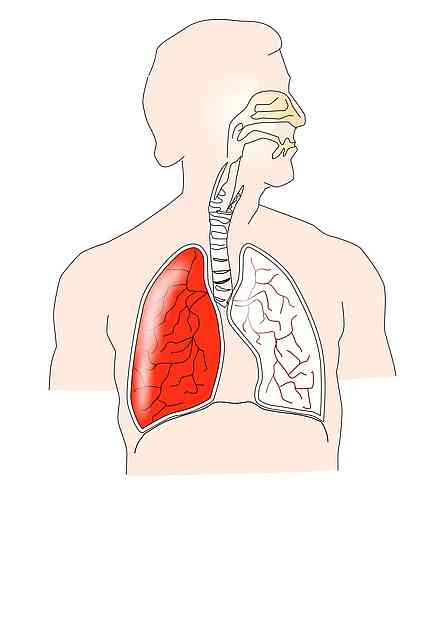
กฎหมายของ Boyle-Mariotte นั้นเกี่ยวข้องกับการทำงานของระบบทางเดินหายใจอย่างใกล้ชิด ในช่วงระยะการดลใจการหดตัวของไดอะแฟรมและกล้ามเนื้ออื่น ๆ เกิดขึ้น ตัวอย่างเช่น intercostals ภายนอกที่สร้างการขยายตัวของกรงซี่โครง.
สิ่งนี้ทำให้ความดันภายใน intrapleural ลดลงซึ่งทำให้เกิดการขยายตัวของปอดซึ่งทำให้ปริมาณปอดเพิ่มขึ้น ดังนั้นความดัน intrapulmonary จะลดลงตามสิ่งที่ระบุไว้ในกฎหมาย Boyle-Mariotte.
เมื่อความดันภายในปอดเป็น subatmospheric อากาศในชั้นบรรยากาศจะไหลเข้าสู่ปอดทำให้ความดันในปอดเพิ่มขึ้น เท่ากับความดันของมันต่อความดันบรรยากาศและสรุปขั้นตอนของแรงบันดาลใจ.
หลังจากนั้นกล้ามเนื้อหายใจเข้าจะคลายตัวและกล้ามเนื้อหายใจจะหดตัว นอกจากนี้การหดตัวของปอดยืดหยุ่นเกิดขึ้นซึ่งเป็นปรากฏการณ์ที่ทำให้ปริมาตรปอดลดลงพร้อมกับการเพิ่มขึ้นของความดัน intrapulmonary ซึ่งสามารถอธิบายได้โดยกฎหมาย Boyle-Mariotte.
โดยการเพิ่มความดัน intrapulmonary และยิ่งใหญ่กว่าความดันบรรยากาศอากาศไหลจากภายในปอดเข้าไปในบรรยากาศ สิ่งนี้จะเกิดขึ้นจนกว่าแรงกดดันจะถูกทำให้เท่ากันซึ่งสรุปขั้นตอนการหมดอายุ.
ตัวอย่าง (การทดลอง)
การทดลอง 1
บอลลูนขนาดเล็กถูกวางไว้อย่างแน่นหนาทำให้เกิดปมในปากของมันภายในหลอดฉีดยาซึ่งมีการถอดลูกสูบออกประมาณ 20 มล. ลูกสูบของกระบอกฉีดยาจะถูกวางไว้ตรงกลางของกระบอกฉีดยาเข็มจะถูกลบออกและช่องอากาศเข้าจะถูกขัดขวาง.
การสังเกต
โดยการดึงลูกสูบของหัวฉีดอย่างช้าๆจะพบว่าบอลลูนพองตัว.
คำอธิบาย
แรงกดสองครั้งจะกระทำที่ผนังของบอลลูน: แรงกดบนใบหน้าด้านใน, ผลิตภัณฑ์ของอากาศที่บรรจุอยู่ภายในบอลลูน, และแรงดันอีกอันบนใบหน้าด้านนอกของบอลลูน, ออกแรงโดยอากาศที่มีอยู่ในกระบอกฉีดยา.
เมื่อดึงลูกสูบของหัวฉีดจะเกิดครึ่งสูญญากาศขึ้นภายใน ดังนั้นความดันอากาศบนใบหน้าด้านนอกของผนังปั๊มจึงลดลงทำให้แรงดันภายในปั๊มค่อนข้างมาก.
แรงกดดันทางตาข่ายนี้ตามกฎหมาย Boyle-Mariote จะทำให้เกิดการขยายตัวของกำแพงบอลลูนและการเพิ่มปริมาณของบอลลูน.
การทดลอง 2
ตัดขวดพลาสติกประมาณครึ่งหนึ่งเพื่อให้แน่ใจว่าการตัดอยู่ในแนวนอนมากที่สุด ในปากขวดจะวางบอลลูนที่ปรับได้อย่างดีในขณะเดียวกันก็มีน้ำจำนวนหนึ่งวางอยู่ในจานลึก.
การสังเกต
โดยการวางก้นขวดด้วยลูกโป่งบนน้ำของจานบอลลูนจะพองตัวในระดับปานกลาง.
คำอธิบาย
น้ำแทนที่อากาศจำนวนหนึ่งเพิ่มความดันของอากาศบนผนังขวดและการตกแต่งภายในของบอลลูน สาเหตุนี้ตามกฎหมายของ Boyle-Mariotte การเพิ่มขึ้นของปริมาณของโลกซึ่งถูกมองเห็นได้จากอัตราเงินเฟ้อของโลก.
การอ้างอิง
- วิกิพีเดีย (2019) กฎหมายของ Boyle สืบค้นจาก: en.wikipedia.org
- บรรณาธิการสารานุกรมบริแทนนิกา (27 กรกฎาคม 2018) กฎหมายของ Boyle สารานุกรมบริแทนนิกา ดึงมาจาก: britannica.com
- Helmenstine, Todd (5 ธันวาคม 2018) สูตรสำหรับกฎของ Boyle ดึงมาจาก: thoughtco.com
- ภาพยนตร์หนุ่มอินเดีย (15 พฤษภาคม 2018) กฎของ Boyle: การทดลองวิทยาศาสตร์สำหรับเด็ก ดึงมาจาก: yifindia.com
- Cecilia Bembibre (22 พฤษภาคม 2011) บอลลูนลมร้อน นิยาม ABC ดึงมาจาก: definicionabc.com
- Ganong, W, F. (2003) สรีรวิทยาการแพทย์ (ฉบับที่ 19) บทบรรณาธิการคู่มือทันสมัย.


