แคลเซียมฟอสเฟต (Ca3 (PO4) 2) โครงสร้างคุณสมบัติการก่อตัวและการใช้งาน
แคลเซียมฟอสเฟต เป็นเกลืออนินทรีย์และตติยภูมิซึ่งมีสูตรทางเคมีคือ Ca3(PO4)2. สูตรระบุว่าองค์ประกอบของเกลือนี้คือ 3: 2 สำหรับแคลเซียมและฟอสเฟตตามลำดับ สิ่งนี้สามารถเห็นได้โดยตรงในภาพด้านล่างซึ่งมีการแสดง Ca cation2+ และประจุลบ PO43-. สำหรับทุก ๆ สาม Ca2+ มีสอง PO43- มีปฏิสัมพันธ์กับพวกเขา.
ในทางกลับกันแคลเซียมฟอสเฟตหมายถึงชุดของเกลือที่แตกต่างกันไปขึ้นอยู่กับอัตราส่วน Ca / P เช่นเดียวกับระดับของความชุ่มชื้นและ pH ในความเป็นจริงมีแคลเซียมฟอสเฟตหลายชนิดที่มีอยู่และสามารถสังเคราะห์ได้ อย่างไรก็ตามตามการตั้งชื่ออย่างแท้จริงแคลเซียมฟอสเฟตหมายถึง tricalcium เท่านั้นที่กล่าวมา.

แคลเซียมฟอสเฟตทั้งหมดรวมถึง Ca3(PO4)2, พวกเขาเป็นสีขาวทึบกับโทนสีเทาเล็กน้อย พวกมันสามารถเป็นเม็ดละเอียดเม็ดผลึกและมีขนาดอนุภาคที่อยู่รอบไมโครมิเตอร์ และแม้กระทั่งอนุภาคนาโนของฟอสเฟตเหล่านี้ก็ถูกเตรียมไว้ด้วยซึ่งวัสดุชีวภาพที่เข้ากันได้กับกระดูกถูกออกแบบมา.
ความเข้ากันได้ทางชีวภาพนี้เกิดจากความจริงที่ว่าเกลือเหล่านี้พบในฟันและในระยะสั้นในเนื้อเยื่อกระดูกของสัตว์เลี้ยงลูกด้วยนม ยกตัวอย่างเช่นไฮดรอกซีอะพาไทต์เป็นผลึกแคลเซียมฟอสเฟตซึ่งจะทำปฏิกิริยากับเฟสอสัณฐานของเกลือเดียวกัน.
ซึ่งหมายความว่ามีแคลเซียมฟอสเฟตอสัณฐานและผลึกอยู่ ด้วยเหตุนี้ความหลากหลายและตัวเลือกที่หลากหลายจึงไม่น่าแปลกใจเมื่อสังเคราะห์วัสดุที่ใช้แคลเซียมฟอสเฟต วัสดุที่นักวิจัยด้านอสังหาริมทรัพย์สนใจมากขึ้นทุกวันทั่วโลกเพื่อมุ่งเน้นการฟื้นฟูกระดูก.
ดัชนี
- 1 โครงสร้างของแคลเซียมฟอสเฟต
- 1.1 แคลเซียมฟอสเฟตอสัณฐาน
- 1.2 ครอบครัวที่เหลือ
- 2 คุณสมบัติทางกายภาพและทางเคมี
- 2.1 ชื่อ
- 2.2 น้ำหนักโมเลกุล
- 2.3 ลักษณะทางกายภาพ
- 2.4 Taste
- 2.5 จุดหลอมเหลว
- 2.6 การละลาย
- 2.7 ความหนาแน่น
- 2.8 ดัชนีหักเห
- 2.9 มาตรฐานการฝึกอบรม
- 2.10 อุณหภูมิการเก็บรักษา
- 2.11 pH
- 3 การฝึกอบรม
- 3.1 แคลเซียมไนเตรทและแอมโมเนียมไฮโดรเจนฟอสเฟต
- 3.2 แคลเซียมไฮดรอกไซด์และกรดฟอสฟอริก
- 4 ใช้
- 4.1 ในเนื้อเยื่อกระดูก
- 4.2 ซีเมนต์ชีวภาพ Bioceramic
- 4.3 แพทย์
- 4.4 อื่น ๆ
- 5 อ้างอิง
โครงสร้างของแคลเซียมฟอสเฟต
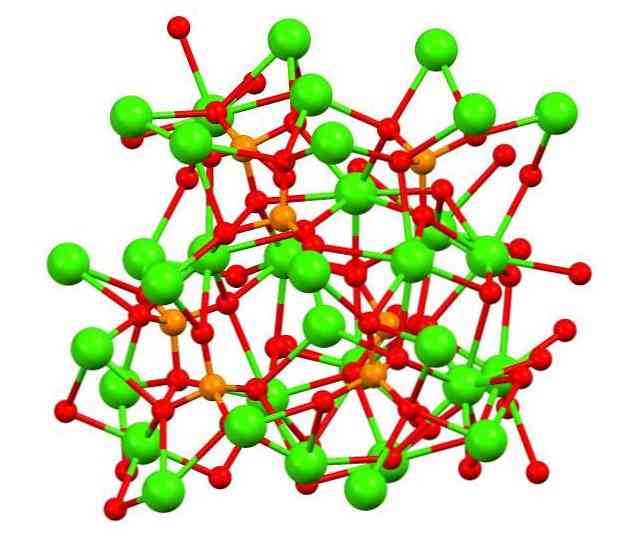
ภาพด้านบนแสดงให้เห็นถึงโครงสร้างของ tribasic calico phosphate ในแร่ whitlockite ที่แปลกซึ่งอาจมีแมกนีเซียมและเหล็กเป็นสารเจือปน.
แม้ว่าเมื่อดูแวบแรกมันอาจซับซ้อน แต่ก็จำเป็นต้องชี้แจงว่าแบบจำลองนั้นมีปฏิสัมพันธ์ระหว่างโควาเลนต์ระหว่างอะตอมออกซิเจนของฟอสเฟตและศูนย์กลางโลหะของแคลเซียม.
โดยวิธีการแสดงมันถูกต้อง แต่การโต้ตอบที่มีไฟฟ้าสถิต; นั่นคือแคทไอออน2+ จะดึงดูดไปที่แอนไอออน PO43- (Ca2+- O-PO33-) ด้วยสิ่งนี้ในใจจึงเป็นที่เข้าใจว่าทำไมในภาพแคลเซียม (ทรงกลมสีเขียว) ล้อมรอบด้วยอะตอมออกซิเจนที่มีประจุลบ (ทรงกลมสีแดง).
เมื่อมีไอออนจำนวนมากมันจะไม่ปล่อยให้มีการจัดเรียงแบบสมมาตรหรือรูปแบบที่มองเห็นได้ แคลิฟอร์เนีย3(PO4)2 Adopts ที่อุณหภูมิต่ำ (T<1000°C) una celda unitaria correspondiente a un sistema cristalino romboédrico; a este polimorfo se le conoce con el nombre de β-Ca3(PO4)2 (β-TCP สำหรับตัวย่อเป็นภาษาอังกฤษ).
ที่อุณหภูมิสูงในทางกลับกันก็จะถูกเปลี่ยนเป็น polymorph α-Ca3(PO4)2 (α-TCP) ซึ่งเซลล์หน่วยสอดคล้องกับระบบผลึกเดี่ยว ที่อุณหภูมิสูงขึ้น polymorph α'-Ca ยังสามารถเกิดขึ้นได้3(PO4)2, ซึ่งเป็นโครงสร้างผลึกหกเหลี่ยม.
แคลเซียมฟอสเฟตอสัณฐาน
โครงสร้างผลึกได้รับการกล่าวถึงสำหรับแคลเซียมฟอสเฟตซึ่งคาดว่าจะได้จากเกลือ อย่างไรก็ตามมันมีความสามารถในการแสดงโครงสร้างที่ไม่เป็นระเบียบและไม่สมมาตรเชื่อมโยงกับประเภทของ "แก้วแคลเซียมฟอสเฟต" มากกว่าผลึกในความหมายที่เข้มงวดของคำจำกัดความ.
เมื่อสิ่งนี้เกิดขึ้นมีการกล่าวกันว่าแคลเซียมฟอสเฟตมีโครงสร้างแบบอสัณฐาน (ACP), แคลเซียมฟอสเฟตอสัณฐาน) ผู้เขียนหลายคนชี้ไปที่โครงสร้างประเภทนี้ซึ่งมีความรับผิดชอบต่อคุณสมบัติทางชีวภาพของ Ca3(PO4)2 ในเนื้อเยื่อกระดูกการซ่อมแซมและการทำให้เป็นไบโอเมตริกเป็นไปได้.
ผ่านการอธิบายโครงสร้างโดยใช้สนามแม่เหล็กนิวเคลียร์ (NMR) พบว่ามีไอออน OH- และ HPO42- ใน ACP ไอออนเหล่านี้เกิดจากการไฮโดรไลซิสของหนึ่งในฟอสเฟต:
PO43- + H2O <=> HPO42- + OH-
เป็นผลให้โครงสร้างที่แท้จริงของ ACP มีความซับซ้อนมากขึ้นซึ่งองค์ประกอบของไอออนจะถูกแทนด้วยสูตร: Ca9(PO4)6 x(HPO4)x(OH)x. 'x' หมายถึงระดับความชุ่มชื้นเนื่องจากถ้า x = 1 สูตรจะเป็น: Ca9(PO4)5(HPO4) (OH).
โครงสร้างที่แตกต่างที่ PCA อาจขึ้นอยู่กับอัตราส่วน Ca / P ฟันกราม; นั่นคือจากปริมาณที่สัมพันธ์กันของแคลเซี่ยมและฟอสเฟตซึ่งเปลี่ยนองค์ประกอบที่เกิดขึ้นทั้งหมด.
ส่วนที่เหลือของครอบครัว
ในความเป็นจริงแล้วแคลเซียมฟอสเฟตเป็นตระกูลของสารประกอบอนินทรีย์ซึ่งสามารถโต้ตอบกับเมทริกซ์อินทรีย์ได้.
ฟอสเฟตอื่นจะได้รับ "เพียง" โดยการเปลี่ยนแอนไอออนที่มาพร้อมกับแคลเซียม (PO)43-, HPO42-, H2PO4-, OH-) เช่นเดียวกับประเภทของสิ่งสกปรกในของแข็ง ดังนั้นฟอสฟอรัสแคลเซียมมากถึงสิบเอ็ดหรือมากกว่านั้นแต่ละอย่างมีโครงสร้างและคุณสมบัติของตัวเองสามารถกำเนิดตามธรรมชาติหรือเทียม.
ด้านล่างนี้คือฟอสเฟตโครงสร้างโครงสร้างทางเคมี:
-แคลเซียมไฮโดรเจนฟอสเฟตไดไฮเดรต CaHPO4∙ 2H2O: monoclinic.
-แคลเซียม dihydrogen ฟอสเฟต monohydrate, Ca (H)2PO4)2∙ชั่วโมง2O: triclinic.
-รัสไดแอกฟอสเฟต, Ca (H)2PO4)2: triclinic.
-Ocalcium ไฮโดรเจนฟอสเฟต (OCP), Ca8H2(PO4)6: triclinic มันเป็นสารตั้งต้นในการสังเคราะห์ไฮดรอกซีอะพาไทต์.
-ไฮดรอกซีอะพาไทต์, แคลิฟอร์เนีย5(PO4)3OH: หกเหลี่ยม.
คุณสมบัติทางกายภาพและทางเคมี
ชื่อ
-แคลเซียมฟอสเฟต
-Tricalcium ฟอสเฟต
-Tricalcium Diphosphate
น้ำหนักโมเลกุล
310.74 g / mol.
คำอธิบายทางกายภาพ
มันเป็นของแข็งสีขาวไม่มีกลิ่น.
รสชาติ
รสจืด.
จุดหลอมเหลว
1670 ºK (1391 ºC).
สามารถในการละลาย
-ไม่ละลายในน้ำในทางปฏิบัติ.
-ไม่ละลายในเอทานอล.
-ละลายในกรดไฮโดรคลอริกเจือจางและกรดไนตริก.
ความหนาแน่น
3.14 g / cm3.
ดัชนีหักเห
1,629
มาตรฐานการฝึกอบรม
4126 kcal / mol.
อุณหภูมิการเก็บรักษา
2-8 ºC.
พีเอช
6-8 ในการระงับน้ำ 50 กรัม / ลิตรของแคลเซียมฟอสเฟต.
การอบรม
แคลเซียมไนเตรตและไฮโดรเจนแอมโมเนียมฟอสเฟต
มีหลายวิธีในการผลิตหรือสร้างแคลเซียมฟอสเฟต หนึ่งในนั้นประกอบด้วยเกลือสองชนิดคือ Ca (NO)3)2∙ 4H2ตและ (NH)4)2HPO4, ก่อนหน้านี้ละลายในแอลกอฮอล์และน้ำสัมบูรณ์ตามลำดับ หนึ่งเกลือให้แคลเซียมและฟอสเฟตอื่น ๆ.
จากส่วนผสมนี้ ACP จะตกตะกอนซึ่งจะถูกทำให้ร้อนในเตาอบที่ 800 ° C และเป็นเวลา 2 ชั่วโมง จากขั้นตอนนี้จะได้รับβ-Ca3(PO4)2. โดยการควบคุมอุณหภูมิเวลาการกวนและการสัมผัสอย่างระมัดระวังการเกิดผลึกนาโนสามารถเกิดขึ้นได้.
ในการสร้าง polymorph α-Ca3(PO4)2 จำเป็นต้องให้ความร้อนฟอสเฟตที่อุณหภูมิสูงกว่า 1,000 ° C การให้ความร้อนนี้เกิดขึ้นต่อหน้าไอออนโลหะอื่นซึ่งทำให้พอลิเมอร์นี้มีความเสถียรเพียงพอที่จะใช้ที่อุณหภูมิห้อง นั่นคือมันยังคงอยู่ในสถานะเมตาที่เสถียร.
แคลเซียมไฮดรอกไซด์และกรดฟอสฟอริก
แคลเซียมฟอสเฟตสามารถเกิดขึ้นได้โดยการผสมสารละลายแคลเซียมไฮดรอกไซด์และกรดฟอสฟอริกด้วยการทำให้เป็นกลางกรดเบสเกิดขึ้น หลังจากผ่านไปครึ่งวันของการสุกในเหล้าแม่และการกรองที่เหมาะสมการล้างการทำให้แห้งและการกรองเป็นผงละเอียดของฟอสฟอรัส amorphous ACP.
ACP ผลิตภัณฑ์ปฏิกิริยาของอุณหภูมิสูงเปลี่ยนตามสมการทางเคมีต่อไปนี้:
2ca9(HPO4) (PO4)5(OH) => 2Ca9(P2O7)0.5(PO4)5(OH) + H2O (ที่ T = 446.60 ° C)
2ca9(P2O7)0.5(PO4)5(OH) => 3Ca3(PO4)2 + 0.5H2O (ที่ T = 748.56 ° C)
ด้วยวิธีนี้ได้รับβ-Ca3(PO4)2, polymorph ที่พบมากที่สุดและมีเสถียรภาพ.
การใช้งาน
ในเนื้อเยื่อกระดูก
แคลิฟอร์เนีย3(PO4)2 มันเป็นองค์ประกอบหลักนินทรีย์ของเถ้ากระดูก มันเป็นองค์ประกอบของการปลูกถ่ายทดแทนกระดูกซึ่งถูกอธิบายโดยความคล้ายคลึงกันทางเคมีกับแร่ธาตุที่มีอยู่ในกระดูก.
วัสดุชีวภาพแคลเซียมฟอสเฟตใช้เพื่อแก้ไขข้อบกพร่องของกระดูกและในการเคลือบขาเทียมโลหะไทเทเนียม แคลเซียมฟอสเฟตถูกสะสมไว้แยกออกจากสิ่งแวดล้อมและชะลอกระบวนการกัดกร่อนของไทเทเนียม.
แคลเซียมฟอสเฟตรวมถึง Ca3(PO4)2, พวกเขาจะใช้สำหรับการผลิตวัสดุเซรามิก วัสดุเหล่านี้สามารถเข้ากันได้ทางชีวภาพและปัจจุบันถูกใช้เพื่อกู้คืนการสูญเสียกระดูกถุงซึ่งเป็นผลมาจากโรคปริทันต์การติดเชื้อในโพรงฟันและเงื่อนไขอื่น ๆ.
อย่างไรก็ตามควรใช้เพื่อเร่งการซ่อมแซมกระดูก periapical ในพื้นที่ที่ไม่มีการติดเชื้อแบคทีเรียเรื้อรัง.
แคลเซียมฟอสเฟตสามารถนำมาใช้ในการซ่อมแซมข้อบกพร่องของกระดูกเมื่อมันเป็นไปไม่ได้ที่จะใช้การปลูกถ่ายอวัยวะกระดูก autogenous มันเป็นไปได้ที่จะใช้มันเพียงอย่างเดียวหรือใช้ร่วมกับโพลิเมอร์ย่อยสลายได้และสลายได้เช่นกรดโพลีไกลโคลิก.
Bioceramic ซีเมนต์
แคลเซียมฟอสเฟตซีเมนต์ (CPC) เป็นสารชีวภาพชนิดหนึ่งที่ใช้ในการซ่อมแซมเนื้อเยื่อกระดูก มันทำโดยการผสมผงแคลเซียมฟอสเฟตชนิดต่าง ๆ กับน้ำไว้เป็นผง วางสามารถฉีดหรือปรับไปที่ข้อบกพร่องของกระดูกหรือช่อง.
ซีเมนต์ถูกหล่อหลอมแล้วค่อยๆดูดซับและแทนที่ด้วยกระดูกที่สร้างขึ้นใหม่.
ทางการแพทย์
-แคลิฟอร์เนีย3(PO4)2 มันเป็นเกลือพื้นฐานจึงใช้เป็นยาแก้ท้องเฟ้อเพื่อแก้กรดในกระเพาะอาหารส่วนเกินและเพิ่มค่า pH ในยาสีฟันนั้นจะให้แหล่งของแคลเซียมและฟอสเฟตเพื่อช่วยให้กระบวนการของการเกิดฟันและการแข็งตัวของเลือดในเลือดลดลง.
-มันยังใช้เป็นอาหารเสริมแม้ว่าวิธีที่ถูกที่สุดในการเปลี่ยนแคลเซียมก็คือการใช้คาร์บอเนตและซิเตรต.
-แคลเซียมฟอสเฟตสามารถใช้ในการรักษา tetany, hypocalcemia แฝงและการบำรุงรักษา นอกจากนี้ยังมีประโยชน์ในการเสริมแคลเซียมในระหว่างตั้งครรภ์และให้นมบุตร.
-มันถูกใช้ในการบำบัดการปนเปื้อนด้วยไอโซโทปกัมมันตรังสี (Ra-226) และสตรอนเทียม (Sr-90) แคลเซียมฟอสเฟตบล็อกการดูดซับของไอโซโทปกัมมันตรังสีในทางเดินอาหารจึงจำกัดความเสียหายที่เกิดจากพวกมัน.
คนอื่น ๆ
-แคลเซียมฟอสเฟตใช้เป็นอาหารสำหรับนก นอกจากนี้ยังใช้ในยาสีฟันเพื่อควบคุมเคลือบฟัน.
-มันถูกใช้เป็นสารป้องกันการเกิด caking ตัวอย่างเช่นเพื่อป้องกันการบีบอัดเกลือจากโต๊ะ.
-มันทำหน้าที่เป็นสารฟอกขาวสำหรับแป้ง ในขณะที่หมูหมูป้องกันไม่ให้สีที่ไม่พึงประสงค์และปรับปรุงสภาพของการทอด.
การอ้างอิง
- Tung M.S. (1998) แคลเซียมฟอสเฟต: โครงสร้างองค์ประกอบการละลายและความเสถียร ใน: Amjad Z. (eds) แคลเซียมฟอสเฟตในระบบชีวภาพและอุตสาหกรรม สปริงเกอร์บอสตันแมสซาชูเซตส์.
- Liu Lang, Yanzeng Wu, Chao Xu, Suchun Yu, Xiaopei Wu และ Honglian Dai (2018) "การสังเคราะห์, การศึกษาคุณสมบัติของนาโนฟอสฟอรัสและการยับยั้งเซลล์มะเร็งตับและเซลล์," วารสารของวัสดุนาโน, ฉบับที่. 2018, หมายเลขบทความ 7083416, 7 หน้า, 2018.
- ซี่โครง, คริสต์และเรย์, คริสเตียน (2010) Amorphous แคลเซียมฟอสเฟต: การสังเคราะห์คุณสมบัติและการใช้งานในวัสดุชีวภาพ Acta Biomaterialia, vol. 6 (n ° 9) PP 3362-3378 ISSN 1742-7061
- วิกิพีเดีย (2019) Tricalcium ฟอสเฟต สืบค้นจาก: en.wikipedia.org
- Abida และคณะ (2017) Tricalcium ฟอสเฟตผง: การเตรียมการศึกษาลักษณะและความสามารถในการบดอัด วารสารเคมีเมดิเตอร์เรเนียนปี 2017, 6 (3), 71-76.
- PubChem (2019) แคลเซียมฟอสเฟต สืบค้นจาก: pubchem.ncbi.nlm.nih.gov
- เอลส์ (2019) แคลเซียมฟอสเฟต วิทยาศาสตร์โดยตรง ดึงมาจาก: sciencedirect.com


