ขั้นตอนการแยกน้ำด้วยไฟฟ้า, เทคนิค, สิ่งที่เหมาะกับการทดลองในบ้าน
น้ำอิเล็กโทรไล เป็นการสลายตัวของน้ำเป็นส่วนประกอบพื้นฐานโดยการใช้กระแสไฟฟ้า เมื่อดำเนินการไฮโดรเจนและโมเลกุลออกซิเจนจะเกิดขึ้นบนพื้นผิวที่เฉื่อยสอง H2 และ O2. พื้นผิวทั้งสองนี้เป็นที่รู้จักกันดีในชื่อของขั้วไฟฟ้า.
ตามทฤษฎีแล้วปริมาตรของ H2 ที่เกิดขึ้นจะต้องเป็นสองเท่าของ O2. ทำไม? เนื่องจากโมเลกุลของน้ำมีอัตราส่วน H / O เท่ากับ 2 นั่นคือสอง H ต่อออกซิเจน ความสัมพันธ์นี้ถูกตรวจสอบโดยตรงด้วยสูตรทางเคมีของมัน H2O. อย่างไรก็ตามปัจจัยการทดลองจำนวนมากมีอิทธิพลต่อปริมาณที่ได้รับ.

หากอิเล็กโทรไลซิสถูกดำเนินการภายในหลอดที่จมอยู่ในน้ำ (ภาพบนสุด) คอลัมน์ของน้ำที่มีความสูงต่ำกว่าจะตรงกับไฮโดรเจนเนื่องจากมีก๊าซจำนวนมากที่ปล่อยก๊าซออกมากดดันบนพื้นผิวของของเหลว ฟองอากาศรอบขั้วไฟฟ้าและจบลงด้วยการเพิ่มขึ้นหลังจากแรงดันไอน้ำของน้ำหมดอายุ.
โปรดทราบว่าหลอดจะถูกแยกออกจากกันในลักษณะที่มีการโยกย้ายของก๊าซในระดับต่ำจากอิเล็กโทรดหนึ่งไปยังอีก ในระดับต่ำสิ่งนี้ไม่ได้แสดงถึงความเสี่ยงที่กำลังจะเกิดขึ้น แต่ในระดับอุตสาหกรรมส่วนผสมของก๊าซ H2 และ O2 มันมีอันตรายและระเบิดได้สูง.
ด้วยเหตุนี้เซลล์ไฟฟ้าเคมีที่ทำอิเล็กโทรไลต์น้ำจะมีราคาแพงมาก พวกเขาต้องการการออกแบบและองค์ประกอบที่รับประกันได้ว่าก๊าซไม่เคยผสมการจ่ายกระแสไฟฟ้าที่มีกำไรความเข้มข้นสูงของอิเล็กโทรไลต์อิเล็กโทรดพิเศษ (electrocatalysts) และกลไกในการจัดเก็บ H2 ผลิต.
Electrocatalyst เป็นตัวแทนของแรงเสียดทานและในเวลาเดียวกันปีกสำหรับการทำกำไรของอิเล็กโทรไลน้ำ บางส่วนประกอบด้วยออกไซด์ของโลหะมีตระกูลเช่นแพลตตินัมและอิริเดียมซึ่งมีราคาสูงมาก มันอยู่ที่จุดนี้โดยเฉพาะอย่างยิ่งที่นักวิจัยเข้าร่วมกองกำลังสำหรับการออกแบบขั้วไฟฟ้าที่มีประสิทธิภาพเสถียรและราคาถูก.
เหตุผลสำหรับความพยายามเหล่านี้คือเพื่อเร่งการก่อตัวของ O2, ซึ่งให้ที่ความเร็วต่ำเมื่อเทียบกับ H2. สิ่งนี้จะชะลอตัวลงโดยอิเล็กโทรดที่เกิดขึ้น O2 มันนำมาซึ่งผลที่ตามมาโดยทั่วไปคือการประยุกต์ใช้ศักยภาพที่มากเกินความจำเป็น เหมือนกันคืออะไรเพื่อลดประสิทธิภาพและค่าใช้จ่ายที่สูงขึ้น.
ดัชนี
- 1 ปฏิกิริยาของกระแสไฟฟ้า
- 1.1 ปฏิกิริยาครึ่งเซลล์
- 2 ขั้นตอน
- 3 เทคนิค
- 3.1 กระแสไฟฟ้าด้วยน้ำอัลคาไลน์
- 3.2 กระแสไฟฟ้าด้วยเมมเบรนอิเล็กโทรไลต์
- 3.3 อิเล็กโทรไลซิสกับออกไซด์ที่เป็นของแข็ง
- 4 การใช้กระแสไฟฟ้าในน้ำคืออะไร??
- 4.1 การผลิตไฮโดรเจนและการใช้ประโยชน์
- 4.2 เป็นวิธีการแก้จุดบกพร่อง
- 4.3 ในฐานะที่เป็นออกซิเจน
- 5 การทดลองในบ้าน
- 5.1 ตัวแปรบ้าน
- 6 อ้างอิง
ปฏิกิริยาอิเล็กโทรไล
กระแสไฟฟ้าของน้ำเกี่ยวข้องกับลักษณะที่ซับซ้อนมากมาย อย่างไรก็ตามในแง่ทั่วไปพื้นฐานของมันอยู่ในปฏิกิริยาระดับโลกที่เรียบง่าย:
2H2O (l) => 2H2(g) + O2(G)
ตามที่สังเกตในสมการโมเลกุลของน้ำสองโมเลกุลจะเข้ามา: โดยปกติจะต้องลดลงหรือได้รับอิเล็กตรอนในขณะที่อีกอันจะต้องออกซิไดซ์หรือสูญเสียอิเล็กตรอน.
The H2 มันเป็นผลมาจากการลดน้ำเพราะการได้รับอิเล็กตรอนจะส่งเสริมโปรตอน H+ สามารถถูกพันธะโควาเลนต์และออกซิเจนเปลี่ยนเป็น OH-. ดังนั้นทาง2 เกิดขึ้นที่ขั้วลบซึ่งเป็นขั้วไฟฟ้าที่เกิดการลดลง.
ในขณะที่ O2 มาจากการออกซิเดชันของน้ำเพราะสูญเสียอิเล็กตรอนที่ทำให้มันจับกับไฮโดรเจนและจึงปล่อยโปรตอน H+. ต2 เกิดขึ้นที่ขั้วบวกอิเล็กโทรดที่เกิดออกซิเดชัน; และแตกต่างจากอิเล็กโทรดอื่น ๆ ค่า pH รอบ ๆ ขั้วบวกนั้นเป็นกรดและไม่เป็นพื้นฐาน.
ปฏิกิริยาครึ่งเซลล์
สามารถสรุปได้ด้วยสมการทางเคมีต่อไปนี้สำหรับปฏิกิริยาครึ่งเซลล์:
2H2O + 2e- => H2 + 2OH- (แคโทดพื้นฐาน)
2H2O => O2 + 4H+ + 4e- (ขั้วบวก, กรด)
อย่างไรก็ตามน้ำไม่สามารถสูญเสียอิเล็กตรอนได้มากขึ้น (4e-) ซึ่งโมเลกุลของน้ำอื่น ๆ ชนะที่แคโทด (2e-); ดังนั้นสมการแรกจะต้องคูณด้วย 2 แล้วจึงลบด้วยสมการที่สองเพื่อให้ได้สมการสุทธิ:
2 (2H2O + 2e- => H2 + 2OH-)
2H2O => O2 + 4H+ + 4e-
6H2O => 2H2 + O2 + 4H+ + 4OH-
แต่ 4H+ และ 4OH- พวกเขาเป็น 4H2หรือดังนั้นกำจัดสี่ H หกโมเลกุล2หรือปล่อยให้สอง และผลลัพธ์ก็คือปฏิกิริยาระดับโลกที่เพิ่งเกิดขึ้น.
ปฏิกิริยาครึ่งเซลล์จะเปลี่ยนไปตามค่า pH เทคนิคและยังมีศักยภาพในการลดหรือเกิดออกซิเดชันซึ่งกำหนดจำนวนกระแสไฟฟ้าที่จะต้องจัดหาเพื่อให้อิเล็กโทรไลซิสของน้ำเกิดขึ้นเองตามธรรมชาติ.
กระบวนการ
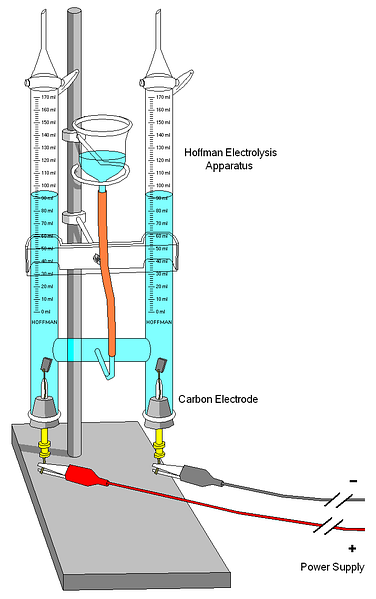
ภาพด้านบนแสดงโวลต์มิเตอร์ Hoffman ไส้กุญแจจะเต็มไปด้วยน้ำและอิเล็กโทรไลต์ที่เลือกผ่านหัวฉีดตรงกลาง บทบาทของอิเล็กโทรไลต์เหล่านี้คือการเพิ่มการนำไฟฟ้าของน้ำเนื่องจากภายใต้สภาวะปกติมีไอออน H น้อยมาก3O+ และโอ้- ผลิตภัณฑ์ไอออนไนซ์อัตโนมัติของคุณ.
อิเล็กโทรดทั้งสองมักเป็นแพลทตินัมแม้ว่าในภาพจะถูกแทนที่ด้วยอิเล็กโทรดคาร์บอน ทั้งสองเชื่อมต่อกับแบตเตอรี่ซึ่งมีความต่างศักย์ (ΔV) ที่ส่งเสริมการเกิดออกซิเดชันของน้ำ (การก่อ O)2).
อิเล็กตรอนเคลื่อนที่ไปทั่วทั้งวงจรจนกว่าคุณจะไปถึงอิเล็กโทรดอื่นที่ซึ่งน้ำชนะและกลายเป็น H2 และโอ้-. ณ จุดนี้ขั้วบวกและขั้วลบจะถูกกำหนดไว้แล้วซึ่งสามารถแยกความแตกต่างโดยความสูงของคอลัมน์น้ำ; หนึ่งในความสูงที่เล็กลงสอดคล้องกับแคโทดที่ H ถูกสร้างขึ้น2.
ในส่วนบนของกระบอกสูบมีปุ่มบางอย่างที่อนุญาตให้ปล่อยก๊าซที่สร้างขึ้น คุณสามารถตรวจสอบอย่างรอบคอบสถานะของ H2 ทำให้ปฏิกิริยากับเปลวไฟซึ่งการเผาไหม้ผลิตน้ำก๊าซ.
เทคนิค
เทคนิคการแยกด้วยน้ำจะแตกต่างกันไปตามปริมาณของ H2 และ O2 ที่เสนอให้สร้าง ก๊าซทั้งสองนั้นมีอันตรายมากถ้ามันถูกผสมเข้าด้วยกันและนั่นคือสาเหตุที่เซลล์อิเล็กโทรไลต์มีการออกแบบที่ซับซ้อนเพื่อลดแรงกดดันของก๊าซและการแพร่กระจายของมันผ่านตัวกลางที่เป็นน้ำ.
นอกจากนี้เทคนิคการสั่นขึ้นอยู่กับเซลล์อิเล็กโทรไลต์ที่เติมลงไปในน้ำและขั้วไฟฟ้าของตัวเอง ในทางตรงกันข้ามบางคนบอกว่าปฏิกิริยาเกิดขึ้นที่อุณหภูมิสูงขึ้นลดการใช้ไฟฟ้าและอื่น ๆ ใช้แรงกดดันมหาศาลในการรักษา H2 เก็บไว้.
ในบรรดาเทคนิคต่าง ๆ สามารถกล่าวถึงสามสิ่งต่อไปนี้:
กระแสไฟฟ้าด้วยน้ำอัลคาไลน์
กระบวนการอิเล็กโทรไลซิสจะดำเนินการด้วยการแก้ปัญหาพื้นฐานของโลหะอัลคาไล ด้วยเทคนิคนี้ปฏิกิริยาเกิดขึ้น:
4H2O (l) + 4e- => 2H2(g) + 4OH-(Aq)
4OH-(ac) => O2(g) + 2H2O (l) + 4e-
ดังที่เห็นได้ทั้งที่แคโทดและแอโนดน้ำมีค่า pH พื้นฐาน และนอกจากนี้ OH- โยกย้ายไปยังขั้วบวกที่พวกเขาออกซิไดซ์ไปที่ O2.
กระแสไฟฟ้าด้วยเมมเบรนอิเล็กโทรไลต์
ในเทคนิคนี้ใช้โพลีเมอร์แข็งที่ทำหน้าที่เป็นเมมเบรนซึมผ่านได้สำหรับ H+, แต่กันน้ำสำหรับก๊าซ สิ่งนี้รับประกันความปลอดภัยที่มากขึ้นในช่วงกระแสไฟฟ้า.
ปฏิกิริยาครึ่งเซลล์สำหรับกรณีนี้คือ:
4H+(ac) + 4e- => 2H2(G)
2H2O (l) => O2(g) + 4H+(ac) + 4e-
ไอออน H+ พวกเขาย้ายจากขั้วบวกไปยังแคโทดที่พวกเขาจะกลายเป็นเอช2.
อิเล็กโทรไลซิสกับออกไซด์ที่เป็นของแข็ง
แตกต่างจากเทคนิคอื่น ๆ โดยใช้ออกไซด์เป็นอิเล็กโทรไลต์ที่อุณหภูมิสูง (600-900ºC) ทำหน้าที่เป็นสื่อกลางในการขนส่งไอออน2-.
ปฏิกิริยาคือ:
2H2O (g) + 4e- => 2H2(g) + 2O2-
2O2- => O2(g) + 4e-
โปรดทราบว่าเวลานี้คือออกไซด์แอนไอออน2-, ผู้ที่เดินทางไปยังขั้วบวก.
การใช้น้ำไฟฟ้าคืออะไร?
การแยกน้ำด้วยไฟฟ้าทำให้เกิดเอช2 (g) และ O2 (G) ประมาณ 5% ของก๊าซไฮโดรเจนที่ผลิตในโลกนั้นผลิตขึ้นด้วยกระแสไฟฟ้าของน้ำ.
The H2 มันเป็นผลพลอยได้จากกระแสไฟฟ้าของสารละลาย NaCl ที่เป็นน้ำ การมีอยู่ของเกลือช่วยให้อิเล็กโตรไลซิสโดยการเพิ่มการนำไฟฟ้าของน้ำ.
ปฏิกิริยาระดับโลกที่เกิดขึ้นคือ:
2NaCl + 2H2O => Cl2 + H2 + 2 NaOH
เพื่อให้เข้าใจถึงความสำคัญอย่างยิ่งของปฏิกิริยานี้จะมีการกล่าวถึงการใช้งานผลิตภัณฑ์ก๊าซบางอย่าง; เพราะในตอนท้ายของวันเหล่านี้เป็นคนที่ผลักดันการพัฒนาวิธีการใหม่เพื่อให้ได้น้ำอิเล็กโทรไลในวิธีที่มีประสิทธิภาพและเป็นสีเขียว.
ในบรรดาทั้งหมดนั้นสิ่งที่ต้องการมากที่สุดคือทำหน้าที่เป็นเซลล์ที่มีพลังแทนที่การใช้เชื้อเพลิงฟอสซิลที่เผาไหม้.
การผลิตไฮโดรเจนและการใช้ประโยชน์
-ไฮโดรเจนที่ผลิตในอิเล็กโทรไลซิสสามารถใช้ในอุตสาหกรรมเคมีที่ทำหน้าที่ในปฏิกิริยาการติดในกระบวนการไฮโดรจิเนชันหรือเป็นตัวรีดิวซ์ในกระบวนการลด.
-นอกจากนี้มันเป็นสิ่งสำคัญในการกระทำบางอย่างที่มีความสำคัญในเชิงพาณิชย์เช่น: การผลิตกรดไฮโดรคลอริก, ไฮโดรเจนเปอร์ออกไซด์, ไฮดรอกซิลามีน ฯลฯ เกี่ยวข้องกับการสังเคราะห์แอมโมเนียโดยปฏิกิริยาเร่งปฏิกิริยากับไนโตรเจน.
-เมื่อรวมกับออกซิเจนจะทำให้เกิดเปลวไฟที่มีปริมาณแคลอรี่สูงโดยมีอุณหภูมิอยู่ระหว่าง 3,000 ถึง 3,500 K อุณหภูมิเหล่านี้สามารถใช้สำหรับการตัดและเชื่อมในอุตสาหกรรมโลหะเพื่อการเจริญเติบโตของผลึกสังเคราะห์การผลิตควอตซ์เป็นต้น.
-การบำบัดน้ำ: ปริมาณไนเตรตที่สูงเกินไปในน้ำสามารถลดลงได้โดยการกำจัดในเครื่องปฏิกรณ์ชีวภาพซึ่งแบคทีเรียใช้ไฮโดรเจนเป็นแหล่งพลังงาน
-ไฮโดรเจนเข้าแทรกแซงในการสังเคราะห์พลาสติกโพลีเอสเตอร์และไนลอน นอกจากนี้ยังเป็นส่วนหนึ่งของการผลิตแก้วเพิ่มการเผาไหม้ในระหว่างการอบ.
-ทำปฏิกิริยากับออกไซด์และคลอไรด์ของโลหะจำนวนมากในหมู่พวกเขา: เงิน, ทองแดง, ตะกั่ว, บิสมัทและปรอทเพื่อผลิตโลหะบริสุทธิ์.
-นอกจากนี้ยังใช้เป็นเชื้อเพลิงในการวิเคราะห์ด้วยเครื่องตรวจจับเปลวไฟ.
เป็นวิธีการแก้จุดบกพร่อง
อิเล็กโทรไลซิสของสารละลายโซเดียมคลอไรด์ใช้สำหรับการทำให้บริสุทธิ์ของน้ำในสระว่ายน้ำ ในช่วงกระแสไฟฟ้าไฮโดรเจนจะถูกผลิตขึ้นในแคโทดและคลอรีน (Cl2) ที่ขั้วบวก มีการพูดถึงอิเล็กโทรไลซิสในกรณีนี้ในฐานะที่เป็นเกลือคลอรีน.
คลอรีนละลายในน้ำก่อให้เกิดกรดไฮโปคลอรัสและโซเดียมไฮโปคลอไรต์ กรดไฮโปคลอรัสและโซเดียมไฮโปคลอไรต์ฆ่าเชื้อในน้ำ.
เป็นแหล่งออกซิเจน
กระแสไฟฟ้าของน้ำยังใช้ในการสร้างออกซิเจนในสถานีอวกาศนานาชาติซึ่งทำหน้าที่รักษาบรรยากาศของออกซิเจนในสถานี.
ไฮโดรเจนสามารถนำมาใช้ในเซลล์เชื้อเพลิงวิธีการเก็บพลังงานและใช้น้ำที่สร้างขึ้นในเซลล์เพื่อการบริโภคโดยนักบินอวกาศ.
การทดลองหน้าแรก
การทดลองด้วยกระแสไฟฟ้าของน้ำได้ดำเนินการที่เครื่องชั่งในห้องปฏิบัติการด้วยโวลต์มิเตอร์ Hoffman หรือชุดประกอบอื่น ๆ ที่ช่วยให้มีองค์ประกอบที่จำเป็นทั้งหมดของเซลล์ไฟฟ้าเคมี.
ในการประกอบและอุปกรณ์ที่เป็นไปได้ทั้งหมดสิ่งที่ง่ายที่สุดคือภาชนะบรรจุน้ำโปร่งใสขนาดใหญ่ นอกจากนี้คุณควรมีโลหะหรือพื้นผิวที่เป็นตัวนำไฟฟ้าเพื่อใช้เป็นขั้วไฟฟ้า หนึ่งสำหรับแคโทดและอื่น ๆ สำหรับขั้วบวก.
เพื่อจุดประสงค์นี้แม้กระทั่งดินสอที่มีจุดกราไฟท์ที่ปลายทั้งสองข้างอาจมีประโยชน์ และในที่สุดแบตเตอรี่ขนาดเล็กและสายเคเบิลบางอย่างที่เชื่อมต่อกับขั้วไฟฟ้าชั่วคราว.
หากไม่ได้ทำในภาชนะใสการก่อตัวของฟองก๊าซจะไม่ได้รับการชื่นชม.
ตัวแปรบ้าน
แม้ว่ากระแสไฟฟ้าของน้ำเป็นเรื่องที่มีแง่มุมที่น่าสนใจและมีความหวังมากมายสำหรับผู้ที่แสวงหาแหล่งพลังงานทางเลือก แต่การทดลองใช้ในบ้านอาจทำให้เด็ก ๆ และผู้ชมอื่น ๆ เบื่อหน่าย.
ดังนั้นสามารถใช้แรงดันไฟฟ้าที่เพียงพอในการสร้าง H2 และ O2 สลับตัวแปรบางอย่างและสังเกตการเปลี่ยนแปลง.
สิ่งแรกคือการเปลี่ยนแปลงของ pH ของน้ำโดยใช้น้ำส้มสายชูเพื่อทำให้เป็นกรดน้ำหรือนา2CO3 เพื่ออ้างอิงมันเล็กน้อย การเปลี่ยนแปลงปริมาณฟองอากาศที่สังเกตต้องเกิดขึ้น.
นอกจากนี้การทดสอบเดียวกันสามารถทำซ้ำได้ด้วยน้ำเย็นและน้ำร้อน ด้วยวิธีนี้ผลกระทบของอุณหภูมิที่มีต่อปฏิกิริยาจะถูกไตร่ตรองไว้.
สุดท้ายเพื่อให้การเก็บข้อมูลไม่มีสีน้อยลงคุณสามารถหันไปใช้สารละลายน้ำกะหล่ำปลีสีม่วงเจือจางมาก น้ำผลไม้นี้เป็นตัวบ่งชี้กรดเบสของแหล่งกำเนิดตามธรรมชาติ.
การเพิ่มลงในคอนเทนเนอร์ด้วยอิเล็กโทรดที่แนะนำนั้นจะสังเกตได้ว่าที่ขั้วบวกน้ำจะเปลี่ยนเป็นสีชมพู (กรด) ในขณะที่แคโทดสีจะเป็นสีเหลือง (พื้นฐาน).
การอ้างอิง
- วิกิพีเดีย (2018) กระแสไฟฟ้าของน้ำ สืบค้นจาก: en.wikipedia.org
- แชปลินเอ็ม (16 พฤศจิกายน 2018) กระแสไฟฟ้าของน้ำ โครงสร้างของน้ำและวิทยาศาสตร์ ดึงจาก: 1.lsbu.ac.uk
- ประสิทธิภาพการใช้พลังงานและพลังงานทดแทน ( N.d. ) การผลิตไฮโดรเจน: กระแสไฟฟ้า ดึงมาจาก: energy.gov
- Phys.org (14 กุมภาพันธ์ 2018) ตัวเร่งปฏิกิริยาที่มีประสิทธิภาพสูงและต้นทุนต่ำสำหรับการแยกน้ำ สืบค้นจาก: phys.org
- เคมีเคมี (18 มิถุนายน 2558) กระแสไฟฟ้าของน้ำ ดึงมาจาก: chem.libretexts.org
- Xiang C. , M. Papadantonakisab K. และ S. Lewis N. (2016) หลักการและการใช้งานระบบอิเล็กโทรไลซิสสำหรับการแยกน้ำ ราชสมาคมเคมี.
- ผู้สำเร็จราชการแห่งมหาวิทยาลัยมินนิโซตา (2018) กระแสไฟฟ้าของน้ำ 2 มหาวิทยาลัยมินนิโซตา ดึงมาจาก: chem.umn.edu


