คุณสมบัติไฮโดรเจนซัลไฟด์ (H2S) ความเสี่ยงและการใช้ประโยชน์
ไฮโดรเจนซัลไฟด์ เป็นชื่อสามัญของไฮโดรเจนซัลไฟด์ (H2S) มันถือได้ว่าเป็นกรดไฮดราไซด์ในสารละลาย (H2S (aq)).
การพิจารณาของกรดซัลคาไรด์จะได้รับทั้งๆที่ความสามารถในการละลายต่ำในน้ำของสารเคมีนี้ โครงสร้างของมันถูกนำเสนอในรูปที่ 1 (EMBL-EBI, 2005).
ดังนั้นไฮโดรเจนซัลไฟด์จึงละลายได้ในน้ำเล็กน้อย เมื่อละลายจะเกิดเป็นกรดซัลไฟด์ไอออนหรือไฮโดรซัลไฟด์ (HS)-) สารละลายน้ำของไฮโดรเจนซัลไฟด์หรือไฮโดรเจนซัลไฟด์ไม่มีสีและเมื่อสัมผัสกับอากาศค่อย ๆ ออกซิไดซ์ธาตุกำมะถันซึ่งไม่ละลายในน้ำ.
กำมะถัน dianion S.2- มันมีอยู่ในสารละลายที่เป็นด่างอย่างยิ่งเท่านั้น เป็นพื้นฐานที่ยอดเยี่ยมด้วย pKa> 14.
The H2S เกิดขึ้นจากการที่กำมะถันธาตุสัมผัสกับสารอินทรีย์โดยเฉพาะที่อุณหภูมิสูง ไฮโดรเจนซัลไฟด์เป็นโควาเลนต์ไฮไดรด์ที่เกี่ยวข้องทางเคมีกับน้ำ (H2O) เนื่องจากออกซิเจนและซัลเฟอร์ผลิตในกลุ่มเดียวกันกับตารางธาตุ.
มันมักจะส่งผลให้แบคทีเรียทำลายสารอินทรีย์ในกรณีที่ไม่มีออกซิเจนเช่นในหนองน้ำและท่อระบายน้ำทิ้ง (รวมถึงกระบวนการย่อยสลายแบบไม่ใช้ออกซิเจน) นอกจากนี้ยังเกิดขึ้นในก๊าซภูเขาไฟก๊าซธรรมชาติและน้ำบางแห่ง.
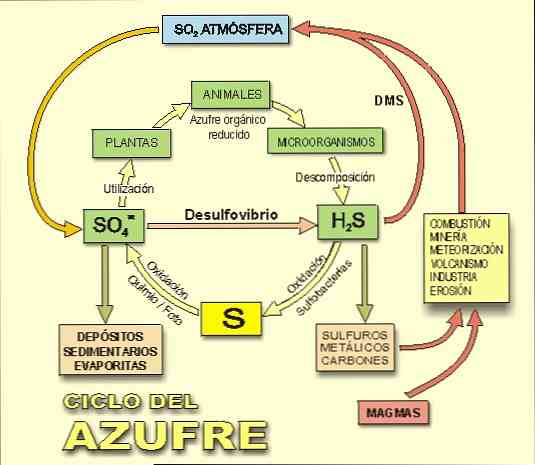
สิ่งสำคัญคือต้องคำนึงว่าไฮโดรเจนซัลไฟด์เป็นผู้มีส่วนร่วมในวัฏจักรกำมะถันซึ่งเป็นวัฏจักรทางชีวเคมีของกำมะถันบนโลก (รูปที่ 2).
ดังที่ได้กล่าวมาแล้วแบคทีเรียที่ลดซัลเฟอร์และซัลเฟตได้รับพลังงานออกซิเดชันจากไฮโดรเจนหรือโมเลกุลอินทรีย์ในกรณีที่ไม่มีออกซิเจนโดยการลดซัลเฟอร์หรือซัลเฟตเป็นไฮโดรเจนซัลไฟด์.
แบคทีเรียอื่น ๆ ปล่อยไฮโดรเจนซัลไฟด์จากกรดอะมิโนที่มีซัลเฟอร์ แบคทีเรียหลายกลุ่มสามารถใช้ไฮโดรเจนซัลไฟด์เป็นเชื้อเพลิงออกซิไดซ์กับธาตุกำมะถันหรือซัลเฟตโดยใช้ออกซิเจนหรือไนเตรตเป็นสารออกซิแดนท์.
แบคทีเรียกำมะถันบริสุทธิ์และแบคทีเรียสีเขียวกำมะถันใช้ไฮโดรเจนซัลไฟด์เป็นผู้บริจาคอิเล็กตรอนในการสังเคราะห์ด้วยแสงจึงผลิตธาตุกำมะถัน.
อันที่จริงแล้วการสังเคราะห์ด้วยแสงโหมดนี้มีอายุมากกว่าโหมดของไซยาโนแบคทีเรียแบคทีเรียสาหร่ายและพืชที่ใช้น้ำเป็นผู้บริจาคอิเล็กตรอนและปล่อยออกซิเจน (Human Metabolome Database, 2017).
ดัชนี
- 1 ในกรณีที่ผลิตไฮโดรเจนซัลไฟด์?
- 2 คุณสมบัติทางกายภาพและทางเคมี
- 3 ปฏิกิริยาและอันตราย
- 3.1 การสูดดม
- 3.2 การสัมผัสทางผิวหนัง
- 3.3 สัมผัสกับตา
- 4 ใช้
- 4.1 1- การผลิตกำมะถัน
- 4.2 2- เคมีวิเคราะห์
- 4.3 3- การใช้งานอื่น ๆ
สถานที่ผลิตไฮโดรเจนซัลไฟด์?
ไฮโดรเจนซัลไฟด์ (H2S) เกิดขึ้นตามธรรมชาติในน้ำมันดิบก๊าซธรรมชาติก๊าซภูเขาไฟและน้ำพุร้อน นอกจากนี้ยังสามารถเป็นผลมาจากการย่อยสลายแบคทีเรียของสารอินทรีย์ มันถูกผลิตโดยของเสียจากมนุษย์และสัตว์.
แบคทีเรียที่พบในปากและทางเดินอาหารผลิตไฮโดรเจนซัลไฟด์จากแบคทีเรียที่สลายวัสดุที่มีโปรตีนจากพืชหรือสัตว์.
ไฮโดรเจนซัลไฟด์อาจเป็นผลมาจากกิจกรรมอุตสาหกรรมเช่นการแปรรูปอาหารโค้กโอเวนโรงงานกระดาษคราฟท์โรงฟอกหนังและโรงกลั่นปิโตรเลียม (หน่วยงานสำหรับสารพิษและรีจิสตรีโรค 2011).
คุณสมบัติทางกายภาพและทางเคมี
ไฮโดรเจนซัลไฟด์เป็นก๊าซไม่มีสีมีกลิ่นรุนแรงของไข่เน่า สารละลายไฮโดรเจนซัลไฟด์ไม่มีสีโดยไม่มีกลิ่น.
สารประกอบนี้มีน้ำหนักโมเลกุล 34.1 g / mol สารละลายในน้ำมีความหนาแน่น 1.343 g / ml มันมีจุดหลอมเหลวที่ -82 ° C และจุดเดือดที่ -60 ° C มันละลายได้ในน้ำเล็กน้อยสามารถละลายได้เพียง 4 กรัมต่อลิตรของตัวทำละลายนี้ที่ 20 ° C (Royal Society of Chemistry, 2015).
ไฮโดรเจนซัลไฟด์ทำปฏิกิริยาเป็นกรดและเป็นตัวรีดิวซ์ มันระเบิดเมื่อสัมผัสกับออกซิเจน difluoride, bromine pentafluoride, คลอรีน trifluoride, dichloride ออกไซด์และ fulminate เงิน มันสามารถจุดชนวนและระเบิดเมื่อสัมผัสกับผงทองแดงในที่ที่มีออกซิเจน.
โดยสามารถตอบสนองในทำนองเดียวกันกับผงโลหะอื่น ๆ มันจี้ใจดำเมื่อสัมผัสกับโลหะออกไซด์และเปอร์ออกไซด์ (แบเรียมเปอร์ออกไซด์โครเมียมออกไซด์ทองแดงออกไซด์ก๊าซตะกั่วแมงกานีสไดออกไซด์นิกเกิลออกไซด์, เงินออกไซด์ก๊าซเงินแทลเลียมออกไซด์โซเดียมเปอร์ออกไซด์ เมอร์คิวออกไซด์, แคลเซียมออกไซด์).
มันถูกจุดติดด้วยซิลเวอร์โบรเมต, ตะกั่ว (II) ไฮโปคลอไรต์, ทองแดงโครเมต, กรดไนตริก, ตะกั่วออกไซด์ (IV) และออกไซด์ มันสามารถจุดไฟได้ถ้าผ่านท่อเหล็กที่เป็นสนิม ทำปฏิกิริยากับฐานความร้อน.
ความร้อนของการเกิดปฏิกิริยากับมะนาวโซดาโซเดียมไฮดรอกไซโพแทสเซียมไฮดรอกไซแบเรียมไฮดรอกไซอาจทำให้เกิดการเผาไหม้หรือการระเบิดของส่วน unreacted ในการปรากฏตัวของอากาศ / ออกซิเจน (ก๊าซไข่เน่า 2016).
ปฏิกิริยาและอันตราย
The H2S ถือเป็นสารประกอบที่มีความเสถียรแม้ว่าจะมีความไวไฟสูงและเป็นพิษอย่างยิ่ง.
สารประกอบนั้นหนักกว่าอากาศและสามารถเดินทางไกลไปยังแหล่งกำเนิดประกายไฟและสำรองได้ สามารถก่อให้เกิดของผสมที่ระเบิดได้กับอากาศในช่วงกว้าง.
มันยังทำปฏิกิริยาระเบิดกับโบรมีนเพนตาฟลูออไรด์, คลอรีนไตรฟลูออไรด์, ไนโตรเจนไตรโอไดด์, ไนโตรเจนไตรคลอไรด์, ออกซิเจนดิฟลูออไรด์และฟีนิลไดเซียมคลอไรด์.
เมื่อถูกความร้อนจะสลายตัวก็ปล่อยควันพิษสูงของซัลเฟอร์ออกไซด์ เข้ากันไม่ได้กับวัสดุหลายชนิดรวมทั้งสารโลหะกรดไนตริกแข็งแรงโบรมีน pentafluoride คลอรีน trifluoride, ไตรไอโอไนโตรเจนไนโตรเจนไตรคลอไรด์, difluoride ออกซิเจนและฟีนิลคลอไรด์ไดอะโซเนียม.
ไฮโดรเจนซัลไฟด์ (H2S) รับผิดชอบต่อเหตุการณ์ที่เกิดพิษจากการทำงานโดยเฉพาะอย่างยิ่งในอุตสาหกรรมน้ำมัน ผลทางคลินิกของเอช2S ขึ้นอยู่กับความเข้มข้นและระยะเวลาของการเปิดรับแสง.
The H2S เป็นอันตรายถึงชีวิตได้ทันทีเมื่อมีความเข้มข้นมากกว่า 500-1000 ส่วนต่อล้านส่วน (ppm) แต่การสัมผัสกับที่ลดลงเป็น 10-500 ppm ความเข้มข้นอาจทำให้เกิดอาการทางเดินหายใจต่างๆตั้งแต่โรคจมูกอักเสบจากความล้มเหลวทางเดินหายใจเฉียบพลัน.
The H2S ยังสามารถส่งผลกระทบต่อหลายอวัยวะทำให้เกิดความผิดปกติชั่วคราวหรือถาวรในระบบประสาท, หัวใจและหลอดเลือด, ไต, ตับและระบบโลหิต.
กรณีของการสัมผัสกับ H จะถูกนำเสนอ2S ที่นำไปสู่การมีส่วนร่วมของหลายอวัยวะ, การหายใจล้มเหลวเฉียบพลัน, การจัดระเบียบของโรคปอดบวมและการช็อกคล้ายกับการติดเชื้อเฉียบพลัน ในกรณีนี้ผู้ป่วยยังพัฒนาโรคปอดอุดกั้นและ จำกัด อย่างอ่อนโยนและเส้นประสาทส่วนปลาย (Al-Tawfiq, 2010).
การสูด
ในกรณีที่สูดหายใจเข้าไปให้นำออกไปข้างนอกแล้วพักผ่อนในท่าที่สบายเพื่อหายใจ ถ้าไม่หายใจให้ทำการช่วยหายใจ หากหายใจลำบากบุคลากรที่ผ่านการฝึกอบรมควรให้ออกซิเจน.
การสัมผัสทางผิวหนัง
ในกรณีที่สัมผัสกับผิวหนังควรล้างด้วยน้ำปริมาณมาก ของเหลวที่มีความดันสามารถทำให้เกิดอาการบวมเป็นน้ำเหลือง ในกรณีที่สัมผัสกับของเหลวที่มีความดันควรแช่แข็งในโซนแช่แข็งทันทีด้วยน้ำอุ่นไม่เกิน 41 ° C.
อุณหภูมิของน้ำจะต้องทนได้กับผิวปกติ ควรอุ่นเครื่องของผิวหนังเป็นเวลาอย่างน้อย 15 นาทีหรือจนกว่าสีและความรู้สึกปกติจะกลับสู่บริเวณที่ได้รับผลกระทบ ในกรณีของการสัมผัสขนาดใหญ่เสื้อผ้าจะถูกลบออกในขณะที่อาบน้ำด้วยน้ำอุ่น.
สัมผัสกับตา
ในกรณีที่สัมผัสกับดวงตาให้ล้างตาด้วยน้ำสะอาดอย่างน้อย 15 นาที ให้เปลือกตาเปิดและอยู่ห่างจากลูกตาเพื่อให้แน่ใจว่าพื้นผิวทั้งหมดล้างอย่างทั่วถึง.
การกลืนกินจะไม่ถือเป็นเส้นทางการสัมผัสที่เป็นไปได้ สำหรับกรณีอื่น ๆ ต้องได้รับการรักษาพยาบาลทันที (Praxair, 2016).
การใช้งาน
1- การผลิตกำมะถัน
กู้คืนหน่วยซานตาคลอสกำมะถันประกอบด้วยการเผาไหม้เตาหม้อไอน้ำความร้อนเหลือทิ้งเป็นกำมะถันคอนเดนเซอร์และจำนวนของขั้นตอนการเร่งปฏิกิริยาของแต่ละคนที่ใช้อุ่น, เตียงตัวเร่งปฏิกิริยาและกำมะถันคอนเดนเซอร์ โดยปกติแล้วสองหรือสามขั้นตอนมีการใช้ตัวเร่งปฏิกิริยา.
กระบวนการของคลอสเปลี่ยนไฮโดรเจนซัลไฟด์เป็นธาตุกำมะถันผ่านปฏิกิริยาสองขั้นตอน.
ขั้นตอนแรกเกี่ยวข้องกับการเผาไหม้ควบคุมของอาหารสัตว์เพื่อแปลงไฮโดรเจนซัลไฟด์ประมาณหนึ่งในสามเป็นก๊าซซัลเฟอร์ไดออกไซด์และปฏิกิริยาที่ไม่เป็นตัวเร่งปฏิกิริยาของไฮโดรเจนซัลไฟด์ที่ไม่เผาด้วยก๊าซซัลเฟอร์ไดออกไซด์.
ในขั้นตอนที่สองปฏิกิริยาของคลอสไฮโดรเจนไฮโดรเจนซัลไฟด์และซัลเฟอร์ไดออกไซด์ทำปฏิกิริยากับตัวเร่งปฏิกิริยาเพื่อผลิตกำมะถันและน้ำ.
ปริมาณของอากาศเผาไหม้ถูกควบคุมอย่างเข้มงวดเพื่อเพิ่มการกู้คืนกำมะถันเช่นการรักษาปฏิกิริยาปริมาณสารสัมพันธ์ที่เหมาะสมไฮโดรเจนซัลไฟด์ 2: 1 ถึงก๊าซซัลเฟอร์ไดออกไซด์ผ่านเครื่องปฏิกรณ์ปลายน้ำ.
โดยปกติแล้วการกู้คืนกำมะถันสูงถึง 97% สามารถทำได้ (US Library of Medicine, 2011).
2- เคมีวิเคราะห์
เป็นเวลากว่าศตวรรษที่ไฮโดรเจนซัลไฟด์มีความสำคัญในการวิเคราะห์ทางเคมีในการวิเคราะห์อนินทรีย์เชิงคุณภาพของไอออนโลหะ.
ในการวิเคราะห์เหล่านี้ไอออนของโลหะหนัก (และไม่ใช่โลหะ) จะตกตะกอน (เช่น Pb (II), Cu (II), Hg (II), As (III) จากสารละลายหลังจากสัมผัสกับ H2S การตกตะกอนที่เกิดขึ้นจะละลายอีกครั้งด้วยการเลือกบางส่วนและจะถูกระบุดังนั้น.
3- การใช้งานอื่น ๆ
สารประกอบนี้ยังใช้เพื่อแยกดิวเทอเรียมออกไซด์หรือน้ำหนักออกจากน้ำธรรมดาผ่านกระบวนการซัลไฟด์ Girdler.
นักวิทยาศาสตร์ที่ University of Exeter ค้นพบว่าการได้รับก๊าซไฮโดรเจนซัลไฟด์จากเซลล์เพียงเล็กน้อยสามารถป้องกันความเสียหายจากไมโตคอนเดรีย.
เมื่อเซลล์ถูกตรึงด้วยโรคเอนไซม์จะถูกดึงดูดไปยังเซลล์เพื่อผลิตไฮโดรเจนซัลไฟด์ในปริมาณเล็กน้อย การศึกษาครั้งนี้อาจมีผลกระทบมากขึ้นในการป้องกันจังหวะโรคหัวใจและโรคข้ออักเสบ (Stampler, 2014).
ไฮโดรเจนซัลไฟด์สามารถมีคุณสมบัติต่อต้านริ้วรอยโดยการปิดกั้นสารเคมีทำลายภายในเซลล์มีคุณสมบัติคล้ายกับ resveratrol สารต้านอนุมูลอิสระที่พบในไวน์แดง.
การอ้างอิง
- เอเจนซี่สำหรับสารพิษและสำนักทะเบียนโรค (2011, 3 มีนาคม). ไฮโดรเจนซัลไฟด์คาร์บอนิลซัลไฟด์. สืบค้นจาก atsdr.cdc.gov.
- Al-Tawfiq, B. D. (2010) การได้รับไฮโดรเจนซัลไฟด์ในผู้ชายที่เป็นผู้ใหญ่. พงศาวดารของ Saudi Med. 30 (1) , 76-80.
- EMBL-EBI (2005, 13 ธันวาคม). ไฮโดรเจนซัลไฟด์. กู้คืนจาก ebi.ac.uk.
- สารานุกรมบริทานิก้า ( S.F. ). ไฮโดรเจนซัลไฟด์. กู้คืนจาก britannica.com.
- ฐานข้อมูลเมตาโบโลเมของมนุษย์ (2017, 2 มีนาคม). ไฮโดรเจนซัลไฟด์ . เรียกดูจาก hmdb.ca.
- ซัลเฟตในน้ำ. (2016) สืบค้นจาก cameochemicals.noaa.gov.
- (2016, 17 ตุลาคม). เอกสารข้อมูลความปลอดภัยของไฮโดรเจนซัลไฟด์. กู้คืนจาก praxair.com.
- ราชสมาคมเคมี (2015). ไฮโดรเจนซัลไฟด์. ดึงมาจาก chemspider.com.
- Stampler, L. (2014, 11 กรกฎาคม). สารประกอบที่มีกลิ่นเหม็นอาจช่วยป้องกันความเสียหายของเซลล์ได้. เรียกดูจาก time.com.
- หอสมุดแห่งชาติการแพทย์ (2011, 22 กันยายน). ธาตุกำมะถัน. สืบค้นจาก toxnet.nlm.nih.gov.


